题目内容
下表是元素周期表的一部分,回答下列有关问题:
(1)在这些元素中,最活泼的金属元素是 ,最活泼的非金属元素是 ,最不活泼的元素是 .(以上均填元素符号)
(2)在这些元素的最高价氧化物对应的水化物中,酸性最强的酸是 ,碱性最强的碱是 ,呈两性的氢氧化物是 .(以上均填化学式)
(3)(2)和(8)的气态氢化物的沸点比较高的是 (填化学式),原因是 .
(4)在(3)与(4)中,化学性质较活泼的是 (填元素符号),证明该结论的化学实验是 .
(5)在(8)和(12)形成的单质中,化学性质较活泼的是 (填化学式),证明该结论的化学实验是 .(用化学方程式表示)
族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | (1) | (2) | ||||||
| 3 | (3) | (4) | (5) | (6) | (7) | (8) | (9) | |
| 4 | (10) | (11) | (12) |
(2)在这些元素的最高价氧化物对应的水化物中,酸性最强的酸是
(3)(2)和(8)的气态氢化物的沸点比较高的是
(4)在(3)与(4)中,化学性质较活泼的是
(5)在(8)和(12)形成的单质中,化学性质较活泼的是
考点:元素周期表的结构及其应用,元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:由元素在周期表的位置可知,(1)~(12)元素分别为N、F、Na、Mg、Al、Si、S、Cl、Ar、K、Ca、Br,
(1)最活泼金属在元素周期表左下角,最活泼非金属在元素周期表右上方,稀有气体的性质最不活泼;
(2)Cl的最高价氧化物对应的水化物酸性最强,K的最高价氧化物对应的水化物碱性最强,Al的最高价氧化物对应的水化物有两性;
(3)HF中含氢键,沸点高;
(4)同周期,从左向右金属性减弱,利用与水或酸反应的剧烈程度分析;
(5)同主族,从上到下非金属性减弱,利用单质之间的置换反应证明.
(1)最活泼金属在元素周期表左下角,最活泼非金属在元素周期表右上方,稀有气体的性质最不活泼;
(2)Cl的最高价氧化物对应的水化物酸性最强,K的最高价氧化物对应的水化物碱性最强,Al的最高价氧化物对应的水化物有两性;
(3)HF中含氢键,沸点高;
(4)同周期,从左向右金属性减弱,利用与水或酸反应的剧烈程度分析;
(5)同主族,从上到下非金属性减弱,利用单质之间的置换反应证明.
解答:
解:由元素在周期表的位置可知,(1)~(12)元素分别为N、F、Na、Mg、Al、Si、S、Cl、Ar、K、Ca、Br,
(1)最活泼金属为K,最活泼非金属为F,Ar的性质最不活泼,故答案为:K;F;Ar;
(2)Cl的最高价氧化物对应的水化物HClO4酸性最强,K的最高价氧化物对应的水化物KOH的碱性最强,呈两性的氢氧化物是Al(OH)3,
故答案为:HClO4;KOH;Al(OH)3;
(3)HF中含氢键,沸点高遇HBr,故答案为:HF;分子间存在氢键;
(4)同周期,从左向右金属性减弱,则化学性质活泼的为Na,与水或酸反应钠比镁剧烈可说明,
故答案为:Na;与水或酸反应钠比镁剧烈;
与水或酸反应的剧烈程度分析;
(5)同主族,从上到下非金属性减弱,则化学性质较活泼的是Cl2,如Cl2+2KBr=2KCl+Br2可证明,
故答案为:Cl2;Cl2+2KBr=2KCl+Br2.
(1)最活泼金属为K,最活泼非金属为F,Ar的性质最不活泼,故答案为:K;F;Ar;
(2)Cl的最高价氧化物对应的水化物HClO4酸性最强,K的最高价氧化物对应的水化物KOH的碱性最强,呈两性的氢氧化物是Al(OH)3,
故答案为:HClO4;KOH;Al(OH)3;
(3)HF中含氢键,沸点高遇HBr,故答案为:HF;分子间存在氢键;
(4)同周期,从左向右金属性减弱,则化学性质活泼的为Na,与水或酸反应钠比镁剧烈可说明,
故答案为:Na;与水或酸反应钠比镁剧烈;
与水或酸反应的剧烈程度分析;
(5)同主族,从上到下非金属性减弱,则化学性质较活泼的是Cl2,如Cl2+2KBr=2KCl+Br2可证明,
故答案为:Cl2;Cl2+2KBr=2KCl+Br2.
点评:本题考查元素周期表及应用,为高频考点,把握元素在周期表的位置及元素周期律为解答的关键,注意金属性、非金属性比较方法的归纳,题目难度不大.

练习册系列答案
相关题目
相同温度下,醋酸在醋酸钠溶液和水中的电离常数分别为K1和K2,其大小关系正确的是( )
| A、K1>K2 |
| B、K1=K2 |
| C、K1<K2 |
| D、不能确定 |
下列溶液中的Cl-物质的量与100mL 1mol?L-1 AlCl3溶液中Cl-相等的是( )
| A、150mL 1mol?L-1氯化钠溶液 |
| B、75mL 2mol?L-1氯化镁溶液 |
| C、50mL 3mol?L-1氯化钾溶液 |
| D、50mL 1mol?L-1氯化铁溶液 |
下列离子方程式书写正确的是( )
| A、等物质的量的CO2与氢氧化钠溶液反应:CO2+2OH-═CO32-+H2O | ||||
| B、少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-═CaSO3↓+2HClO | ||||
| C、氢氧化钙溶液与等物质的量的稀H2SO4混合:Ca2++OH-+H++SO42-═CaSO4↓+H2O | ||||
D、用石墨电极电解饱和食盐水:2H2O+2Cl-
|
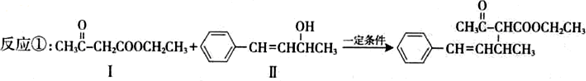
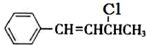 可生成化合物Ⅱ,所需的反应条件为
可生成化合物Ⅱ,所需的反应条件为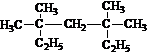 系统命名为
系统命名为