题目内容
19.下列分离或提纯物质的方法正确的是( )| A. | 用蒸发法进行海水淡化 | |
| B. | 用酒精萃取碘水中的碘 | |
| C. | 用渗析的方法除去淀粉溶液中含有的少量NaCl | |
| D. | 用加热→蒸发的方法可以除去粗盐中的CaCl2、MgCl2等杂质 |
分析 A.海水中水的沸点较低;
B.酒精与水互溶;
C.淀粉不能透过半透膜,而氯化钠可以;
D.加热→蒸发不能除去可溶性离子.
解答 解:A.海水中水的沸点较低,应选择蒸馏法进行海水淡化,而利用蒸发海水获得NaCl,故A错误;
B.酒精与水互溶,则不能选择酒精萃取碘水中的碘,应选苯或四氯化碳萃取碘水中的碘,故B错误;
C.淀粉不能透过半透膜,而氯化钠可以,则用渗析的方法除去淀粉溶液中含有的少量NaCl,故C正确;
D.加热→蒸发不能除去可溶性离子,则应选碳酸钠、NaOH将CaCl2、MgCl2等转化为沉淀,然后过滤、蒸发,故D错误;
故选C.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异、混合物分离提纯为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
10.下列叙述正确的是( )
| A. | 氯化钠溶液在电流作用下电离成钠离子和氯离子的过程叫电离 | |
| B. | 凡溶于水后能电离出氢离子的化合物都是酸 | |
| C. | 二氧化碳溶于水后能导电,故二氧化碳属于电解质 | |
| D. | 硫酸钡难溶于水,但溶解部分完全电离,故硫酸钡是强电解质 |
11.对于N2(g)+3H2(g)?2NH3(g)△H<0的反应,达到化学平衡状态的标志为( )
| A. | 断开1个N≡N键的同时有6个N-H键生成 | |
| B. | 混合气体的密度不变 | |
| C. | 混合气体的平均相对分子质量不变 | |
| D. | N2、H2、NH3分子数之比为1:3:2的状态 |
14.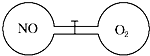 一定温度下,两个体积相等的连通容器用活塞分开,左右两室各充入一定量NO和O2,恰好使两容器内气体密度相同,打开活塞,充分混合反应.下列判断正确的是(不考虑NO2转化为N2O4)( )
一定温度下,两个体积相等的连通容器用活塞分开,左右两室各充入一定量NO和O2,恰好使两容器内气体密度相同,打开活塞,充分混合反应.下列判断正确的是(不考虑NO2转化为N2O4)( )
 一定温度下,两个体积相等的连通容器用活塞分开,左右两室各充入一定量NO和O2,恰好使两容器内气体密度相同,打开活塞,充分混合反应.下列判断正确的是(不考虑NO2转化为N2O4)( )
一定温度下,两个体积相等的连通容器用活塞分开,左右两室各充入一定量NO和O2,恰好使两容器内气体密度相同,打开活塞,充分混合反应.下列判断正确的是(不考虑NO2转化为N2O4)( )| A. | 最终容器内无O2存在 | B. | 反应前、后左室气体压强不变 | ||
| C. | 反应前、后右室气体密度不变 | D. | 开始时左右两室气体分子数相同 |


 利用图装置,可以模拟铁的电化学防护.
利用图装置,可以模拟铁的电化学防护.