题目内容
8.往磷酸钠溶液中加入足量盐酸,可发生如下反应:Na3PO4+3HCl→H3PO4+3NaCl,但把浓磷酸跟氯化钠固体混合后加热,又可发生如下反应:H3PO4+NaCl$\stackrel{△}{→}$NaH2PO4+HCl↑,请问为什么第一个反应是用盐酸制磷酸,而第二个反应却能用H3PO4制HCl?(提示:注意反应物HCl和生成物HCl的状态)分析 盐酸为强酸,酸性比磷酸强,但盐酸易挥发,磷酸沸点较高,以此解答该题.
解答 解:盐酸酸性比磷酸强,则在往磷酸钠溶液中加入足量盐酸,可生成磷酸,由于磷酸的沸点较高,难以挥发,但盐酸易挥发,可用浓磷酸跟氯化钠固体混合后加热,可制备HCl,
答:盐酸酸性比磷酸强,可制备磷酸,盐酸易挥发,磷酸难挥发,可用浓磷酸制备HCl.
点评 本题考查酸性的比较以及反应原理的探究,侧重于学生的分析、实验能力的考查,注意把握物质的性质以及反应原理的把握,难度不大.

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
19.下列分离或提纯物质的方法正确的是( )
| A. | 用蒸发法进行海水淡化 | |
| B. | 用酒精萃取碘水中的碘 | |
| C. | 用渗析的方法除去淀粉溶液中含有的少量NaCl | |
| D. | 用加热→蒸发的方法可以除去粗盐中的CaCl2、MgCl2等杂质 |
3.在下列叙述中,不正确的是( )
| A. | 40K和40Ca原子中的质子数和中子数都不相等 | |
| B. | H2和D2互为同位素 | |
| C. | 互为同位素的原子,它们的原子核内的中子数一定不相等 | |
| D. | 互为同位素的原子,它们原子核内的质子数一定相等 |
13.NPG的结构式如图,有关NPG说法错误的是( )


| A. | NPG与乙二醇互为同系物 | |
| B. | 1mol该醇与足量的钠反应放出1mol H2 | |
| C. | NPG一定条件下能发生取代反应、酯化反应、氧化反应、加成反应、加聚反应 | |
| D. | 分子式为C5H12O2 |
5.某无色透明的溶液能够与铝作用生成氢气,则在此溶液中一定能大量共存的离子组是( )
| A. | HCO3-、NO3-、Ba2+、Cl- | B. | Na+、Ba2+、Cl-、NO3- | ||
| C. | K+、NH4+、Cl-、OH- | D. | Na+、K+、SO42-、I- |
2.氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性;还原剂的还原性大于还原产物的还原性.现有以下反应( )
①Cl2+2KBr═2KCl+Br2,②KClO3+6HCl═3Cl2+KCl+3H2O,③2KBrO3+Cl2═Br2+2KClO3,
下列说法正确的是.
①Cl2+2KBr═2KCl+Br2,②KClO3+6HCl═3Cl2+KCl+3H2O,③2KBrO3+Cl2═Br2+2KClO3,
下列说法正确的是.
| A. | 上述三个反应都有单质生成,所以都是置换反应 | |
| B. | 氧化性由强到弱顺序为 KBrO3>KClO3>Cl2>Br2 | |
| C. | 反应②中还原剂与氧化剂的物质的量之比为6:1 | |
| D. | ③中lmol还原剂反应则氧化剂得到电子的物质的量为2mol |
 、醛基-CHO、羧基-COOH、-COOR酯基.
、醛基-CHO、羧基-COOH、-COOR酯基.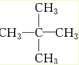 ,名称为2,2-二甲基丙烷.
,名称为2,2-二甲基丙烷.
