题目内容
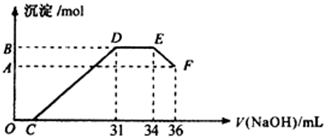
1.氧化锌为白色粉末,可用于湿疹、癣等皮肤病的治疗.纯化工业级氧化锌(含有Fe(+2价)、Mn(+2价)、Ni(+2价)等杂质)的流程如图所示:
提示:在本实验条件下,Ni(+2价)不能被氧化;高锰酸钾的还原产物是MnO2.
回答下列问题:
(1)反应②中除掉的杂质离子是Fe2+和Mn2+,发生反应的离子方程式MnO4-+3Fe2++7H2O=3Fe(OH)3↓+MnO2↓+5H+、2MnO4-+3Mn2++2H2O=5MnO2↓+4H+;在加高锰酸钾溶液前,若pH较低,对除杂的影响是铁离子和锰离子不能生成沉淀,从而无法除去铁和锰杂质.
(2)反应③过滤得到的滤渣成分为锌、镍.
(3)反应④形成的沉淀要用水洗,检查沉淀是否洗涤干净的方法是取最后一次少量水洗液于试管中,滴入1~2滴稀盐酸,再滴入氯化钡溶液,若无白色沉淀生成,则说明沉淀已经洗涤干净.
(4)反应④中产物的成分可能是ZnCO3•xZn(OH)2.取干燥后的滤饼10.55g,锻烧后可得到产品8.1g,则x等于3.
分析 纯化工业级氧化锌和稀硫酸反应导致溶液中存在Fe2+、Mn2+、Zn2+和Ni2+,向浸出液中加入适量高锰酸钾溶液并调节溶液的pH约为5,Ni(Ⅱ)不能被氧化,Fe2+、Mn2+被氧化而被除去,同时溶液中有MnO2生成,过滤后,向滤液中加入Zn过滤,Zn和Ni2+发生氧化还原反应生成Ni,溶液中存在Zn2+,向滤液中加入碳酸钠溶液,生成碳酸锌沉淀,煅烧碳酸锌沉淀生成ZnO,
(1)根据题意,Ni(Ⅱ)不能被氧化,反应②中除掉的杂质离子是Fe2+和Mn2+,根据MnO4-+具有氧化性,能将Fe2+和Mn2+氧化,根据电子得失进行配平;加高锰酸钾溶液前,若pH较低,铁离子和锰离子不能生成沉淀,从而无法除去铁和锰杂质.
(2)反应③为锌与镍离子的发生反应得到锌离子和镍;得到的滤渣中,除了过量的锌外还有金属镍.
(3)检验沉淀是否洗涤干净的方法是最后一次洗涤液,检验表面是否含有硫酸根离子;
(4)根据关系式ZnCO3•xZn(OH)2~(x+1)ZnO来计算.
解答 解:纯化工业级氧化锌和稀硫酸反应导致溶液中存在Fe2+、Mn2+、Zn2+和Ni2+,向浸出液中加入适量高锰酸钾溶液并调节溶液的pH约为5,Ni(Ⅱ)不能被氧化,Fe2+、Mn2+被氧化而被除去,同时溶液中有MnO2生成,过滤后,向滤液中加入Zn过滤,Zn和Ni2+发生氧化还原反应生成Ni,溶液中存在Zn2+,向滤液中加入碳酸钠溶液,生成碳酸锌沉淀,煅烧碳酸锌沉淀生成ZnO,
(1)根据题意,Ni(Ⅱ)不能被氧化,反应②中除掉的杂质离子是Fe2+和Mn2+,发生的离子方程式为MnO4-+3Fe2++7H2O=3Fe(OH)3↓+MnO2↓+5H+、2MnO4-+3Mn2++2H2O=5MnO2↓+4H+;加高锰酸钾溶液前,若pH较低,铁离子和锰离子不能生成沉淀,从而无法除去铁和锰杂质;
故答案为:Fe2+和Mn2+;MnO4-+3Fe2++7H2O=3Fe(OH)3↓+MnO2↓+5H+、2MnO4-+3Mn2++2H2O=5MnO2↓+4H+;铁离子和锰离子不能生成沉淀,从而无法除去铁和锰杂质;
(2)得到的滤渣中,除了过量的锌外还有金属镍,故答案为:锌、镍;
(3)由于溶液中硫酸根离子属于杂质离子,因此可以检验测定洗涤液中是否存在硫酸根离子,操作为:取最后一次少量水洗液于试管中,滴入1~2滴稀盐酸,再滴入氯化钡溶液,若无白色沉淀生成,则说明沉淀已经洗涤干净,
故答案为:取最后一次少量水洗液于试管中,滴入1~2滴稀盐酸,再滴入氯化钡溶液,若无白色沉淀生成,则说明沉淀已经洗涤干净;
(4)根据关系式ZnCO3•xZn(OH)2 ~(x+1)ZnO
125+99x 81(x+1)
10.55g 8.1g
解得:x=3,
故答案为:3.
点评 本题考查混合物的分离和提纯,侧重考查学生分析问题、解答问题能力,明确流程图中各个步骤发生的反应及溶液中存在的微粒,知道常见离子的检验方法及实验现象,题目难度中等.

 阅读快车系列答案
阅读快车系列答案| A. | 金刚石 | B. | 氟化镁 | C. | 冰 | D. | 金属钾 |
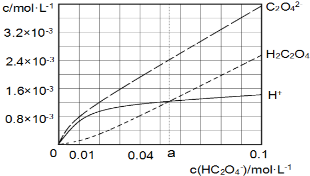 25℃时,往水中不断加入NaHC2O4固体,部分微粒浓度随c(HC2O4)的变化趋势如下图所示.下列说法正确的是( )
25℃时,往水中不断加入NaHC2O4固体,部分微粒浓度随c(HC2O4)的变化趋势如下图所示.下列说法正确的是( )| A. | 当c(HC2O4ˉ)=0.1mol•Lˉ1时,c(H+)>c(C2O42-)-c(H2C2O4) | |
| B. | 当c(HC2O4ˉ)>amol•Lˉ1时,c(H+)<c(H2C2O4),HC2O4ˉ的水解程度大于电离程度 | |
| C. | HC2O4ˉ?C2O42-+H+,Ka(HC2O4ˉ)=a | |
| D. | 将0.08mol•Lˉ1H2C2O4溶液与等浓度NaOH溶液等体积混合后(忽略体积变化),c(Na+)>c(HC2O4ˉ)>c(C2O42-)>c(H2C2O4)>c(H+)>c(OHˉ) |
CO(g)+2H2(g)?CH3OH(g)△H
(1)上述物质的有关化学键的键能(单位:kJ•mol-1)数据如下
C≡0:1076,H-H:436,C-H:408,C-O:351,O-H:463;
①上述生成CH3OH的反应的△H=-90kJ/mol.
②若2CO(g)+4H2(g)═CH3OCH3(g)+H2O(g)△H=-204.7kJ•mol-1,一定条件下,CH3OH(g)可进一步转化为CH30CH3(g)与H2O(g),试写出对应的热化学方程式:2CH3OH(g)=CH3OCH3(g)+H2O(g)△H=-24.7kJ/mol.
(2)分别向a、b、c三个容积相同的恒容密封容器中冲入10molCO与20molH2,在适当条件下发生反应CO(g)+2H2(g)?CH3OH(g)△H,反应过程中H2的浓度(mol•L-1)随时间(min)的变化如图中a、b、c曲线所示.
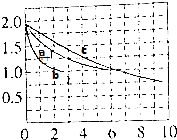
①b容器中的反应在3min时达到平衡,则b容器中v(CO)=$\frac{1}{6}$mol/(L.min).
②容器a、b中的反应条件的差异是b中使用催化剂,若a、c容器中的反应温度不同,则温度较低的容器是b(选填a或c).
③a容器中反应的平衡常数=1,三个容器中平衡常数相对大小关系为c>a=b.
为了寻找合成甲醇的适宜温度和压强,某科研小组设计了三组实验,部分实验数据如下表所示.
| 实验编号 | T(℃) | n(CO)/n(H2) | p(MPa) |
| ① | 160 | $\frac{2}{3}$ | 1 |
| ② | x | $\frac{2}{3}$ | 5 |
| ③ | 260 | y | 5 |
| A. | 用惰性电极电解氯化钠溶液:2Cl-+2H+═H2↑+Cl2↑ | |
| B. | 向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- | |
| C. | Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O | |
| D. | Fe(NO3)2 溶液中滴加少量稀盐酸:Fe2++NO3-+4H+═Fe3++NO↑+2H2O |
 .
. .
. 有如下化学反应:2A(g)+B(g)?2C(g),△H<0.
有如下化学反应:2A(g)+B(g)?2C(g),△H<0.