题目内容
用NA表示阿伏加德罗常数,下列叙述不正确的是( )
| A、1 mol CO2 的体积为22.4L |
| B、CO2的摩尔质量为44g |
| C、64g SO2含有氧原子数2NA |
| D、NA个CO2的质量(g)与CO2的相对分子质量数值相同 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、不知 CO2 所处的状态,故无法计算体积;
B、摩尔质量的单位为g/mol;
C、根据n=
并结合 SO2的分子式来计算;
D、根据n=
并结合一种物质的摩尔质量与其相对分子质量在数值上相等来分析.
B、摩尔质量的单位为g/mol;
C、根据n=
| m |
| M |
D、根据n=
| N |
| NA |
解答:
解:A、不知 CO2 所处的状态,即不知气体摩尔体积的数值,V=n?Vm,故无法计算气体的体积,故A错误;
B、摩尔质量的单位为g/mol,故B错误;
C、根据n=
可知SO2的物质的量n=
=1mol,根据二氧化硫的分子式SO2,可知1molSO2中含2mol氧原子,个数为2NA,故C正确;
D、NA个CO2的物质的量n=
=
=1mol,质量m=n?M=1mol×44g/mol=44g,而CO2的相对分子质量为44,但两者单位不同,故只是数值相同,故D正确;
故选AB.
B、摩尔质量的单位为g/mol,故B错误;
C、根据n=
| m |
| M |
| 64g |
| 64g/mol |
D、NA个CO2的物质的量n=
| N |
| NA |
| NA |
| NA |
故选AB.
点评:本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的运用以及物质的结构是解题关键,难度不大.

练习册系列答案
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
在pH=1的澄清透明溶液中,不能大量共存的离子组是( )
A、Al3+、Ag+、NO
| ||||
B、Cu2+、NH
| ||||
| C、Ba2+、K+、Cl-、Br- | ||||
D、Zn2+、Na+、NO
|
设NA表示阿伏加德罗常数,下列说法正确的是( )
A、1L1mol/L的Na2CO3溶液中含CO
| ||
| B、100mL 10mol/L的浓硝酸与足量铜反应,硝酸得到的电子数为0.5NA | ||
| C、常温下100mL0.1mol/L醋酸溶液中含醋酸分子0.01NA | ||
| D、0.1molNa2O2与足量水反应转移电子数0.1NA |
将一定量氯化钙溶于90g水中,欲使每100个水分子中含有1个Cl-,这一定量的氯化钙是( )
| A、0.3mol |
| B、0.025mol |
| C、0.05mol |
| D、5.55g |
有关常温下pH均为3的醋酸溶液和盐酸的说法正确的是( )
| A、两种溶液中,由水电离出的氢离子浓度均为l×10-11 mol?L-1 |
| B、分别加水稀释100倍后,两种溶液的pH仍相等 |
| C、中和同体积的这两种酸溶液所需要NaOH物质的量也相等 |
| D、分别加入足量锌片,两种溶液生成H2的体积相等 |
室温时,pH=10的氨水和Na2CO3溶液中,水电离产生的C(H+)前者与后者之比( )
| A、1:1 |
| B、10?10:10?4 |
| C、10?4:10?10 |
| D、10?10:10?7 |
过氧乙酸(CH3COOOH)是一种高效消毒剂,可以迅速杀灭多种微生物,包括多种病毒(如 SARS病毒)、细菌、真菌及芽孢.过氧乙酸可由冰醋酸与过氧化氢在一定条件下作用制得,有关过氧乙酸的叙述中正确的是( )
| A、过氧乙酸与羟基乙酸(HOCH2COOH)互为同分异构体 | ||
| B、因含有过氧基“-O-O-”而有强氧化性 | ||
C、由下列过氧乙酸的制取原理可以看出,过氧乙酸是酯的同系物CH3COOH+H2O2
| ||
| D、过氧乙酸易分解生成乙酸和氧气,不可直接用手接触原液,使用时不可稀释 |
关于下列装置说法正确的是( )
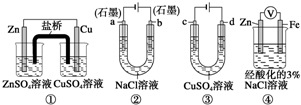

| A、装置②工作一段时间后,a极附近溶液的pH增大 |
| B、用装置③精炼铜时,c极为粗铜 |
| C、装置①中,盐桥中的K+移向ZnSO4溶液 |
| D、装置④中电子由Zn流向Fe,装置中有Fe2+生成 |



