题目内容
关于下列装置说法正确的是( )
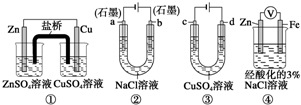

| A、装置②工作一段时间后,a极附近溶液的pH增大 |
| B、用装置③精炼铜时,c极为粗铜 |
| C、装置①中,盐桥中的K+移向ZnSO4溶液 |
| D、装置④中电子由Zn流向Fe,装置中有Fe2+生成 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A.装置②a电极上氢离子放电,同时电极附近生成氢氧根离子,b电极上氯离子放电;
B.电解精炼粗铜时,粗铜作阳极、纯铜作阴极;
C.含有盐桥的原电池中,盐桥中阳离子向正极所在溶液移动,阴离子向负极所在溶液移动;
D.该装置构成原电池,Zn易失电子作负极、Fe作正极,电子从负极沿导线流向正极.
B.电解精炼粗铜时,粗铜作阳极、纯铜作阴极;
C.含有盐桥的原电池中,盐桥中阳离子向正极所在溶液移动,阴离子向负极所在溶液移动;
D.该装置构成原电池,Zn易失电子作负极、Fe作正极,电子从负极沿导线流向正极.
解答:
解:A.装置②a电极上电极反应式为2H2O+2e-=2OH-+H2↑、b电极反应式为2Cl--2e-=Cl2↑,a电极附近有氢氧根离子生成,所以溶液pH增大,故A正确;
B.电解精炼粗铜时,粗铜作阳极、纯铜作阴极,则c为纯铜、d为粗铜,故B错误;
C.含有盐桥的原电池中,盐桥中阳离子向正极所在溶液移动,阴离子向负极所在溶液移动,该装置中Zn作负极、Cu作正极,则盐桥中的K+移向CuSO4溶液,故C错误;
D.该装置构成原电池,Zn易失电子作负极、Fe作正极,电子从负极Zn沿导线流向正极Fe,正极上氢离子放电生成氢气,所以溶液中没有亚铁离子生成,故D错误;
故选A.
B.电解精炼粗铜时,粗铜作阳极、纯铜作阴极,则c为纯铜、d为粗铜,故B错误;
C.含有盐桥的原电池中,盐桥中阳离子向正极所在溶液移动,阴离子向负极所在溶液移动,该装置中Zn作负极、Cu作正极,则盐桥中的K+移向CuSO4溶液,故C错误;
D.该装置构成原电池,Zn易失电子作负极、Fe作正极,电子从负极Zn沿导线流向正极Fe,正极上氢离子放电生成氢气,所以溶液中没有亚铁离子生成,故D错误;
故选A.
点评:本题考查原电池和电解池原理,明确各个电极上发生的反应、离子移动方向即可解答,知道盐桥的作用,题目难度不大.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
用NA表示阿伏加德罗常数,下列叙述不正确的是( )
| A、1 mol CO2 的体积为22.4L |
| B、CO2的摩尔质量为44g |
| C、64g SO2含有氧原子数2NA |
| D、NA个CO2的质量(g)与CO2的相对分子质量数值相同 |
下列说法不正确的是( )
| A、核磁共振仪、红外光谱仪、质谱仪、紫外光谱仪、元素分析仪、紫外可见分光光度计等都是定性或定量研究物质组成或结构的现代仪器 |
| B、利用元素周期律,人们在过渡元素中寻找各种性能优良的催化剂,使反应的温度降低并提高反应物的转化率,从而起到很好的节能效果 |
| C、化学家鲍林提出了氢键理论和蛋白质分子的螺旋结构模型,为DNA分子双螺旋结构模型的提出奠定了基础 |
| D、垃圾焚烧法已成为许多城市垃圾处理的主要方法之一,利用垃圾焚烧产生的热能发电或供热,能较充分的利用生活垃圾中的生物质能 |
下列叙述不正确的是( )
| A、Fe(OH)3 胶体进行电泳实验,阴极附近颜色加深 |
| B、在熔融态能导电的物质,该物质中一定含有离子键 |
| C、用渗析的方法可以除去蛋白质溶液中混有的少量NaCl |
| D、铜片做阳极,铁片做阴极,电解氯化铜溶液,铁片表面析出铜 |
20℃的纯水的pH和80℃的纯水的pH相比较( )
| A、前者大 | B、后者大 |
| C、相等 | D、无法判断 |
如图是部分短周期元素化合价与原子序数的关系图,下列说法不正确的是( )


| A、电负性:X>Y>Z |
| B、气态氢化物的稳定性及其水溶液的酸性:R>W |
| C、W、X形成的化合物以及它们与水反应生成物都是共价化合物 |
| D、Y、Z、W的最高价氧化物对应的水化物两两之间都能发生反应 |
25℃时,下列各组离子在制定溶液中能大量共存的是( )
A、澄清透明溶液中:K+ MnO
| ||
| B、含有较多SO32-的溶液:H+ Na+ ClO- Ca2+ | ||
| C、中性溶液中:K+ SO42- Fe3+ Cl- | ||
| D、滴入甲基橙显红色的溶液中:Cl- AlO2- NH4+ Ba2+ |
不能用有关胶体的观点解释的现象是( )
| A、在河流人海口处易形成三角洲 |
| B、在NaHCO3溶液中滴入CaCl2溶液,看不到沉淀 |
| C、少许FeCl3饱和溶液逐滴滴入沸水中,看不到红褐色沉淀 |
| D、同一支钢笔,同时使用不同牌号的墨水易发生堵塞 |