题目内容
9.有一瓶溶液,其中可能含有H+、K+、Ba2+、NH4+、Al3+、SO42-、CO32-、AlO2-和Cl-.取该溶液进行了以下实验:(1)用pH试纸检验,发现溶液显酸性;
(2)取部分溶液,加入NaOH 溶液使溶液从酸性变为碱性,此过程中均无沉淀生成;
(3)取部分上述碱性溶液,加Na2CO3溶液,有白色沉淀生成;
(4)将(2)得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝;
根据上述实验事实,可知原溶液中肯定含有的离子是H+、Ba2+、NH4+、Al3+、Cl-;肯定没有的离子是SO42-、CO32-、AlO2-;还不能确定是否含有的离子是K+,如何确定该离子是否存在焰色反应.
分析 (1)用pH试纸检验,发现溶液显酸性,说明含有H+,则不含CO32-、AlO2-;
(2)取部分溶液,加入NaOH 溶液使溶液从酸性变为碱性,此过程中均无沉淀生成,说明含有Al3+;
(3)取部分上述碱性溶液,加Na2CO3溶液,有白色沉淀生成,则含有Ba2+,则不含有SO42-,由溶液电中性可知一定含有Cl-;
(4)将(2)得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝,说明含有NH4+,以此解答该题.
解答 解:(1)用pH试纸检验,发现溶液显酸性,说明含有H+,则不含CO32-、AlO2-;
(2)取部分溶液,加入NaOH 溶液使溶液从酸性变为碱性,此过程中均无沉淀生成,说明含有Al3+;
(3)取部分上述碱性溶液,加Na2CO3溶液,有白色沉淀生成,则含有Ba2+,则不含有SO42-,由溶液电中性可知一定含有Cl-;
(4)将(2)得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝,说明含有NH4+,
不能确定的离子为,可用焰色反应鉴别,
故答案为:H+、Ba2+、NH4+、Al3+、Cl-;SO42-、CO32-、AlO2-;K+;焰色反应.
点评 本题考查了常见的离子检验方法,题目难度中等,涉及的离子之间的反应较多,注意根据有关离子间的反应和现象分析,充分考查了学生的分析、理解能力及灵活应用所学知识的能力.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
1.如图是产生和收集气体的实验装置示意图,该装置适合于( )


| A. | 用H2O2溶液和MnO2制取O2 | B. | 用浓盐酸和MnO2制取Cl2 | ||
| C. | 用稀硝酸和Cu制取NO | D. | 用NH4Cl和Ca(OH)2制取NH3 |
19.下列有关化学用语表示不正确的是( )
| A. | 丙烯醛的结构简式:CH2═CHCHO | |
| B. | CSO的电子式: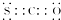 | |
| C. | 硫酸氢钠熔融时的电离方程式:NaHSO4═Na++HSO4- | |
| D. | S2-的结构示意图: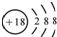 |
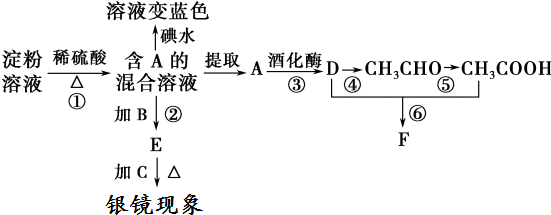
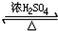 CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O

 现有A、B、C、D、E、F原子序数依次增大的六种元素,它们均位于元素周期表有前四周期,A与B位于不同周期且B元素的原子含有3个能级,B元素原子的每个能级所含的电子数相同;D的原子核外有8个运动状态不同的电子;E元素与F元素处于同一周期相邻的族,它们的原子序数相差3,且E元素的基态原子有4个未成对电子.请回答下列问题:
现有A、B、C、D、E、F原子序数依次增大的六种元素,它们均位于元素周期表有前四周期,A与B位于不同周期且B元素的原子含有3个能级,B元素原子的每个能级所含的电子数相同;D的原子核外有8个运动状态不同的电子;E元素与F元素处于同一周期相邻的族,它们的原子序数相差3,且E元素的基态原子有4个未成对电子.请回答下列问题: