题目内容
14.设NA表示阿伏加德罗常数,下列说法正确的是( )| A. | 22.4L氮气中含NA个氮原子 | |
| B. | 在标准状况下,1mol水的体积约为22.4L | |
| C. | 0.3 mol•L-1Na2SO4溶液中含0.6NA个Na+ | |
| D. | 18 g水中所含的氢原子数目为2NA |
分析 A、氮气所处的状态不明确;
B、标况下水为液态;
C、溶液体积不明确;
D、求出水的物质的量,然后根据水中含2个H原子来分析.
解答 解:A、氮气所处的状态不明确,故其物质的量无法计算,则含有的N原子个数无法计算,故A错误;
B、标况下水为液态,故1mol水的体积小于22.4L,故B错误;
C、溶液体积不明确,故溶液中的钠离子的个数无法计算,故C错误;
D、18g水的物质的量为1mol,而水中含2个H原子,故1mol水中含2NA个H原子,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
5.表是元素周期表的一部分,根据所给的10种元素,完成以下各小题.
(1)镁的原子结构示意图为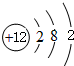 .
.
(2)H2SO4与HClO4中,酸性较强的是HClO4.
(3)NaOH与Al(OH)3中,属于两性氢氧化物的是Al(OH)3,它常用作治疗胃酸(含盐酸)过多的药物,该反应的化学方程式为Al(OH)3+3HCl═AlCl3+3H2O.
(4)碳元素形成的一种氧化物的化学式是CO或CO2,该物质中C元素与O元素的质量比为3:4(或3:8).(相对原子质量:C-12 O-16)
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | C | N | O | Ne | ||||
| 3 | Na | Mg | Al | Si | S | Cl |
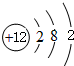 .
.(2)H2SO4与HClO4中,酸性较强的是HClO4.
(3)NaOH与Al(OH)3中,属于两性氢氧化物的是Al(OH)3,它常用作治疗胃酸(含盐酸)过多的药物,该反应的化学方程式为Al(OH)3+3HCl═AlCl3+3H2O.
(4)碳元素形成的一种氧化物的化学式是CO或CO2,该物质中C元素与O元素的质量比为3:4(或3:8).(相对原子质量:C-12 O-16)
2.下列物质属于纯净物的是( )
| A. | 氢氧化铁胶体 | B. | 碘酒 | C. | 胆矾(CuSO4•5H2O ) | D. | 生铁 |
9.下列各项中表达正确的是( )
| A. | 第VⅡA族元素形成的氢化物中沸点最高的是HI | |
| B. | 第三周期元素形成的简单离子中,半径最小的是Al3+ | |
| C. | 用电子式表示HCl形成过程: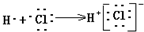 | |
| D. | 水分子很稳定性是因为水分子间易形成氢键 |
4.金刚石和石墨是碳元素的两种结构不同的单质(同素异形体).在 100kPa 时,含 1mol 碳原子的石墨转化为金刚石,要吸收 1.895kJ 的热量.据此试判断下列结论正确的是( )
| A. | 金刚石比石墨稳定 | |
| B. | 石墨比金刚石稳定 | |
| C. | 含 1mol 碳原子的石墨比含 1mol 碳原子的金刚石总能量高 | |
| D. | 石墨和金刚石互为同位素 |