题目内容
5.含碘食盐中加的碘一般是碘酸钾,下列说法正确的是( )| A. | 碘酸钾易挥发 | |
| B. | 碘酸钾是盐 | |
| C. | 用淀粉就能直接检验碘盐中的碘酸钾 | |
| D. | 碘酸钾可氧化氯化钠 |
分析 A.离子晶体沸点较高,常温下为固体,难挥发;
B.盐是指由金属离子和酸根离子构成的化合物;
C.淀粉试液能检验碘单质,不能检验含碘元素的化合物;
D.碘酸钾和氯化钠不反应.
解答 解:A.碘酸钾为钾离子和碘酸根离子构成的离子化合物,常温下为固体,沸点较高,难挥发,故A错误;
B.碘酸钾为钾离子和碘酸根离子构成的化合物,属于盐,故B正确;
C.碘遇淀粉试液变蓝色,所以淀粉试液能检验碘单质,食盐中含有碘酸钾而不是碘单质,淀粉试液和碘酸钾不反应,所以不能用淀粉检验碘盐中的碘酸钾,故C错误;
D.氯和碘属于同一主族,氯的非金属性强于碘,碘酸钾不能氧化氯化钠,故D错误;
故选B.
点评 本题考查了碘及其化合物的性质,注意碘遇淀粉试液变蓝色是碘单质的特性,不是含碘化合物,可以据此现象确定碘单质的存在,题目难度不大.

练习册系列答案
相关题目
15.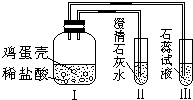 某同学做“证明鸡蛋壳的主要成分是碳酸盐”的实验时,设计了如图所示的方案.经检验装置气密性合格并加入试剂.下列说法中不正确的是( )
某同学做“证明鸡蛋壳的主要成分是碳酸盐”的实验时,设计了如图所示的方案.经检验装置气密性合格并加入试剂.下列说法中不正确的是( )
 某同学做“证明鸡蛋壳的主要成分是碳酸盐”的实验时,设计了如图所示的方案.经检验装置气密性合格并加入试剂.下列说法中不正确的是( )
某同学做“证明鸡蛋壳的主要成分是碳酸盐”的实验时,设计了如图所示的方案.经检验装置气密性合格并加入试剂.下列说法中不正确的是( )| A. | 鸡蛋壳发生了分解反应 | |
| B. | Ⅰ中发生的现象为鸡蛋壳逐渐溶解,产生大量气泡 | |
| C. | II中的澄清石灰水变浑浊 | |
| D. | III中紫色石蕊试液变红 |
16.将一定质量的甲烷和一氧化碳的混合气体在足量的氧气中充分燃烧,将生成物依次通入盛有足量浓硫酸和氢氧化钠溶液的洗气瓶,实验测得装有浓硫酸的洗气瓶增重5.4克,装有氢氧化钠溶液的洗气瓶增重8.8克.混合气体中甲烷和一氧化碳的物质的量之比为( )
| A. | 12:7 | B. | 3:1 | C. | 1:3 | D. | 1:1 |
13.“绿色化学”的主要内容之一是指从技术、经济上设计可行的化学反应,使原子充分利用,不产生污染物.下列化学反应符合“绿色化学”理念的是( )
| A. | 制CuSO4:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O | |
| B. | 制CuSO4:CuO+H2SO4(稀)=CuSO4+H2O | |
| C. | 制Cu(NO3)2:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O | |
| D. | 制Cu(NO3)2:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O |
10.下列过程的△H<0的是( )
| A. | Ba(OH)2•8H2O晶体和NH4Cl晶体混合反应 | |
| B. | 煅烧石灰石 | |
| C. | CH3COOH?CH3COO-+H+ | |
| D. | 生石灰溶于水 |
14.下列关于次氯酸的说法不正确的是( )
| A. | 次氯酸是一种弱酸 | B. | 次氯酸具有强还原性 | ||
| C. | 次氯酸不稳定,见光分解 | D. | 次氯酸具有漂白性 |
15.常温下,将一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如表:
下列判断正确的是( )
| 实验编号 | c(HA)/mol•L-1 | c(NaOH)/mol•L-1 | 混合溶液的pH |
| 甲 | 0.1 | 0.1 | pH=a |
| 乙 | 0.2 | 0.2 | pH=9 |
| 丙 | c1 | 0.2 | pH=7 |
| 丁 | 0.2 | 0.1 | pH<7 |
| A. | a=7 | |
| B. | 在乙组混合液中由水电离出的c(OH-)=10-5 mol•L-1 | |
| C. | c1=0.2 | |
| D. | 丁组混合液中:c(Na+)>c(A-)>c(H+)>c(OH-) |