题目内容
20.向MgSO4和Al2(SO4)3的混合溶液中,逐滴加入NaOH溶液.下列图象中,能正确表示上述反应的是(横坐标表示加入NaOH溶液的体积,纵坐标表示反应生成沉淀的质量)( )| A. | 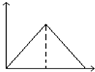 | B. | 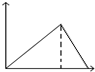 | C. | 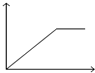 | D. | 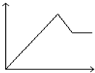 |
分析 根据发生的反应Mg2++2OH-═Mg(OH)2↓、Al3++3OH-═Al(OH)3↓、Al(OH)3+OH-═AlO2-+2H2O来分析.
解答 解:因横坐标表示加入NaOH溶液的体积,纵坐标表示反应生成沉淀的质量,
则向MgSO4和Al2(SO4)3的混合溶液中,逐滴加入NaOH溶液,发生Mg2++2OH-═Mg(OH)2↓、Al3++3OH-═Al(OH)3↓,则沉淀的质量一直在增大,直到最大;然后发生Al(OH)3+OH-═AlO2-+2H2O,沉淀的质量减少,但氢氧化镁不与碱反应,则最后沉淀的质量为一定值,显然只有D符合,
故选D.
点评 本题考查了化学反应与图象的关系,明确图象中坐标及点、线、面的意义,结合物质的溶解性来分析解答,注意氢氧化铝能溶于强碱但不溶于弱碱,题目难度不大.

练习册系列答案
 优百分课时互动系列答案
优百分课时互动系列答案
相关题目
10.某溶液中含有HCO3-、SO32-、K+、Na+ 四种离子,若向其中加少量Na2O2固体后,溶液中上述离子浓度基本保持不变的是( )
| A. | Na+ | B. | K+ | C. | SO32- | D. | HCO3- |
11.如表实验中根据现象所得结论正确的是( )
| 操作 | 现象 | 结论 | |
| A | 向某未知溶液中加入盐酸酸化的BaCl2溶液 | 生成白色沉淀 | 该溶液中一定含有SO42- |
| B | 用一束强光照射Na2SiO3溶液 | 溶液中出现一条光亮的通路 | 溶液中可能含有硅酸胶体 |
| C | 向盛有Fe(NO3)2溶液的试管中滴入几滴0.1mol/LH2SO4溶液 | 试管口出现红棕色气体 | 溶液中NO3-被Fe2+还原为NO2 |
| D | 淀粉溶液中加稀硫酸,加热片刻后再滴加银氨溶液,并用水浴加热 | 无银镜生成 | 淀粉未发生水解 |
| A. | A | B. | B | C. | C | D. | D |
5.含碘食盐中加的碘一般是碘酸钾,下列说法正确的是( )
| A. | 碘酸钾易挥发 | |
| B. | 碘酸钾是盐 | |
| C. | 用淀粉就能直接检验碘盐中的碘酸钾 | |
| D. | 碘酸钾可氧化氯化钠 |
12.2L 1mol•L-1 AlCl3溶液与1L 2mol•L-1 NaCl溶液中的Cl-的物质的量浓度之比( )
| A. | 3:1 | B. | 1:2 | C. | 3:2 | D. | 1:1 |
9.下列叙述中,你认为科学的是( )
| A. | 某广告语:本饮料含淀粉,糖尿病人可以大量食用 | |
| B. | 到城乡结合处燃放鞭炮,可避免污染环境 | |
| C. | 淡水资源在地球上分布很广,取之不尽,用之不竭 | |
| D. | 大气中二氧化碳含量的增多是造成“温室效应”的主要原因 |
10.设NA为阿伏加罗常数的值,下列叙述正确的是( )
| A. | 在标况下,11.2 L NO与11.2 L O2混合后所含分子数为0.75NA | |
| B. | 常温常压下,16gO3所含的电子数为8NA | |
| C. | 5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$2HNO3+4N2↑+9H2O反应中,生成28gN2时,转移的电子数目为3.75NA | |
| D. | 铝跟氢氧化钠溶液反应生成1mol氢气时,转移的电子数为NA |
 ,反应类型取代反应.
,反应类型取代反应.