题目内容
15.下列有关物质分离的说法合理的是( )| A. | 除去KNO3中少量NaCl,将混合物制成热的饱和溶液,冷却结晶,过滤 | |
| B. | 除去氯化钙溶液中的氯化铁杂质,加生石灰调节溶液的pH为3.7,再过滤 | |
| C. | 除去乙烷中混有的少量乙烯,将混合气体通入足量酸性KMnO4溶液中 | |
| D. | 加热法除去Ca(0H)2固体中混有的NH4Cl固体. |
分析 A.硝酸钾和氯化钠的溶解度随温度的变化不同,可用重结晶法分离;
B.CaO促进铁离子水解;
C.乙烯被高锰酸钾氧化生成二氧化碳;
D.加热时氯化铵与Ca(0H)2反应生成氨气.
解答 解:A.硝酸钾和氯化钠的溶解度随温度的变化不同,则除去KNO3中少量NaCl,将混合物制成热的饱和溶液,冷却结晶,过滤可得到硝酸钾,故A正确;
B.生石灰促进氯化铁的水解,使铁离子转化为沉淀,则调节溶液的pH为3.7,再过滤即可除杂,故B正确;
C.乙烯被高锰酸钾氧化生成二氧化碳,引入新杂质,应选溴水、洗气可除杂,故C错误;
D.加热时氯化铵与Ca(0H)2反应生成氨气,则加热法不能除杂,故D错误;
故选AB.
点评 本题考查物质的分离、提纯,为高频考点,侧重于学生的分析能力、实验能力的考查,注意把握物质的性质的异同以及除杂的原则,题目难度不大.

练习册系列答案
相关题目
5.化学能与热能、电能等能相互转化.关于化学能与其他能量相互转化的说法正确的是( )
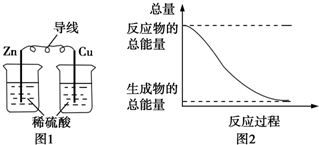

| A. | 图1所示的装置能将化学能转变为电能 | |
| B. | 图2所示的反应为吸热反应 | |
| C. | 中和反应中,反应物的总能量比生成物的总能量低 | |
| D. | 化学反应中能量变化的主要原因是化学键的断裂与生成 |
6.一定温度下,在体积为10L的密闭容器中,3molX和1molY进行应:2X(g)+Y(g)?Z(g),经2min达到平衡,生成0.6mol Z,下列说法正确的是( )
| A. | 以X浓度变化表示的反应速率为0.01 mol/(L•s) | |
| B. | 将容器体积变为20L,Z的平衡浓度为原来的1/2 | |
| C. | 若增大压强,则物质Y的转化率减小 | |
| D. | 若升高温度,X的体积分数增大,则该反应的△H<0 |
3.X、Y、Z、W是原子序数依次增大的短周期元素,Y、Z同周期且相邻,X、W同主族且与Y处于不同周期,Y、Z原子的电子数总和与X、W原子的电子数总和之比为5:4,下列说法正确的是( )
| A. | 原子半径:r(W)>r(Z)>r(Y)>r(X) | |
| B. | Y的简单气态氢化物的热稳定性比Z的强 | |
| C. | 由X、Z组成的化合物与由Z、W组成的化合物只能发生化合反应 | |
| D. | 由X、Y、Z三种元素组成的化合物可以是酸、碱或盐 |
10.下列说法不正确的是( )
| A. | C2H6和C9H20一定互为同系物 | |
| B. | 丙氨酸和苯丙氨酸脱水缩合,最多可生成3中二肽 | |
| C. | 葡萄糖在人体内被氧化,最终转化为二氧化碳和水,并释放能量 | |
| D. | 向鸡蛋清溶液中加入饱和(NH4)2SO4溶液,有沉淀析出,再加水沉淀会溶解 |
4.下列有关中和热测定实验叙述正确的是( )
| A. | 测定中和热时,大小两烧杯间填满碎纸的作用只是固定小烧杯 | |
| B. | 用50mL 0.50mo1•L-1的氢氧化钠溶液,分别与50mL 0.50mo1•L-1的盐酸和50mL 0.25mo1•L-1的硫酸充分反应,两反应测定的中和热相等 | |
| C. | 不能用铜丝代替玻璃棒搅拌酸碱混合液 | |
| D. | 酸碱混合时,量筒中NaOH溶液应缓缓倒入小烧杯中,不断用玻璃棒搅拌 |
11.其他条件不变的情况下,下列说法不正确的是( )
| A. | 对于反应nA(g)+B(g)?2C(g),平衡后增大压强,A的百分含量减小,则n≥2 | |
| B. | 对于反应2A(g)?B(g)△H<0,恒温恒容,压强不再变化说明反应达到平衡状态 | |
| C. | 对于反应2A(g)?B(g),恒温恒容条件下,气体密度不变,说明达到平衡状态 | |
| D. | 对于反应2A(g)?B(g),若v(A)正=2v(B)逆,说明反应达到平衡状态 |
8.2006年夏季,云南的某些湖泊发生水华现象,其原因是水体出现富营养化,使某些藻类迅速繁殖,导致水生生态系统的破坏.下列选项中能够使水体富营养化的物质是( )
| A. | 含氮、磷的化合物 | B. | 含氯的化合物 | C. | 含硫的化合物 | D. | 含碳的化合物 |
 某化学兴趣小组为了探究某些气体的性质,设计了如图所示的实验装置.实验时将A、D中产生的气体同时通入C中.(K为止水夹,部分夹持仪器已略去)
某化学兴趣小组为了探究某些气体的性质,设计了如图所示的实验装置.实验时将A、D中产生的气体同时通入C中.(K为止水夹,部分夹持仪器已略去)