题目内容
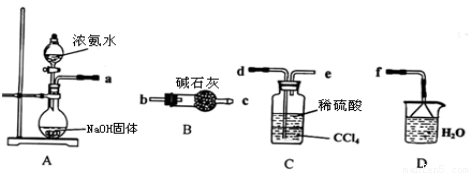
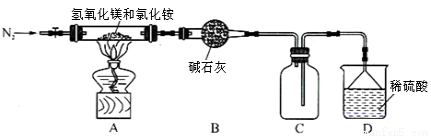
以下是在实验室模拟“侯氏制碱法”生产流程的示意图:则下列叙述错误的是( )


| A、A气体是NH3,B气体是CO2 |
| B、把纯碱及第Ⅲ步所得晶体与某些固体酸性物质(如酒石酸)混合可制泡腾片 |
| C、第Ⅲ步操作用到的主要玻璃仪器是烧杯、漏斗、玻璃棒 |
| D、第Ⅳ步操作是将晶体溶于水后加热、蒸发、结晶 |
考点:纯碱工业(侯氏制碱法)
专题:元素及其化合物,化学应用
分析:A.依据侯德榜制碱的原理:向氨化的饱和食盐水中通入足量二氧化碳气体析出碳酸氢钠,加热分解碳酸氢钠来制备碳酸钠;
B.泡腾片主要成分为碳酸氢钠和酒石酸,通常是碳酸盐和固态酸的化合物;
C.第Ⅲ步通过过滤操作得到碳酸氢钠晶体;
D.第Ⅳ步操作是将晶体碳酸氢钠直接加热分解得到碳酸钠固体;
B.泡腾片主要成分为碳酸氢钠和酒石酸,通常是碳酸盐和固态酸的化合物;
C.第Ⅲ步通过过滤操作得到碳酸氢钠晶体;
D.第Ⅳ步操作是将晶体碳酸氢钠直接加热分解得到碳酸钠固体;
解答:
解:A.氨气易溶于水,二氧化碳能溶于水,依据侯德榜制碱的原理:向氨化的饱和食盐水中通入二氧化碳气体析出碳酸氢钠,加热反应制备纯碱,所以气体A为氨气,B为二氧化碳,故A正确;
B.第Ⅲ步操作是过滤操操作,通过过滤得到碳酸氢钠晶体,把纯碱及碳酸氢钠与某些固体酸性物质(如酒石酸)混合可制得泡腾片,故B正确;
C.第Ⅲ步操作是过滤操作,通过过滤得到碳酸氢钠晶体,所以需要的仪器有:烧杯、漏斗、玻璃棒,故C正确;
D.第Ⅳ步操作是将晶体碳酸氢钠直接加热分解得到碳酸钠固体,故D错误;
故选D.
B.第Ⅲ步操作是过滤操操作,通过过滤得到碳酸氢钠晶体,把纯碱及碳酸氢钠与某些固体酸性物质(如酒石酸)混合可制得泡腾片,故B正确;
C.第Ⅲ步操作是过滤操作,通过过滤得到碳酸氢钠晶体,所以需要的仪器有:烧杯、漏斗、玻璃棒,故C正确;
D.第Ⅳ步操作是将晶体碳酸氢钠直接加热分解得到碳酸钠固体,故D错误;
故选D.
点评:本题考查了侯德榜制碱的工作原理和流程分析,掌握工艺流程和反应原理是解题关键,题目难度中等.

练习册系列答案
相关题目
下列各组离子可能大量共存的是( )
| A、不能使酚酞试液变红的无色溶液中:Na+、CO32-、K+、ClO- |
| B、能与金属铝反应放出氢气的溶液中:K+、NO3-、Cl-、NH4+ |
| C、常温下水电离出的c(H+)?c(OH-)=10-20的溶液中:Na+、Cl-、S2-、SO32- |
| D、无色透明溶液:K+、HCO3-、NO3-、SO42-、Fe3+ |
三聚氯氰是叫种重要的精细化工产品,广泛用于制造农药、染料、炸药、医药等工业.目前工业上生产三聚氯氰的反应原理为:3NaCN+3Cl2
3NaCl+ 下列有关说法正确的是( )
下列有关说法正确的是( )
| 活性炭 |
| 400℃ |
 下列有关说法正确的是( )
下列有关说法正确的是( )| A、三聚氯氰中C1的化合价是+1 |
| B、该反应中NaCN被还原 |
| C、三聚氯氰分子中既含σ键又含π健 |
| D、36.9 g三聚氯氰中含有1.204×1023个原子 |
对有机物 的表述不正确的是( )
的表述不正确的是( )
 的表述不正确的是( )
的表述不正确的是( )| A、该物质能发生加成、取代、氧化反应 |
| B、该物质遇FeC13溶液显色,lmol该物质能与2mo1Br2发生取代反应 |
| C、该物质的分子式为C11H15O3 |
| D、1mol该物质最多消耗Na,NaOH,NaHC03的物质的量之比为2:2:1 |
 A.1mol Na2CO3和1mol NaOH B.lmol Na2CO3和2molNaOH
A.1mol Na2CO3和1mol NaOH B.lmol Na2CO3和2molNaOH
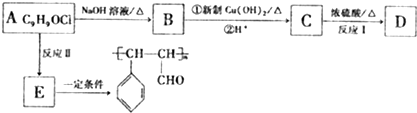
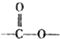 结构的芳香族化介物的同分异构体有
结构的芳香族化介物的同分异构体有