题目内容
25℃时,0.1mol/L的HA溶液中
=1010
①HA是 (填“强电解质”或“弱电解质”),将含0.1molHA的溶液用NaOH溶液滴定至中性,耗NaOH的物质的量 0.1mol(填>、<、=)
②在加水稀释HA溶液的过程中,随着水量的增加而增大的是 (填字母)
A.
B.
C.c(H+)与c(OH-)的乘积 D.c(OH-)
| c(H+) |
| c(OH-) |
①HA是
②在加水稀释HA溶液的过程中,随着水量的增加而增大的是
A.
| c(H+) |
| c(HA) |
| c(HA) |
| c(A) |
考点:弱电解质在水溶液中的电离平衡,强电解质和弱电解质的概念
专题:
分析:25℃时,0.1mol/L的HA溶液中
=1010,则c(H+)=1.0×10-2mol/L,c(OH-)=1.0×10-12mol/L,说明HA是弱酸,NaA溶液显碱性,加水稀释HA溶液,促进HA电离平衡正向移动,水的离子积常数只受温度影响,据此分析.
| c(H+) |
| c(OH-) |
解答:
解:①25℃时,0.1mol/L的HA溶液中
=1010,则c(H+)=1.0×10-2mol/L,c(OH-)=1.0×10-12mol/L,说明HA是弱酸,NaA溶液显碱性,将含0.1molHA的溶液用NaOH溶液滴定至中性,耗NaOH的物质的量小于0.1mol,故答案为:弱电解质;<;
②加水稀释HA溶液,促进HA电离平衡正向移动,n(H+)和n(A-)增大,n(HA)减小,水的离子积常数只受温度影响,
A、n(H+)和n(A-)增大,n(HA)减小,所以
增大,故A正确;
B、n(H+)和n(A-)增大,n(HA)减小,所以
减小,故B错误;
C、水的离子积常数只受温度影响,c(H+)与c(OH-)的乘积不变,故C错误;
D、弱酸HA加水稀释,溶液酸性减弱,氢离子浓度减小,氢氧根离子浓度增大,故D正确;
故答案为:AD.
| c(H+) |
| c(OH-) |
②加水稀释HA溶液,促进HA电离平衡正向移动,n(H+)和n(A-)增大,n(HA)减小,水的离子积常数只受温度影响,
A、n(H+)和n(A-)增大,n(HA)减小,所以
| c(H+) |
| c(HA) |
B、n(H+)和n(A-)增大,n(HA)减小,所以
| c(HA) |
| c(A-) |
C、水的离子积常数只受温度影响,c(H+)与c(OH-)的乘积不变,故C错误;
D、弱酸HA加水稀释,溶液酸性减弱,氢离子浓度减小,氢氧根离子浓度增大,故D正确;
故答案为:AD.
点评:本题考查了弱电解质判断、盐类水解、弱酸加水稀释时离子浓度的变化,注意水的离子积只受温度影响,难度不大.

练习册系列答案
相关题目
以下是在实验室模拟“侯氏制碱法”生产流程的示意图:则下列叙述错误的是( )


| A、A气体是NH3,B气体是CO2 |
| B、把纯碱及第Ⅲ步所得晶体与某些固体酸性物质(如酒石酸)混合可制泡腾片 |
| C、第Ⅲ步操作用到的主要玻璃仪器是烧杯、漏斗、玻璃棒 |
| D、第Ⅳ步操作是将晶体溶于水后加热、蒸发、结晶 |
下列叙述不正确的是( )
| A、植物油的不饱和程度高于动物油,植物油更易氧化变质 |
| B、除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤、分液 |
| C、过氧化钠中含有离子键和非极性共价键,阴离子与阳离子的物质的量之比为1:1 |
| D、向某溶液中滴入稀盐酸产生使澄清石灰水变浑浊的气体,该溶液不一定含有CO32- |
已知:Ksp(AgCl)=1.56×10-10,Ksp(AgI)=1.56×10-16,Ksp(Ag2CrO4)=2.0×10-12.下列有关说法正确的是( )
| A、相同温度下,饱和溶液中的Ag+浓度:AgCl>Ag2CrO4>AgI |
| B、向饱和食盐水中加AgNO3,形成AgCl沉淀时,溶液中的Ag+浓度为1.34×10-5 mol?L-1 |
| C、向含AgI难溶物的溶液中,逐滴加入饱和食盐水,原难溶物会变成白色 |
| D、向含Cl-、I-和CrO42-浓度均为0.010 mol?L-1的溶液中,逐滴加入AgNO3溶液,最先形成Ag2CrO4沉淀 |
室温下向10mL pH=3的醋酸溶液中加水稀释后,下对说法正确的是( )
| A、溶液中导电粒子的数目减少? | ||
| B、醋酸的电离程度增大,c(H+)亦增大 | ||
C、溶液中
| ||
| D、再加入10 mL pH=ll的NaOH溶液,混合液的PH=7 |
NA为阿伏加德罗常数,关于a g亚硫酸钠晶体(Na2SO3?7H2O)的说法中正确的是( )
A、含Na+数目为
| ||
B、含氧原子数目为
| ||
C、完全氧化SO32-时转移电子数目为
| ||
D、含结晶水分子数目为
|

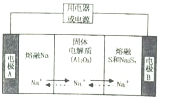 金属及其化合物在国民经济发展中起着重要作用
金属及其化合物在国民经济发展中起着重要作用