��Ŀ����
20��A��B��C���ֶ�����Ԫ�أ�A�ĵ�������������壬B�ǵؿ��к�������Ԫ�أ�C�ĵ���ͨ���������һ�ֻ���ɫ�����壬�����峣��������ˮ��ɱ���������밴Ҫ����գ���1�����Ԫ�ط���AHBO
��2��CԪ�������ڱ��е�λ�õ������ڵڢ�A��
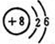
��3��B��ԭ�ӽṹʾ��ͼΪ��
��4��A��B�γɵĻ�����ĵ���ʽΪ
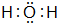 ��
��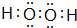 �����ڹ��ۻ����
�����ڹ��ۻ������5��д����C�ĵ�����ȡƯ��Һ�����ӷ�Ӧ����ʽ��Cl2+2OH-=Cl-+ClO-+H2O��
���� A��B��C���ֶ�����Ԫ�أ�A�ĵ�������������壬��AΪHԪ�أ�B�ǵؿ��к�������Ԫ�أ���BΪOԪ�أ�C�ĵ���ͨ���������һ�ֻ���ɫ�������ж�ΪCl2�������峣��������ˮ��ɱ����������CΪClԪ�أ�
��� �⣺A��B��C���ֶ�����Ԫ�أ�A�ĵ�������������壬��AΪHԪ�أ�B�ǵؿ��к�������Ԫ�أ���BΪOԪ�أ�C�ĵ���ͨ���������һ�ֻ���ɫ�������ж�ΪCl2�������峣��������ˮ��ɱ����������CΪClԪ�أ�
��1��AΪHԪ�أ�BΪOԪ�أ��ʴ�Ϊ��H��O��
��2��CΪClԪ�أ������ڱ��е�λ�ã��������ڵڢ�A�壬�ʴ�Ϊ���������ڵڢ�A�壻
��3��BΪOԪ�أ�ԭ�ӽṹʾ��ͼΪ�� ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��4��A��B�γɵĻ�����ΪH2O��H2O2������ʽΪ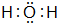 ��
��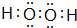 �����ڹ��ۻ����
�����ڹ��ۻ����
�ʴ�Ϊ��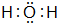 ��
��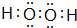 �����ۣ�
�����ۣ�
��5����C�ĵ�����ȡƯ��Һ�����ӷ�Ӧ����ʽ��Cl2+2OH-=Cl-+ClO-+H2O��
�ʴ�Ϊ��Cl2+2OH-=Cl-+ClO-+H2O��
���� ���⿼��ṹ����λ�ù�ϵӦ�ã����ػ�ѧ����Ŀ��飬ע��Ի���֪ʶ���������գ�

��ϰ��ϵ�д�
�����Ŀ
9�����й��ڻ�ѧ��Ӧ���ʵ�˵������ȷ���ǣ�������
| A�� | ��ѧ��Ӧ����ͨ���õ�λʱ���ڷ�Ӧ���������������仯����ʾ | |
| B�� | �ò�ͬ���ʵ�Ũ�ȱ仯��ʾͬһʱ���ڡ�ͬһ��Ӧ������ʱ������ֵ֮�ȵ��ڷ�Ӧ����ʽ�ж�Ӧ���ʵĻ�ѧ������֮�� | |
| C�� | ��Ӧ����Խ����λʱ����������IJ�����Խ�� | |
| D�� | �ڷ�Ӧ�����У���Ӧ��Ũ����С�������÷�Ӧ���ʾ�Ļ�ѧ��Ӧ����Ϊ��ֵ |
15������������ȷ���ǣ�������
| A�� | ԭ�Ӱ뾶��Al��Mg��Na��H | B�� | ���ȶ��ԣ�NH3��PH3��H2S��HCl | ||
| C�� | Ԫ�طǽ����ԣ�F��O��N��C | D�� | ���ԣ�HClO4��H2SiO3��H3PO4��H2CO3 |
5��ԭ�ӵĵ����Ų�Ϊ[Ar]3d54s2��Ԫ��λ�ڣ�������
| A�� | s�� | B�� | p�� | C�� | d�� | D�� | f�� |
12�������й�����ת������ʶ��ȷ���ǣ�������
| A�� | ͨ��ֲ��Ĺ�����ã�̫����ת��Ϊ���� | |
| B�� | ʹ�õ�¯����ʳ�������ת��Ϊ��ѧ�� | |
| C�� | �������ڻ�ѧ�仯�Ĺ���������ת���ϱ������ⷢ����һЩ����ת����Ϊ��������Ч | |
| D�� | ȼ��ȼ�գ�ֻ�ǽ���ѧ��ת��Ϊ���� |
10�������������ʵıȽ��У���ȷ���ǣ�������
| A�� | �⻯���ȶ��ԣ�HBr��HCl��PH3 | B�� | ���Ӱ뾶��Na+��Cl-��F- | ||
| C�� | ���ԣ�NaOH��Mg��OH��2��Al��OH��3 | D�� | ���ӵĻ�ԭ�� Cl��Br��I |
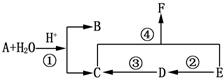
 ��
��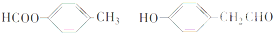 ��
��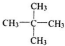 ��
��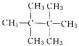 ��д�ṹ��ʽ��
��д�ṹ��ʽ��