题目内容
实验室模拟合成氨和氨催化氧化的流程如图为已知实验室可用饱和亚硝酸钠(NaNO2)溶液与饱和氯化铵溶液经加热后反应制取氮气.
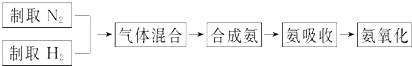
(1)从图1中选择制取气体的合适装置为氮气 、氢气
(2)氮气和氢气通过图2甲装置,图2甲装置的作用除了将气体混合外,还可以 、
(3)氨合成器出来经冷却的气体连续通入乙装置的水中吸收氨, (填会或不会)发生倒吸,
原因是
(4)图2乙装置吸收一段时间氨后,再通入空气,将经加热的铂丝插入乙装置的锥形瓶,能使铂丝保持红热,原因是该反应是一个放热反应,锥形瓶中还可观察到的现象是
(5)写出乙装置中氨氧化的化学方程式为 .
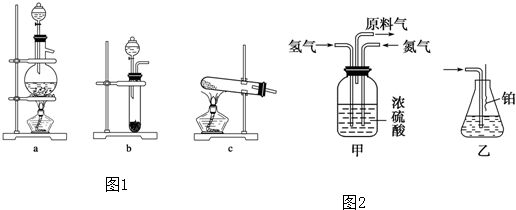

(1)从图1中选择制取气体的合适装置为氮气
(2)氮气和氢气通过图2甲装置,图2甲装置的作用除了将气体混合外,还可以
(3)氨合成器出来经冷却的气体连续通入乙装置的水中吸收氨,
原因是
(4)图2乙装置吸收一段时间氨后,再通入空气,将经加热的铂丝插入乙装置的锥形瓶,能使铂丝保持红热,原因是该反应是一个放热反应,锥形瓶中还可观察到的现象是
(5)写出乙装置中氨氧化的化学方程式为

考点:氨的制取和性质
专题:氮族元素
分析:(1)可根据制取气体的药品状态和条件选择合适的制取仪器;
(2)通过观察图2甲装置中冒气泡的速率来控制气体流量;
(3)合成氨的反应是可逆的,还会有一些氮气、氢气存在,据此来回答;
(4)一氧化氮遇空气就变为二氧化氮,二氧化氮是红棕色气体;
(5)氨的催化氧化生成一氧化氮和水,据此写出反应的化学方程式.
(2)通过观察图2甲装置中冒气泡的速率来控制气体流量;
(3)合成氨的反应是可逆的,还会有一些氮气、氢气存在,据此来回答;
(4)一氧化氮遇空气就变为二氧化氮,二氧化氮是红棕色气体;
(5)氨的催化氧化生成一氧化氮和水,据此写出反应的化学方程式.
解答:
解:(1)实验室可用饱和亚硝酸钠(NaNO2)溶液与饱和氯化铵溶液经加热后反应制取氮气,是溶液与溶液反应,且需要加热,可以选择a;
实验室里用金属锌粒和稀硫酸反应制取氢气,是固体和液体反应,不需要加热,可以选择装置b,
故答案为:a;b;
(2)氮气和氢气通过甲装置,图2甲装置中的浓硫酸可以将氮气和氢气干燥,同时可以根据甲装置中冒气泡的速率来控制气体流量,
故答案为:干燥气体;控制氢气和氮气的流速;
(3)合成氨的反应为为可逆反应,还会有一些氮气、氢气存在,这样会缓解氨气极易溶于水导致的气压差,不会倒吸,
故答案为:不会;因为混合气体中含有大量难溶于水的氮气、氢气两种气体;
(4)氨的催化氧化反应是一个放热反应,将经加热的铂丝插入乙装置的锥形瓶内,能使铂丝保持红热,同时氨催化氧化产物一氧化氮极易变为二氧化氮,二氧化氮是红棕色气体,
故答案为:有红棕色气体产生;
(5)根据反应物的性质进行分析,氨的催化氧化生成一氧化氮和水,氨的催化氧化反应为:4NH3+5O2
4NO+6H2O,
故答案为:4NH3+5O2
4NO+6H2O.
实验室里用金属锌粒和稀硫酸反应制取氢气,是固体和液体反应,不需要加热,可以选择装置b,
故答案为:a;b;
(2)氮气和氢气通过甲装置,图2甲装置中的浓硫酸可以将氮气和氢气干燥,同时可以根据甲装置中冒气泡的速率来控制气体流量,
故答案为:干燥气体;控制氢气和氮气的流速;
(3)合成氨的反应为为可逆反应,还会有一些氮气、氢气存在,这样会缓解氨气极易溶于水导致的气压差,不会倒吸,
故答案为:不会;因为混合气体中含有大量难溶于水的氮气、氢气两种气体;
(4)氨的催化氧化反应是一个放热反应,将经加热的铂丝插入乙装置的锥形瓶内,能使铂丝保持红热,同时氨催化氧化产物一氧化氮极易变为二氧化氮,二氧化氮是红棕色气体,
故答案为:有红棕色气体产生;
(5)根据反应物的性质进行分析,氨的催化氧化生成一氧化氮和水,氨的催化氧化反应为:4NH3+5O2
| ||
| △ |
故答案为:4NH3+5O2
| ||
| △ |
点评:本题考查了氨气的制法及化学性质,是一道关于氨气的制取和性质知识的综合题目,题目难度中等,试题综合性强,注意掌握氨气的实验室制法原理,明确氨气的化学性质,试题有利于培养学生的分析、理解能力及灵活应用所学知识的能力.

练习册系列答案
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案
相关题目
2014南京青奥会,体操运动员在比赛时为了防滑.常在手掌上涂抹碳酸镁粉末,碳酸镁属于 ( )
| A、酸 | B、碱 | C、盐 | D、氧化物 |
在一定温度下,可逆反应达到平衡时,生成物平衡浓度的系数次方的乘积与反应物平衡浓度的系数次方的乘积之比是一个常数,该常数就叫做化学平衡常数,用符号K表示.在一定温度下的密闭容器中存在如下反应:2SO2(g)+O2(g)
2SO3(g),已知c(SO2)始=0.4mol?L-1,c(O2)始=1mol?L-1经测定该反应在该温度下的平衡常数K=19,则此反应中SO2的转化量为( )
| 催化剂 |
| △ |
| A、0.24 mol?L-1 |
| B、0.28 mol?L-1 |
| C、0.32 mol?L-1 |
| D、0.26 mol?L-1 |
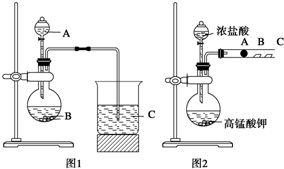 某研究性学习小组设计了一组实验来探究元素周期律.甲同学:根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成N、C、Si三种非金属元素的非金属性强弱比较的实验研究;
某研究性学习小组设计了一组实验来探究元素周期律.甲同学:根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成N、C、Si三种非金属元素的非金属性强弱比较的实验研究;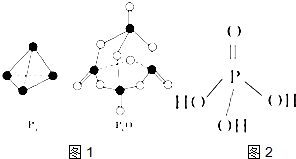 第五主族的磷单质及其化合物在工业上有广泛应用.
第五主族的磷单质及其化合物在工业上有广泛应用.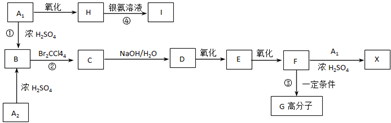
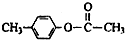 、
、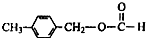 外,其余的结构简式:
外,其余的结构简式: