题目内容
在标准状况下,把1体积Cl2、5体积O2跟11体积H2混合,这三种气体的物质的量之比是 ,质量比是 ,混合气体的平均相对分子质量是 ;如果在密闭容器中将混合气体用电火花引燃后,恰好完全反应,所得盐酸(ρ=1.143g/cm3)的物质的量浓度是 .
考点:物质的量的相关计算
专题:
分析:相同条件下,气体体积之比等于其物质的量之比,根据m=nM计算质量之比,根据
=
计算平均摩尔质量,进而确定平均相对分子质量;恰好反应得到盐酸,计算溶液质量分数,再根据c=
计算所得盐酸物质的量浓度.
. |
| M |
| m总 |
| n总 |
| 1000ρω |
| M |
解答:
解:相同条件下,气体体积之比等于其物质的量之比,故1体积Cl2、5体积O2跟11体积H2混合,三种气体的物质的量之比是1:5:11,质量之比为1×71:5×32:11×2=71:160:22,平均相对分子质量为
=14.9,用电火花引燃后,恰好完全反应,得到HCl与水的物质的量之比为2:10,所得溶液中HCl质量分数为
×100%,故所得盐酸物质的量浓度为
mol/L=9.04mol/L,
故答案为:1:15:11;71:160:22;14.9;9.04mol/L.
| 71+160+22 |
| 1+5+11 |
| 2×36.5 |
| 2×36.5+10×18 |
1000×1.143×
| ||
| 36.5 |
故答案为:1:15:11;71:160:22;14.9;9.04mol/L.
点评:本题考查混合物计算、物质的量有关计算,难度不大,注意对基础知识的理解掌握,注意理解掌握物质的量浓度与质量分数的之间的关系.

练习册系列答案
相关题目
运用相关化学知识进行判断,下列结论正确的是( )
| A、晶体硅熔点高硬度大,因而可用于制作半导体材料 |
| B、SO2使溴水褪色与乙醛使溴水褪色的原理相同 |
| C、硅胶可作袋装食品的干燥剂,P2O5可用于干燥Cl2和NH3 |
| D、金属汞一旦洒落在实验室地面或桌面时,必须尽可能收集,并深埋处理 |
下列叙述正确的是( )
| A、氧气约占空气质量的21% |
| B、氢气中氢元素的化合价为+1价 |
| C、氧气能支持燃烧,可做燃料 |
| D、一氧化碳和木炭都具有还原性 |
若agCO2含b个分子,则阿伏加德罗常数的值为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列图式表示正确的是( )
A、二氧化碳 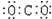 |
B、N原子的价电子电子排布图: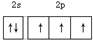 |
C、铝离子的结构示意图 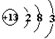 |
| D、乙醇的分子式:C2H5OH |