题目内容
20.已知温度T时水的离子积常数为Kw.该温度下,将浓度为a mol•L-1的一元酸HA与b mol•L-1的NaOH等体积混合,混合溶液中c(H+)=$\sqrt{{K}_{w}}$mol•L-1.下列说法不正确的是( )| A. | 混合溶液呈中性 | |
| B. | a≥b | |
| C. | 混合溶液中,c(A-)=c(Na+) | |
| D. | 混合液中水电离出c(OH-)大于该温度下纯水电离出c(OH-) |
分析 温度T时水的离子积常数为KW,浓度为a mol/L的一元酸HA与b mol/L的一元碱NaOH等体积混合,混合后溶液中c(H+)=$\sqrt{{K}_{w}}$mol/L,而c(H+)×c(OH-)=KW,则c(OH-)=c(H+),说明溶液呈中性.若酸为一元强酸,则酸与氢氧化钠浓度相等,若酸为一元弱酸,则酸稍过量.根据电荷守恒可知c(A-)=c(Na+).
解答 解:A.温度T时水的离子积常数为KW,浓度为a mol/L的一元酸HA与b mol/L的一元碱NaOH等体积混合,混合后溶液中c(H+)=$\sqrt{{K}_{w}}$mol/L,而c(H+)×c(OH-)=KW,则c(OH-)=c(H+),说明溶液呈中性,故A正确;
B.若酸为一元强酸,则酸与氢氧化钠浓度相等,若酸为一元弱酸,恰好反应生成为强碱弱酸盐,溶液呈碱性,故酸稍过量,则a≥b,故B正确;
C.根据电荷守恒:c(A-)+c(OH-)=c(H+)+c(Na+),溶液呈中性c(OH-)=c(H+),则c(A-)=c(Na+),故C正确;
D.混合液中水电离出c(OH-)等于该温度下纯水电离出c(OH-),故D错误.
故选:D.
点评 本题考查离子浓度大小比较、水的离子积、酸碱混合的定性判断等,题目难度中等,注意溶液呈中性应存在c(H+)=c(OH-).

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
11.在配制一定物质的量浓度的盐酸时,下列错误操作可使所配制溶液的浓度偏高的是( )
| A. | 用量筒量取浓盐酸时俯视量筒刻度进行读数 | |
| B. | 定容时俯视容量瓶瓶颈刻度线 | |
| C. | 溶解搅拌时有液体飞溅 | |
| D. | 摇匀后见液面下降,再加水至刻度线 |
8.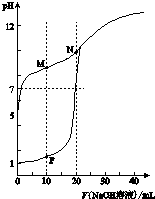 温室下,用0.1mol•L-1NaOH溶液分别滴定体积均为20ml浓度均为0.1mol•L-1HCl溶液和HX溶液,溶液的pH随加入NaOH溶液体积变化图,下列说法不正确的是( )
温室下,用0.1mol•L-1NaOH溶液分别滴定体积均为20ml浓度均为0.1mol•L-1HCl溶液和HX溶液,溶液的pH随加入NaOH溶液体积变化图,下列说法不正确的是( )
 温室下,用0.1mol•L-1NaOH溶液分别滴定体积均为20ml浓度均为0.1mol•L-1HCl溶液和HX溶液,溶液的pH随加入NaOH溶液体积变化图,下列说法不正确的是( )
温室下,用0.1mol•L-1NaOH溶液分别滴定体积均为20ml浓度均为0.1mol•L-1HCl溶液和HX溶液,溶液的pH随加入NaOH溶液体积变化图,下列说法不正确的是( )| A. | HX为弱酸 | |
| B. | M点c(HX)-c(X-)>c(OH-)-c(H+) | |
| C. | 将P点和N点的溶液为混合,呈酸性 | |
| D. | 向N点溶液中通入HCl至pH=7:c(Na+)>c(HX)=c(Cl-)>c(X-) |
15.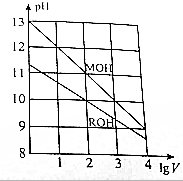 常温下,向浓度相同、体积均为1L的MOH和ROH溶液,分别加水稀释至体积V,pH随1gV的变化如图所示,下列叙述错误的是( )
常温下,向浓度相同、体积均为1L的MOH和ROH溶液,分别加水稀释至体积V,pH随1gV的变化如图所示,下列叙述错误的是( )
 常温下,向浓度相同、体积均为1L的MOH和ROH溶液,分别加水稀释至体积V,pH随1gV的变化如图所示,下列叙述错误的是( )
常温下,向浓度相同、体积均为1L的MOH和ROH溶液,分别加水稀释至体积V,pH随1gV的变化如图所示,下列叙述错误的是( )| A. | MOH是强碱,ROH是弱碱 | |
| B. | 原ROH溶液的浓度为1.0mol/L | |
| C. | 常温下,ROH的电离平衡常数Kb约为1.1×10-5 | |
| D. | 当1gV=2时,若两溶液同时升高温度,则$\frac{c({M}^{+})}{c({R}^{+})}<10$ |
12.下列能量转化过程中没有化学能变化的是( )
| A. | 氯化铵热分解反应 | B. | 氮气和氢气化合生成氨的反应 | ||
| C. | 碘升华 | D. | 绿色植物的光合作用生成淀粉 |
10.下列关于氧化物及过氧化物的说法中正确的是( )
| A. | 因为H2O2和Na2O2都是过氧化物,所以二者化学键的类型完全相同 | |
| B. | 标准状况下,2.24 L NO2和N2O4组成的混合气体中,原子总数是分子总数的3倍 | |
| C. | NO、NO2、SO2、SO3都是酸性氧化物 | |
| D. | 常温常压下,5.6 L SO2与足量的O2混合,充分反应后,生成的SO3物质的量小于0.25 mol |
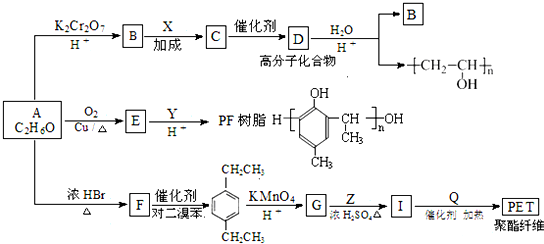
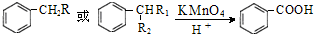 (R为H原子或烃基)
(R为H原子或烃基)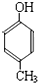
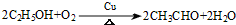
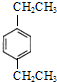 的同分异构体W也能被酸性高锰酸钾溶液氧化为G,W的所有可能结构简式为
的同分异构体W也能被酸性高锰酸钾溶液氧化为G,W的所有可能结构简式为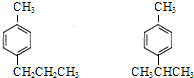

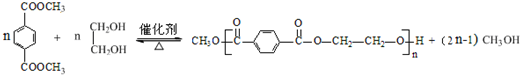 .
.