题目内容
20.工业上通过电解饱和的食盐水来制取氯气.现取500ml含NaCl为11.7g的饱和食盐水进行电解,2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑
在标准状况下制得Cl2多少升?所得NaOH的物质的量浓度为多少?(电解前后溶液体积保持不变)
分析 计算NaCl的物质的量,根据化学方程式计算生成氯气、氢氧化钠物质的量,再根据V=nVm计算氯气体积,根据c=$\frac{n}{V}$计算NaOH的物质的量浓度.
解答 解:11.7g NaCl的物质的量为$\frac{11.7g}{58.5g/mol}$=0.2mol
2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑
2 2 1
0.2mol n(NaOH) n(Cl2)
所以n(Cl2)=$\frac{0.2mol×1}{2}$=0.1mol
n(NaOH)=$\frac{0.2mol×2}{2}$=0.2mol
则标况下生成氯气体积为0.1mol×22.4L/mol=2.24L,
所得NaOH的物质的量浓度为$\frac{0.2mol}{0.5L}$=0.4mol/L,
答:在标准状况下制得Cl2为2.24L,所得NaOH的物质的量浓度为0.4mol/L.
点评 本题以氯碱工业为载体,考查化学方程式有关计算,比较基础,旨在考查学生对基础知识的理解掌握与应用.

练习册系列答案
相关题目
9.下列关于SO2的叙述中,正确的是( )
| A. | 可以用碱石灰来干燥SO2气体 | |
| B. | 通入BaCl2溶液中,能生成白色沉淀 | |
| C. | 因为SO2有漂白性,所以它能使品红溶液、溴水褪色 | |
| D. | 将SO2气体通入装有品红溶液的试管里,红色逐渐褪去,给试管加热恢复红色 |
10.下列反应的离子方程式的书写不正确的是( )
| A. | 向漂粉精溶液中通入过量的二氧化碳:ClO-+H2O+CO2═HClO+HCO3- | |
| B. | 氯气与水反应:Cl2+H2O═2H++Cl-+ClO- | |
| C. | 二氧化锰与浓盐酸反应:MnO2+4H++4Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2H2O+2Cl2↑, | |
| D. | 碳酸钙粉末与新制氯水反应:CaCO3+2H+═Ca2++H2O+CO2↑ |
15.一定温度下,反应C(s)+H2O(g)?CO(g)+H2(g)在密闭容器中进行,一段时间后达到平衡,下列措施不能使平衡发生移动的是( )
①增加C的物质的量 ②保持容器容积不变,充入N2使体系压强增大 ③将容器的容积缩小一半 ④保持压强不变,充入N2使容器容积变大.
①增加C的物质的量 ②保持容器容积不变,充入N2使体系压强增大 ③将容器的容积缩小一半 ④保持压强不变,充入N2使容器容积变大.
| A. | ①② | B. | ②③ | C. | ①④ | D. | ③④ |
5. 进入冬季北方开始供暖后,雾霾天气愈发严重,各地PM2.5、PM10经常“爆表”.引发雾霾天气的污染物中,最为常见的是机动车尾气中的氮氧化物和燃煤产生的烟气.
进入冬季北方开始供暖后,雾霾天气愈发严重,各地PM2.5、PM10经常“爆表”.引发雾霾天气的污染物中,最为常见的是机动车尾气中的氮氧化物和燃煤产生的烟气.
Ⅰ、已知反应N2O4(g)?2NO2(g)△H,随温度升高,混合气体的颜色变深.将一定量N2O4气体充入绝热容器一段时间后,研究压缩和拉伸活塞过程中混合气体的气体的透光率(气体颜色越浅,透光率越大)随时间变化情况.下列说法能说明透光率不再发生改变的有ad.
a.气体颜色不再改变 b.△H不再改变
c.v正(N2O4)=2v逆(NO2) d.N2O4的转化率不再改变
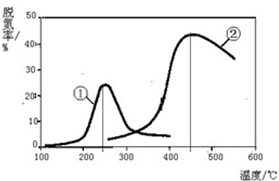
Ⅱ、用NH3催化还原NOx可以消除氮氧化物的污染.右下图,采用NH3作还原剂,烟气以一定的流速通过两种不同催化剂,测量逸出气体中氮氧化物含量,从而确定烟气脱氮率(注:脱氮率即氮氧化物转化率),反应原理为:
NO(g)+NO2(g)+2NH3(g)?2N2(g)+3H2O(g).
(1)该反应的△S>0(填“>”、“=”或“<”).
(2)以下说法正确的是C.
A.第②种催化剂比第①种催化剂脱氮率高
B.相同条件下,改变压强对脱氮率没有影响
C.催化剂①、②分别适合于250℃和450℃左右脱氮
Ⅲ、用CH4催化还原NOx也可以消除氮氧化物的污染.
(3)已知:CH4(g)的标准燃烧热为-890kJ/mol,蒸发1mol H2O(l)需要吸收44kJ热量.
CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H=-1114kJ/mol
2NO(g)+O2(g)═2NO2(g)△H=-114kJ/mol
写出CH4催化还原NO2(g)生成N2和H2O(g)的热化学方程式:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=-844kJ/mol.
(4)在温度为T1℃和T2℃时,分别将0.5mol CH4和1.2mol NO2充入体积为1L的密闭容器中,测得NO2的物质的量随时间变化数据如下表:
①温度为T1℃时,0~20min内,v(CH4)=0.0125mol/(L.s).
②T1<T2(填“>”或“<”,下空同);判断理由是升高温度,NO2的物质的量增大,平衡逆向移动,正反应为放热反应.
③T1℃时,反应CH4(g)+2NO2(g)?N2(g)+CO2(g)+2H2O(g)平衡常数K=6.4.
④温度为T2℃时,达平衡后,再向容器中加入0.5mol CH4和1.2mol NO2,达新平衡时CH4的转化率将减小(填“增大”、“减小”或“不变”).
 进入冬季北方开始供暖后,雾霾天气愈发严重,各地PM2.5、PM10经常“爆表”.引发雾霾天气的污染物中,最为常见的是机动车尾气中的氮氧化物和燃煤产生的烟气.
进入冬季北方开始供暖后,雾霾天气愈发严重,各地PM2.5、PM10经常“爆表”.引发雾霾天气的污染物中,最为常见的是机动车尾气中的氮氧化物和燃煤产生的烟气.Ⅰ、已知反应N2O4(g)?2NO2(g)△H,随温度升高,混合气体的颜色变深.将一定量N2O4气体充入绝热容器一段时间后,研究压缩和拉伸活塞过程中混合气体的气体的透光率(气体颜色越浅,透光率越大)随时间变化情况.下列说法能说明透光率不再发生改变的有ad.
a.气体颜色不再改变 b.△H不再改变
c.v正(N2O4)=2v逆(NO2) d.N2O4的转化率不再改变
Ⅱ、用NH3催化还原NOx可以消除氮氧化物的污染.右下图,采用NH3作还原剂,烟气以一定的流速通过两种不同催化剂,测量逸出气体中氮氧化物含量,从而确定烟气脱氮率(注:脱氮率即氮氧化物转化率),反应原理为:
NO(g)+NO2(g)+2NH3(g)?2N2(g)+3H2O(g).
(1)该反应的△S>0(填“>”、“=”或“<”).
(2)以下说法正确的是C.
A.第②种催化剂比第①种催化剂脱氮率高
B.相同条件下,改变压强对脱氮率没有影响
C.催化剂①、②分别适合于250℃和450℃左右脱氮
Ⅲ、用CH4催化还原NOx也可以消除氮氧化物的污染.
(3)已知:CH4(g)的标准燃烧热为-890kJ/mol,蒸发1mol H2O(l)需要吸收44kJ热量.
CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H=-1114kJ/mol
2NO(g)+O2(g)═2NO2(g)△H=-114kJ/mol
写出CH4催化还原NO2(g)生成N2和H2O(g)的热化学方程式:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=-844kJ/mol.
(4)在温度为T1℃和T2℃时,分别将0.5mol CH4和1.2mol NO2充入体积为1L的密闭容器中,测得NO2的物质的量随时间变化数据如下表:
时间/min 温度/℃ | 0 | 10 | 20 | 40 | 50 |
| T1 | 1.2 | 0.9 | 0.7 | 0.4 | 0.4 |
| T2 | 1.2 | 0.8 | 0.56 | … | 0.5 |
②T1<T2(填“>”或“<”,下空同);判断理由是升高温度,NO2的物质的量增大,平衡逆向移动,正反应为放热反应.
③T1℃时,反应CH4(g)+2NO2(g)?N2(g)+CO2(g)+2H2O(g)平衡常数K=6.4.
④温度为T2℃时,达平衡后,再向容器中加入0.5mol CH4和1.2mol NO2,达新平衡时CH4的转化率将减小(填“增大”、“减小”或“不变”).
12.如图为某化学兴趣小组设计的一个原电池,装置中电流表的指针发生偏转,则X应为( )
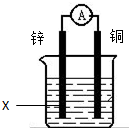

| A. | 水 | B. | 酒精 | C. | 稀硫酸 | D. | 植物油 |
9.在一定温度下的定容密闭容器中,当下列物理量不再发生变化时,表明反应A(s)+2B(g)?C(g)+D(g)已达到平衡状态的是( )
①混合气体的压强 ②混合气体的密度 ③B的物质的量浓度 ④混合气体的平均相对分子质量
⑤气体的总物质的量.
①混合气体的压强 ②混合气体的密度 ③B的物质的量浓度 ④混合气体的平均相对分子质量
⑤气体的总物质的量.
| A. | ②③④ | B. | ①②③ | C. | ③④⑤ | D. | ①④⑤ |
10.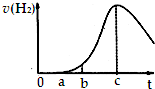 把在空气中久置的铝片5.0g投入盛有 500mL 0.5mol•L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间可用如图的坐标曲线来表示,则( )
把在空气中久置的铝片5.0g投入盛有 500mL 0.5mol•L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间可用如图的坐标曲线来表示,则( )
 把在空气中久置的铝片5.0g投入盛有 500mL 0.5mol•L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间可用如图的坐标曲线来表示,则( )
把在空气中久置的铝片5.0g投入盛有 500mL 0.5mol•L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间可用如图的坐标曲线来表示,则( )| A. | 曲线由0→a段发生了氧化还原反应 | |
| B. | 曲线由b→c段,产生氢气的速率增加较快的主要原因是反应放热 | |
| C. | c点达到了平衡 | |
| D. | c点以后,反应逐渐消耗了产生的氢气 |