题目内容
12.下列说法不正确的是( )| A. | 126C和146C是两种核素 | |
| B. | 纤维素和淀粉互为同分异构体 | |
| C. | CH3COOCH2CH3和CH3CH2OOCCH3是同物质 | |
| D. | CH3CH2COOH可看成是由-C2H5和-COOH两种基团组成 |
分析 A、核素的种类由质子数和中子数决定;
B、同分异构体是指分子式相同,但结构不同的化合物;
C、CH3COOCH2CH3和CH3CH2OOCCH3都是指乙酸乙酯;
D、羧酸可以看成羧基和烃基组成.
解答 解:A、126C和146C的质子数都为6,中子数分别为6,8,是两种不同的核素,故A正确;
B、淀粉和纤维素的分子式为(C6H10O5)n,聚合度n不同,分子式不同,不是同分异构体,故B错误;
C、CH3COOCH2CH3和CH3CH2OOCCH3都是指乙酸乙酯,属于同种物质,故C正确;
D、丙酸(CH3CH2COOH)可看成是由-C2H5和-COOH两种基团组成,故D正确;
故选B.
点评 本题主要考查了核素、同分异构体的判断、有机物的结构,难度不大,注意对同分异构体定义的理解.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
3.用含有Al2O3、SiO2和少量FeO•xFe2O3的铝灰制备Al2(SO4)3•18H2O,工艺流程如下(部分操作和条件略):
Ⅰ.向铝灰中加入过量稀H2SO4,过滤;
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色;
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ.再经过一系列操作,分离得到产品.
(1)步骤Ⅰ中过滤所得滤渣主要成分为:SiO2,H2SO4溶解Al2O3的离子方程式为:Al2O3+6H+=2Al3++3H2O.
(2)步骤Ⅱ中加入KMnO4时发生反应的离子方程式为:MnO4-+5Fe2++8H+=5Fe3++Mn2++4H2O.
(3)已知:生成氢氧化物沉淀的pH
注:金属离子的起始浓度均为0.1mol•L-1
根据表中数据解释步骤Ⅱ的目的:pH约为3时,Fe2+和Al3+不能形成沉淀,将Fe2+氧化为Fe3+,可使铁完全沉淀.
(4)已知:一定条件下,MnO4-可与Mn2+反应生成MnO2.
①向Ⅲ的沉淀中加入浓盐酸并加热,能说明沉淀中存在MnO2的现象是:生成黄绿色气体.
②步骤Ⅳ中加入MnSO4的目的是:除去过量的MnO4-.
(5)步骤Ⅴ中“一系列操作”是蒸发浓缩、冷却结晶.
Ⅰ.向铝灰中加入过量稀H2SO4,过滤;
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色;
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ.再经过一系列操作,分离得到产品.
(1)步骤Ⅰ中过滤所得滤渣主要成分为:SiO2,H2SO4溶解Al2O3的离子方程式为:Al2O3+6H+=2Al3++3H2O.
(2)步骤Ⅱ中加入KMnO4时发生反应的离子方程式为:MnO4-+5Fe2++8H+=5Fe3++Mn2++4H2O.
(3)已知:生成氢氧化物沉淀的pH
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
根据表中数据解释步骤Ⅱ的目的:pH约为3时,Fe2+和Al3+不能形成沉淀,将Fe2+氧化为Fe3+,可使铁完全沉淀.
(4)已知:一定条件下,MnO4-可与Mn2+反应生成MnO2.
①向Ⅲ的沉淀中加入浓盐酸并加热,能说明沉淀中存在MnO2的现象是:生成黄绿色气体.
②步骤Ⅳ中加入MnSO4的目的是:除去过量的MnO4-.
(5)步骤Ⅴ中“一系列操作”是蒸发浓缩、冷却结晶.
20.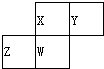 如图为元素周期表中短周期的一部分,四种元素均为非稀有气体元素.下列关于这四种元素及其化合物的说法中正确的是( )
如图为元素周期表中短周期的一部分,四种元素均为非稀有气体元素.下列关于这四种元素及其化合物的说法中正确的是( )
 如图为元素周期表中短周期的一部分,四种元素均为非稀有气体元素.下列关于这四种元素及其化合物的说法中正确的是( )
如图为元素周期表中短周期的一部分,四种元素均为非稀有气体元素.下列关于这四种元素及其化合物的说法中正确的是( )| A. | 原子半径:Z>W>X>Y | |
| B. | 气态氢化物的稳定性:Z>W>X>Y | |
| C. | W的最高正化合价与负化合价的绝对值不可能相等 | |
| D. | Z的最高价氧化物的水化物可能为强碱 |
7.下列有关有机物分离提纯的方法正确的是( )
| A. | 溴苯中混有溴,加入KI溶液,振荡,用汽油萃取出I2 | |
| B. | 乙烷中混有乙烯,通过氢气在一定条件下反应,使乙烯转化为乙烷 | |
| C. | 乙烯中混有CO2和SO2,将其通过盛有NaOH溶液的洗气瓶,再干燥 | |
| D. | 除去乙醇中的微量水可加入金属钠,使其完全反应 |
4.只用下列试剂中的一种就能鉴别AgNO3、Na2CO3、K2SO4三种溶液,则该试剂是( )
| A. | KNO3溶液 | B. | Na2SO4溶液 | C. | NaOH溶液 | D. | 稀HCl |
1.下列解释事实的方程式正确的是( )
| A. | 将NO2通入水中,红棕色消失:3NO2+H2O═2HNO3+O2 | |
| B. | 向含有Hg2+的废水中加入Na2S 产生沉淀:Hg2++S2-═Hg+S↓ | |
| C. | Na 与水反应产生气体:2Na+H2O═2Na++2OH-+H2↑ | |
| D. | 向燃煤中加入石灰石可减少 SO2的排放:2CaCO3+O2+2SO2$\frac{\underline{\;\;△\;\;}}{\;}$2CaSO4+2CO2 |
2. 在甲、乙两个装置中,胶头滴管中吸入某种液体,烧瓶中充入(或放入)另一种物质,挤压胶头滴管,加入液体,一段时间后两装置中的气球都有明显胀大.则所用试剂分别可能依次是( )
在甲、乙两个装置中,胶头滴管中吸入某种液体,烧瓶中充入(或放入)另一种物质,挤压胶头滴管,加入液体,一段时间后两装置中的气球都有明显胀大.则所用试剂分别可能依次是( )
 在甲、乙两个装置中,胶头滴管中吸入某种液体,烧瓶中充入(或放入)另一种物质,挤压胶头滴管,加入液体,一段时间后两装置中的气球都有明显胀大.则所用试剂分别可能依次是( )
在甲、乙两个装置中,胶头滴管中吸入某种液体,烧瓶中充入(或放入)另一种物质,挤压胶头滴管,加入液体,一段时间后两装置中的气球都有明显胀大.则所用试剂分别可能依次是( )| A. | 甲:浓硫酸和木炭 乙:浓氨水和SO2 | |
| B. | 甲:双氧水和MnO2 乙:饱和食盐水和HCl | |
| C. | 甲:苯酚和Na2CO3溶液 乙:NaOH溶液和Cl2 | |
| D. | 甲:浓硫酸和蔗糖(滴有几滴水) 乙:氯化亚铁溶液和硫化氢 |