题目内容
9.某饱和一元醇A中含氧的质量分数为34.8%,该醇的结构简式可能为( )| A. | CH3OH | B. | C2H5OH | C. | HO-CH2CH2-OH | D. | CH3CH2CH2OH |
分析 一元醇A分子中含有1个O原子,根据A分子中质量分数约为34.8%可计算出A的相对分子量,结合饱和一元醇的通式确定其分子式,并以此确定结构简式.
解答 解:一元醇A的分子式为CnH2n+2O,氧的质量分数约为34.8%,该醇的相对分子量为$\frac{16}{34.8%}$=46,
A分子中C、H总原子量为:46-16=30,
则14n+2=30,
n=2,
为C2H5OH,
故选B.
点评 本题考查了有机物分子式、结构式的确定,为高频考点,侧重于学生的分析、计算能力的考查,题目难度中等,明确常见有机物结构与性质为解答关键,注意通式在确定有机物分子式中的应用方法.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
19.钢铁厂在冷轧过程中会产生高浓度酸性含铁废水,主要含有H+、Cl-、Fe2+、Fe3+等,其处理的主要工艺流程如下:
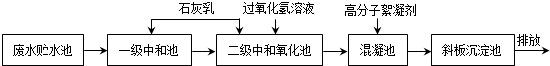
请回答:
(1)废水未经处理直接排放的危害是ab(填字母).
a.腐蚀水利设施 b.影响水生生物的自然生长
(2)石灰乳用于中和含铁废水中的酸,写出石灰乳与盐酸反应的化学方程式:Ca(OH)2+2HCl═CaCl2+2H2O.
(3)过氧化氢的主要作用是b(填字母).
a.还原剂 b.氧化剂
(4)某研究小组对钢铁厂高浓度酸性含铁废水进行监测时,取其样本稀释,测得有关数据如下:
稀释后的溶液中c(Fe3+)=0.12 mol/L.

请回答:
(1)废水未经处理直接排放的危害是ab(填字母).
a.腐蚀水利设施 b.影响水生生物的自然生长
(2)石灰乳用于中和含铁废水中的酸,写出石灰乳与盐酸反应的化学方程式:Ca(OH)2+2HCl═CaCl2+2H2O.
(3)过氧化氢的主要作用是b(填字母).
a.还原剂 b.氧化剂
(4)某研究小组对钢铁厂高浓度酸性含铁废水进行监测时,取其样本稀释,测得有关数据如下:
| 离子 | H+ | Cl- | Fe2+ | Fe3+ |
| 浓度(mol/L) | 0.16 | 0.94 | 0.12 |
17.下列各组中的反应,属于同一反应类型的是( )
| A. | 由溴丙烷水解制丙醇;由丙烯与水反应制丙醇 | |
| B. | 由甲苯硝化制对硝基甲苯;由甲苯氧化制苯甲酸 | |
| C. | 由氯代环己烷消去制环己烯;由丙烯加溴制1,2二溴丙烷 | |
| D. | 由乙酸和乙醇制乙酸乙酯;甲苯硝化制TNT |
14.下列关于热化学反应方程式的描述中正确的是( )
| A. | 稀H2SO4和稀Ba(OH)2溶液反应的热化学方程式为:$\frac{1}{2}$H2SO4(aq)+$\frac{1}{2}$Ba(OH)2(aq)=$\frac{1}{2}$BaSO4(s)+H2O(l)△H=-57.3kJ/mol | |
| B. | 1molCO(g)完全燃烧时放热283.0kJ,则2CO2(g)=2CO(g)+O2(g)反应的△H=+566kJ/mol | |
| C. | 需要加热才能发生的反应一定是吸热反应 | |
| D. | NaOH溶液与稀H2SO4反应中和热的化学方程式为2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l)△H=-114.6kJ/mol |
4.下列对于有机高分子化合物的认识正确的是( )
| A. | 合成有机高分子化合物称聚合物或高聚物,是因为它们大部分是由小分子通过加聚反应制得的 | |
| B. | 有机高分子化合物的相对分子质量很大,因而其结构复杂 | |
| C. | 对于一块高分子材料,n是一个整数值,因而它的相对分子质量是确定的 | |
| D. | 高分子材料可分为天然高分子材料和合成高分子材料两大类 |