题目内容
下列有关铁元素的叙述中正确的是( )
| A、铁是较活泼的金属,它与卤素(X2)反应的生成物均为FeX3 |
| B、氢氧化铁可以由相应的物质通过化合反应而制得 |
| C、氢氧化铁与氢碘酸反应:Fe(OH)3+3HI═FeI3+3H2O |
| D、铁元素位于周期表中第4周期第VIIIB族 |
考点:铁的化学性质,铁的氧化物和氢氧化物
专题:元素及其化合物
分析:A.铁与碘反应生成FeI2;
B.氢氧化亚铁和氧气、水反应可生成氢氧化铁;
C.铁离子具有强氧化性,可氧化碘离子;
D.铁元素位于周期表中第4周期第Ⅷ族.
B.氢氧化亚铁和氧气、水反应可生成氢氧化铁;
C.铁离子具有强氧化性,可氧化碘离子;
D.铁元素位于周期表中第4周期第Ⅷ族.
解答:
解:A.碘的氧化性较弱,铁与碘反应生成FeI2,故A错误;
B.如发生4Fe(OH)2+O2+2H2O=4Fe(OH)3,故B正确;
C.因发生2Fe(OH)3+6H++2I-=2Fe2++I2+6H2O,不可能生成FeI3,故C错误;
D.铁元素位于周期表中第4周期第Ⅷ族,故D错误.
故选B.
B.如发生4Fe(OH)2+O2+2H2O=4Fe(OH)3,故B正确;
C.因发生2Fe(OH)3+6H++2I-=2Fe2++I2+6H2O,不可能生成FeI3,故C错误;
D.铁元素位于周期表中第4周期第Ⅷ族,故D错误.
故选B.
点评:本题考查较为综合,多角度考查铁的单质、化合物的性质,为高频考点,侧重于学生的分析能力和基础知识的综合理解和运用的考查,注意相关基础知识的积累,难度不大.

练习册系列答案
相关题目
下列能够通过催化加氢后得到2、3-二甲基丁烷的是( )
| A、2、3-二甲基-1-丁烯 |
| B、2、3-二甲基-1-丁炔 |
| C、2、3-二甲基-1、3丁二烯 |
| D、2、3-二甲基-2-丁炔 |
某溶液中由水电离产生的C(H+)=1×10-10mol/L,该溶液的溶质不可能是( )
| A、KOH |
| B、Na2CO3 |
| C、HClO4 |
| D、Na HSO4 |
对于平衡:2A+2B?C+2D+3E+H2O(A、B、C、D、E为溶液中可自由移动的微粒),下列判断正确的是( )
| A、加水平衡左移 |
| B、增加A,可提高B的转化率 |
| C、平衡后,按起始投料比,再次投入A和B,则A和B的转化率都将增大 |
| D、升温该平衡一定发生移动 |
高铁酸钠(Na2FeO4)是一种新型的净水剂,对河湖水消毒,是城市饮水处理的新技术,制取Na2FeO4的反应为:Fe2O3+3Na2O2═2Na2FeO4+Na2O,下列说法不正确的是( )
| A、Fe2O3是反应的还原剂 |
| B、此反应中3mol Na2O2转移电子数3mol |
| C、Na2FeO4反应的氧化产物 |
| D、Na2FeO4能消毒杀菌是因其具有强氧化性 |
下列反应的离子方程式正确的是( )
| A、碳酸氢铵溶液与足量氢氧化钠溶液反应并加热NH4++OH-═NH3↑+H2O |
| B、氯化亚铁溶液中加入稀硝酸:3Fe2++4H++NO3-═3Fe3++2H2O+NO↑ |
| C、Fe2O3固体溶于过量氢碘酸溶液中:Fe2O3+6H+═2Fe3++3H2O |
| D、苯酚钠溶液中通入少量的CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32- |
下列有关说法正确的是( )
| A、陶瓷的主要成分是碳酸钙 |
| B、硅是制造半导体的常用材料 |
| C、电解氯化钠溶液制取金属钠 |
| D、用铁槽存放浓盐酸 |
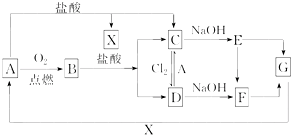 已知A是一种常见金属,F是一种红褐色沉淀.试根据图中转化关系,回答下列问题.
已知A是一种常见金属,F是一种红褐色沉淀.试根据图中转化关系,回答下列问题.