题目内容
某混合物由NaCl、MgCl2两种物质组成,其中Na和Mg两种元素的质量比为23:12.求:
(1)NaCl与MgCl2的物质的量之比 .
(2)氯离子总量为8mol时,Mg2+的物质的量是 .
(1)NaCl与MgCl2的物质的量之比
(2)氯离子总量为8mol时,Mg2+的物质的量是
考点:物质的量的相关计算
专题:计算题
分析:(1)Na和Mg两种元素的质量比为23:12,设质量分别为23g、12g,n(Na)=
=1mol,n(Mg)=
=0.5mol,NaCl与MgCl2的物质的量之比等于n(Na):n(Mg);
(2)Na、Mg的物质的量之比为2:1,设NaCl、MgCl2的物质的量分别为2x、x,利用氯离子守恒计算.
| 23g |
| 23g/mol |
| 12g |
| 24g/mol |
(2)Na、Mg的物质的量之比为2:1,设NaCl、MgCl2的物质的量分别为2x、x,利用氯离子守恒计算.
解答:
解:(1)Na和Mg两种元素的质量比为23:12,
设质量分别为23g、12g,
n(Na)=
=1mol,n(Mg)=
=0.5mol,
NaCl与MgCl2的物质的量之比等于n(Na):n(Mg)=1mol:0.5mol=2:1,
故答案为:2:1;
(2)Na、Mg的物质的量之比为2:1,
设NaCl、MgCl2的物质的量分别为2x、x,
由氯离子守恒可知,2x+x×2=8,
解得x=2mol,
故答案为:2mol.
设质量分别为23g、12g,
n(Na)=
| 23g |
| 23g/mol |
| 12g |
| 24g/mol |
NaCl与MgCl2的物质的量之比等于n(Na):n(Mg)=1mol:0.5mol=2:1,
故答案为:2:1;
(2)Na、Mg的物质的量之比为2:1,
设NaCl、MgCl2的物质的量分别为2x、x,
由氯离子守恒可知,2x+x×2=8,
解得x=2mol,
故答案为:2mol.
点评:本题考查物质的量的有关计算,把握质量、物质的量的关系及物质的构成为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
相关题目
NA代表阿伏伽德罗常数,下列说法正确的是( )
| A、9gD2O中含有的质子数为5NA |
| B、1molCaCl2中含有的离子数为3NA |
| C、30g甲醛中含共用电子对总数为4NA |
| D、71gCl2与足量NaOH溶液反应转移的电子数为2NA |
下列关于物质的量、摩尔质量的叙述中正确的是( )
| A、0.012kg12C中含有约6.02×1023个碳原子 |
| B、1molH2O中含有2 mol氢和1mol氧 |
| C、氢氧化钠的摩尔质量是40g |
| D、2mol水的摩尔质量是1mol水的摩尔质量的2倍 |
下列对化学知识概括合理的一组是( )
①能与酸反应的氧化物,一定是碱性氧化物
②一种元素可能有多种氧化物,但同种化合价只对应一种氧化物
③根据是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应
④根据分散系是否有丁达尔现象将分散系分为溶液、胶体和浊液
⑤在熔化状态和水溶液中均不能导电的物质称为非电解质
⑥氧化剂在反应中被氧化,还原剂在反应中被还原.
①能与酸反应的氧化物,一定是碱性氧化物
②一种元素可能有多种氧化物,但同种化合价只对应一种氧化物
③根据是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应
④根据分散系是否有丁达尔现象将分散系分为溶液、胶体和浊液
⑤在熔化状态和水溶液中均不能导电的物质称为非电解质
⑥氧化剂在反应中被氧化,还原剂在反应中被还原.
| A、只有①②③ | B、只有②③⑤ |
| C、只有③ | D、只有②④⑥ |
在配制一定物质的量浓度的溶液的实验中,下列操作正确的是( )
| A、将氢氧化钠固体放在天平托盘的滤纸上,精确称量并放入烧杯中溶解后,立即注入容量瓶中 |
| B、将准确量取的18.4mol?L-1的硫酸10mL,注入已盛有30mL水的100mL的容量瓶中,加水至刻度线 |
| C、仰视容量瓶刻度线,看到液面超过了容量瓶的刻度线,用胶头滴管吸出刻度线以上的溶液 |
| D、欲配制1000mL 0.1mol?L-1的盐酸,将稀释后的盐酸溶液全部转移到未经干燥的1000mL的容量瓶中,加水至刻度线 |
 如图是某反应体系中的三种气态物质M、N、P的物质的量浓度随时间的变化情况,则下列判断不正确的是( )
如图是某反应体系中的三种气态物质M、N、P的物质的量浓度随时间的变化情况,则下列判断不正确的是( )| A、该反应的化学方程式可表达为2M+N?2P |
| B、在反应时间为20min-25min之内,物质M的反应速率为0.002mol/(L?min) |
| C、当反应时间为20min时,曲线开始发生变化的原理可能是由于增大压强引起的 |
| D、反应在10min达到化学平衡状态,若曲线的变化是由于升温造成的(其它条件不变),则该反应的正反应一定为吸热反应 |
下列有关四种基本反应类型与氧化还原反应关系的说法中正确的是( )
| A、化合反应一定是氧化还原反应 |
| B、分解反应一定不是氧化还原反应 |
| C、置换反应一定是氧化还原反应 |
| D、复分解反应不一定是氧化还原反应 |
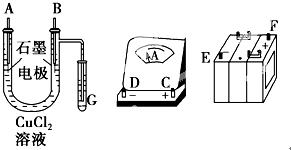 某学生试图用电解法根据电极上析出物质的质量来验证阿伏加德罗常数值,其实验方案的要点为:
某学生试图用电解法根据电极上析出物质的质量来验证阿伏加德罗常数值,其实验方案的要点为: