题目内容
14.下列说法正确的是( )| A. | 按系统命名法,有机物(CH3)2CHCH(CH2CH3)(CH2CH2CH3)的命名为:2-甲基-3-丙基戊烷 | |
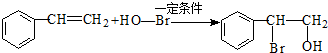
| B. | 已知C-C键可以绕键轴自由旋转,结构简式为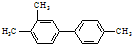 分子中至少有7个碳原子处于同一直线上 分子中至少有7个碳原子处于同一直线上 | |
| C. | 肌醇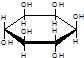 与葡萄糖 与葡萄糖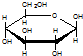 的元素组成相同,化学式均为C6H12O6,满足Cm(H2O)n,因此,均属于糖类化合物 的元素组成相同,化学式均为C6H12O6,满足Cm(H2O)n,因此,均属于糖类化合物 | |
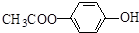
| D. | 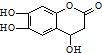 与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H6O6Na4 与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H6O6Na4 |
分析 A、烷烃命名时,要选最长的碳链为主链,从离支链近的一端给主链上碳原子编号,据此分析;
B、由于C-C键可以绕键轴自由旋转,故两个苯环不一定处于同一平面上;
C、根据结构式书写化学式,环上没有标注元素符合的交点为碳原子,肌醇属于醇,不属于糖类;
D、1mol 与能消耗4molNaOH.
与能消耗4molNaOH.
解答 解:A、烷烃命名时,要选最长的碳链为主链,故主链上有6个碳原子,故为己烷,从离支链近的一端给主链上碳原子编号,故在2号和3号碳原子上各有一个甲基和一个乙基,故名称为2-甲基-3-乙基己烷,故A错误;
B、由于C-C键可以绕键轴自由旋转,故两个苯环不一定处于同一平面上,但无论如何旋转, 中至少有6个碳原子共直线,故B错误;
中至少有6个碳原子共直线,故B错误;
C、二者化学式均为C6H12O6,满足Cm(H2O)n,肌醇属于醇,不属于糖类,葡萄糖属于糖类,选项中结葡萄糖为吡喃式构形,故C错误;
D、1mol 含有的2mol酚-OH能消耗2molNaOH,1mol酯基由于能水解为1mol酚羟基和1mol羧基,故能消耗2molNaOH,故1mol此有机物能消耗4molNaOH,反应后产物的分子式为C9H6O6Na4,故D正确.
含有的2mol酚-OH能消耗2molNaOH,1mol酯基由于能水解为1mol酚羟基和1mol羧基,故能消耗2molNaOH,故1mol此有机物能消耗4molNaOH,反应后产物的分子式为C9H6O6Na4,故D正确.
故选D.
点评 本题考查了有机物的命名、原子共直线问题、有机物和NaOH反应后产物的判断等,难度较大,综合性较强.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
4.下列判断合理的是( )
①硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物;
②蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质;
③Na2O2、Fe2O3、A12O3属于碱性氧化物
④根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液;
⑤根据反应中是否有电子的转移将化学反应分为氧化还原反应和非氧化还原反应;
⑥CO2、SO2、NO2都能和碱溶液发生反应,因此它们都属于酸性氧化物.
①硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物;
②蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质;
③Na2O2、Fe2O3、A12O3属于碱性氧化物
④根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液;
⑤根据反应中是否有电子的转移将化学反应分为氧化还原反应和非氧化还原反应;
⑥CO2、SO2、NO2都能和碱溶液发生反应,因此它们都属于酸性氧化物.
| A. | 只有①②④⑤ | B. | 只有①②⑤ | C. | 只有②⑤ | D. | 只有②④⑥ |
2.高效能电池的研发制约电动汽车的推广.有一种新型的燃料电池,它以多孔镍板为电极插入KOH溶液中,然后分别向两极通入乙烷和氧气,其总反应式为:2C2H6+7O2+8KOH═4K2CO3+10H2O,有关此电池的推断正确的是( )
| A. | 负极反应为:14H2O+7O2+28e-═28OH- | |
| B. | 放电过程中KOH的物质的量浓度不变 | |
| C. | 每消耗1molC2H6,则电路上转移的电子为14mol | |
| D. | 放电一段时间后,负极周围的pH升高 |
9.NA为阿伏加德罗常数,下列叙述正确的是( )
| A. | 18gH216O和20gH218O含有的质子数均为10NA | |
| B. | 1L1mol/L的KAl(SO4)2溶液中阳离子总数为2NA | |
| C. | 0.2mol的铁与足量的稀硝酸反应,生成氢气的分子数目为0.3NA | |
| D. | 反应N2+3H2═2NH3达平衡时,每消耗3molH2同时有2NA个N-H断裂 |
6.Li-Al/FeS电池是某科研机构正在研发的一种车载电池,该电池中正极的电极反应式为:2Li++FeS+2e-═Li2S+Fe.有关该电池的下列说法正确的是( )
| A. | Li-Al在电池中作为负极材料,该材料中Li的化合价为+l价 | |
| B. | 用水作电解质溶液 | |
| C. | 该电池的电池反应式为:2Li+FeS═Li2S+Fe | |
| D. | 充电时,阴极发生的电极反应式为:Li2S+Fe-2e-═2Li++FeS |
14.从海水中提取镁的工艺流程图可表示如图:
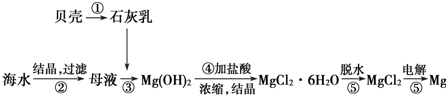
下列说法不正确的是( )

下列说法不正确的是( )
| A. | 用此法提取镁的优点之一是原料来源丰富 | |
| B. | 电解MgCl2时阳极产生镁 | |
| C. | 步骤⑤可将晶体置于HCl气体氛围中脱水制无水氯化镁 | |
| D. | 上述工艺流程中涉及到化合、分解和复分解反应 |
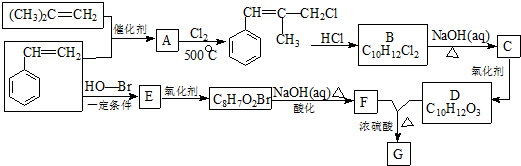
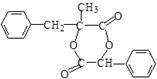 .
. .
. 和
和 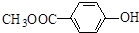 .
.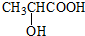 ) 的合成线路
) 的合成线路 .
.