题目内容
17.已知可逆反应aA+bB?cC中,物质的含量A%和C%随温度的变化曲线如图所示,下列说法正确的是( )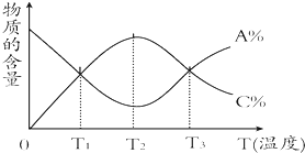
| A. | 该反应在T1、T3温度时达到化学平衡 | |
| B. | 该反应在T2温度时未达到化学平衡 | |
| C. | 升高温度,平衡会向正反应方向移动 | |
| D. | 该反应的正反应是放热反应 |
分析 T2℃之前A%变小,C%从0渐增大,而T2℃之后A%渐大,C%渐小,说明T2℃之前是反应没有达到平衡状态,而T2℃时恰好平衡,T2℃之后是温度升高使平衡向左移动,所以逆反应是吸热反应,正反应为放热反应,据此分析.
解答 解:T2℃之前A%变小,C%从0渐增大,而T2℃之后A%渐大,C%渐小,说明T2℃之前是反应没有达到平衡状态,而T2℃时恰好平衡,T2℃之后是温度升高使平衡向左移动,所以逆反应是吸热反应,正反应为放热反应.
A、T1温度之后A%继续变小,C%继续增大,T3温度之后A%继续增大,C%继续减小,故T1、T3温度时未达到化学平衡,故A错误;
B、T2℃之前A%变小,C%从0渐增大,而T2℃之后A%渐大,C%渐小,而T2℃时恰好平衡,故B错误;
C、T2℃时恰好平衡,T2℃之后A%渐大,C%渐小,说明T2℃之后是温度升高使平衡向左移动,所以逆反应是吸热反应,温度升高使平衡向逆反应移动,故C错误;
D、T2℃时恰好平衡,T2℃之后A%渐大,C%渐小,说明T2℃之后是温度升高使平衡向左移动,所以逆反应是吸热反应,正反应为放热反应,故D正确.
故选:D.
点评 本题考查化学平衡图象、温度对化学平衡的影响,难度中等,明确图象中含量随温度的平衡关系判断T2℃时恰好平衡是解题关键.

练习册系列答案
相关题目
12. 向FeI2、FeBr2的混合溶液中通入适量的氯气,溶液中某些离子的物质的量变化如图所示.下列有关说法中正确的是( )
向FeI2、FeBr2的混合溶液中通入适量的氯气,溶液中某些离子的物质的量变化如图所示.下列有关说法中正确的是( )
 向FeI2、FeBr2的混合溶液中通入适量的氯气,溶液中某些离子的物质的量变化如图所示.下列有关说法中正确的是( )
向FeI2、FeBr2的混合溶液中通入适量的氯气,溶液中某些离子的物质的量变化如图所示.下列有关说法中正确的是( )| A. | 离子的还原性顺序为:Fe2+>I->Br- | |
| B. | 原混合溶液中FeBr2的物质的量为4mol | |
| C. | 原溶液中:n(Fe2+):n(I-):n(Br-)=1:2:3 | |
| D. | 当通入2 mol Cl2时,溶液中发生的离子反应可表示为:2Fe2++2I-+2Cl2═2Fe3++I2+4Cl- |
2.下列叙述正确的是( )
| A. | 某元素基态原最外层有3个未成对电子,最内层有2个电子,其元素符号为N | |
| B. | 某元素的负一价离子的电子层结构与氩相同,其基态原子价电子排布式为[Ne]3s23p5 | |
| C. | 某元素的正三价离子的3d能级为半充满,其基态原子排布式为[Ar]3d64s2 | |
| D. | 某元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,其基态原子的电子排布式为[Ar]3d54s1 |
9.能区别硝酸银、盐酸、氢氧化钾三种溶液的一种试剂是( )
| A. | MgCl2溶液 | B. | FeCl3溶液 | C. | NaNO3溶液 | D. | K2SO4溶液 |
6.100mL Fe2(SO4)3溶液中含有SO42-0.3mol,取25mL溶液稀释到125mL,则稀释后溶液中Fe3+的物质的量浓度是( )
| A. | 0.2 mol/L | B. | 0.3 mol/L | C. | 0.4 mol/L | D. | 0.6 mol/L |
 化学与社会经济建设、生态文明建设、人类健康保障、环境保护等密切相关.
化学与社会经济建设、生态文明建设、人类健康保障、环境保护等密切相关.