题目内容
 SO2(g)+
SO2(g)+| 1 |
| 2 |
SO2(g)完全氧化产生2molSO3(g)的△H=-198kJ/mol.
请回答下列问题:
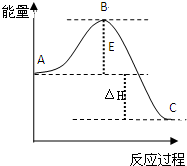
(1)右图中所表示的热化学方程式的意义为
(2)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化.写出该催化循环机理中第二步的化学方程式
(3)已知单质硫的燃烧热为296KJ?mol-1,计算由S(S)生成3.5molSO3(g)放出的热量是
(4)废气中的SO2的含量可用滴定法测量,将一定量的废气通过足量NaOH溶液吸收,然后用碘水滴定,请写出滴定过程中发生的离子方程式
考点:反应热和焓变,二氧化硫的化学性质
专题:化学反应中的能量变化,元素及其化合物
分析:(1)据热化学方程式的含义解答;反应热只与反应物和生成物的能量高低有关;催化剂能够降低反应的活化能;
(2)利用得失电子守恒和原子守恒书写;
(3)利用盖斯定律解答;
(4)利用碘能氧化二氧化硫的原理测定,利用碘与淀粉变蓝色的特性.
(2)利用得失电子守恒和原子守恒书写;
(3)利用盖斯定律解答;
(4)利用碘能氧化二氧化硫的原理测定,利用碘与淀粉变蓝色的特性.
解答:
解:(1)生成2mol三氧化硫放热198KJ,则生成1mol三氧化硫放热99KJ,图示的热化学方程式意义为:在一定的温度和压强下,1molSO2气体与0.5molO2反应生成1molSO3气体放出热量99kJ;E表示反应物活化能,与反应热无关,反应热等于生成物与反应物的能量差;催化剂能够降低反应的活化能,
故答案为:在一定的温度和压强下,1molSO2气体与0.5molO2反应生成1molSO3气体放出热量99kJ;无; 降低; 因为催化剂改变了反应的历程使活化能E降低;
(2)四价钒化合物再被氧气氧化生成V2O5,据得失电子守恒和原子守恒可以形成化学方程式为:4VO2+O2=2V2O5,
故答案为:4VO2+O2=2V2O5;
(3)S的燃烧热加上二氧化硫生成三氧化硫的反应热为1molS生成1mol三氧化硫的反应热为:296KJ/mol+99KJ/mol=395KJ/mol,所以生成3.5mol三氧化硫时放热
395KJ/mol×3.5mol=1382.5KJ,
故答案为:1382.5KJ;
(4)利用碘能氧化亚硫酸根的原理,离子方程式为:SO32-+I2+H2O=SO42-+2I-+2H+;因为碘遇淀粉变蓝色的特性,可以用淀粉溶液作指示剂,当蓝色褪去时达到滴定终点,
故答案为:SO32-+I2+H2O=SO42-+2I-+2H+;淀粉溶液.
故答案为:在一定的温度和压强下,1molSO2气体与0.5molO2反应生成1molSO3气体放出热量99kJ;无; 降低; 因为催化剂改变了反应的历程使活化能E降低;
(2)四价钒化合物再被氧气氧化生成V2O5,据得失电子守恒和原子守恒可以形成化学方程式为:4VO2+O2=2V2O5,
故答案为:4VO2+O2=2V2O5;
(3)S的燃烧热加上二氧化硫生成三氧化硫的反应热为1molS生成1mol三氧化硫的反应热为:296KJ/mol+99KJ/mol=395KJ/mol,所以生成3.5mol三氧化硫时放热
395KJ/mol×3.5mol=1382.5KJ,
故答案为:1382.5KJ;
(4)利用碘能氧化亚硫酸根的原理,离子方程式为:SO32-+I2+H2O=SO42-+2I-+2H+;因为碘遇淀粉变蓝色的特性,可以用淀粉溶液作指示剂,当蓝色褪去时达到滴定终点,
故答案为:SO32-+I2+H2O=SO42-+2I-+2H+;淀粉溶液.
点评:本题考查了热化学方程式的含义、催化剂的催化原理、氧化还原反应方程式的书写、反应热的计算、氧化还原滴定等等,题目有一定难度.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列化学用语表达正确的是( )
| A、乙烯的结构简式:CH2CH2 |
B、丙烯的键线式: |
| C、一定条件下,某密闭容器中充入2molSO2(g)和1molO2(g),达到平衡后,放出QkJ热量,则其热化学方程式为:2SO2(g)+O2(g)═2SO3(g )△H=-QkJ?mol-1 |
| D、甲烷的标准燃烧热△H=-890.3 kJ?mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3kJ?mol-1 |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、在含有大量Al3+的溶液中:K+、Na+、Cl-、HCO3- |
| B、在NaCl溶液中:NH4+、K+、CH3COO-、I- |
| C、0.2mol/L的FeCl3溶液中:NH4+、K+、Br-、SCN- |
| D、pH=1的溶液中:NO3-、SO42-、Na+、Pb2+ |
NA为阿伏加德罗常数,下列说法正确的是( )
| A、1mol 苯中含有碳碳双键的数目为3NA |
| B、28g乙烯所含共用电子对数目为2NA |
| C、1mol-CH3(甲基)中含有电子数为8NA |
| D、现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为3NA |
“能源分类相关图”如图所示,四组能源选项中全部符合图中阴影部分的能源是( )


| A、沼气、风能、太阳能 |
| B、水能、生物能、天然气 |
| C、煤炭、石油、地热能 |
| D、潮汐能、海洋能、核能 |