题目内容
4.下列关于溶液的酸碱性,说法正确的是( )| A. | pH=7的溶液是中性 | |
| B. | 中性溶液中一定有c(H+)=1.0×10-7mol•L-1 | |
| C. | 在100℃时,纯水的pH<7,因此显酸性 | |
| D. | c(OH-)=c(H+)的溶液呈中性 |
分析 A.温度未知,不能根据pH大小判断溶液酸碱性;
B.常温下中性溶液中c(H+)=c(OH-)=1.0×10-7mol•L-1;
C.在100℃时,纯水呈中性.
D.任何水溶液中只要c(H+)=c(OH-),则该溶液一定呈中性.
解答 解:A.在100℃时,纯水的pH=6,呈中性,该温度下pH=7时溶液呈碱性,温度未知,不能根据pH大小判断溶液酸碱性,故A错误;
B.常温下中性溶液中c(H+)=c(OH-)=1.0×10-7mol•L-1,温度不知,中性溶液中不一定有c(H+)=1.0×10-7mol•L-1,故B错误;
C.在100℃时,纯水中存在c(H+)=c(OH-),仍然呈中性,故C错误;
D.任何水溶液中只要存在c(H+)=c(OH-),则该溶液一定呈中性,故D正确;
故选D.
点评 本题考查探究溶液酸碱性判断,为高频考点,要根据溶液中c(H+)、c(OH-)相对大小判断溶液酸碱性,温度未知时不能根据pH大小判断溶液酸碱性,易错选项是B,题目较简单.

练习册系列答案
相关题目
14.某无色透明溶液能与铝作用放出氢气,且溶液中的离子能大量共存的是( )
| A. | K+、NO3-、OH-、Cl- | B. | Cu2+、SO42-、H+、Na+ | ||
| C. | H+、Ba2+、Mg2+、NO3- | D. | NH4+、MnO4-、H+、K+ |
12.纳米材料二氧化钛(TiO2)具有很高的化学活性,可做性能优良的催化剂.
(1)工业上二氧化钛的制备方法是:
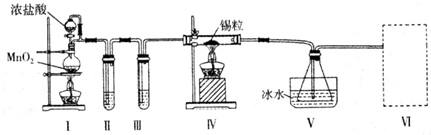
Ⅰ.将干燥后的金红石(主要成分是TiO2,主要杂质是SiO2)与碳粉混合放入氧化炉中,在高温下通入Cl2反应,制得混有SiCl4杂质的TiCl4.
Ⅱ.将SiCl4分离,得到纯净的TiCl4.
Ⅲ.向TiCl4中加水,加热,水解得到沉淀TiO2•xH2O.
Ⅳ.将TiO2•xH2O高温分解得到TiO2.
①据资料卡片中信息判断,TiCl4与SiCl4在常温下的状态是液态;分离二者所采取的操作名称是蒸馏.
②Ⅲ中反应的化学方程式是TiCl4+(x+2)H2O$\frac{\underline{\;\;△\;\;}}{\;}$TiO2•xH2O↓+4HCl.
③如在实验室中完成步骤IV,应将TiO2•xH2O放在坩埚(填字母序号图 1)中加热.
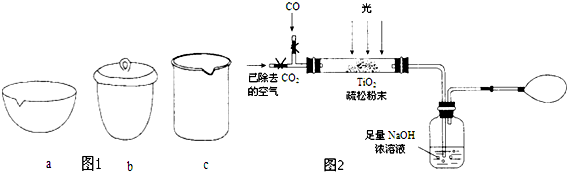
(2)据报道:“生态马路”是在铺设时加入一定量的TiO2,TiO2受太阳光照射后,产生的电子被空气或水中的氧获得,生成H2O2.H2O2能清除路面空气中的CxHy、CO等,其主要是利用了H2O2的氧化性(填“氧化性”或“还原性”).
(3)图2是某研究小组用下列装置模拟“生态马路”的部分原理(夹持装置已略去).
①缓慢通入22.4L(已折算成标准状况)CO气体和足量空气,最终测得NaOH溶液增重11g,则CO的转化率为25%.
②实验①中,当CO气体全部通入后,还要再通一会儿空气,其目的是将生成的CO2气体全部排出被NaOH溶液完全吸收,使实验结果更加精确.
(1)工业上二氧化钛的制备方法是:
Ⅰ.将干燥后的金红石(主要成分是TiO2,主要杂质是SiO2)与碳粉混合放入氧化炉中,在高温下通入Cl2反应,制得混有SiCl4杂质的TiCl4.
Ⅱ.将SiCl4分离,得到纯净的TiCl4.
Ⅲ.向TiCl4中加水,加热,水解得到沉淀TiO2•xH2O.
Ⅳ.将TiO2•xH2O高温分解得到TiO2.
| 资料卡片 | ||
| 物质 | 熔点 | 沸点 |
| SiCl4 | -70℃ | 57.6℃ |
| TiCl4 | -25℃ | 136.5℃ |
②Ⅲ中反应的化学方程式是TiCl4+(x+2)H2O$\frac{\underline{\;\;△\;\;}}{\;}$TiO2•xH2O↓+4HCl.
③如在实验室中完成步骤IV,应将TiO2•xH2O放在坩埚(填字母序号图 1)中加热.

(2)据报道:“生态马路”是在铺设时加入一定量的TiO2,TiO2受太阳光照射后,产生的电子被空气或水中的氧获得,生成H2O2.H2O2能清除路面空气中的CxHy、CO等,其主要是利用了H2O2的氧化性(填“氧化性”或“还原性”).
(3)图2是某研究小组用下列装置模拟“生态马路”的部分原理(夹持装置已略去).
①缓慢通入22.4L(已折算成标准状况)CO气体和足量空气,最终测得NaOH溶液增重11g,则CO的转化率为25%.
②实验①中,当CO气体全部通入后,还要再通一会儿空气,其目的是将生成的CO2气体全部排出被NaOH溶液完全吸收,使实验结果更加精确.
9.2012年12月7日日本明治奶粉检测出放射性核素铯13755Cs而被召回,下列有关铯原子(13755Cs)的说法错误的是( )
| A. | 原子序数为55 | B. | 电子数是55 | C. | 中子数是137 | D. | 质量数是137 |
16.在标准状况下有①6.72L CH4,②3.01×1023个HCl分子,③3.4gNH3.下列对这三种气体的相关量的关系比较不正确的是( )
| A. | 质量:②>①>③ | B. | 氢原子数:②>①>③ | C. | 体积:②>①>③ | D. | 密度:②>③>① |