题目内容
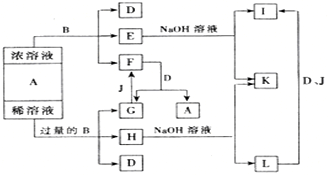
如图,A、B是中学化学里常用的物质,已知A是化合物,B是单质;E溶液中滴入KSCN溶液呈红色.试回答:
(1)B和A的浓溶液反应的条件是 ,简述常温下不易反应的原因 .
(2)写出F和G相互转化的化学方程式
F→G . G→F .
(3)简述L转化为I的现象 ,该反应的化学方程式为 .

(1)B和A的浓溶液反应的条件是
(2)写出F和G相互转化的化学方程式
F→G
(3)简述L转化为I的现象
考点:无机物的推断
专题:推断题
分析:A、B是中学化学里常用的物质,A是化合物,B是单质,E溶液中滴入KSCN溶液呈红色,说明E含有Fe3+离子,E中加入NaOH溶液得到K与I,H溶液中加入NaOH溶液得到K与L,且L与D、J转化得到I,K为钠盐,I为Fe(OH)3,L为Fe(OH)2,H为含Fe2+离子的溶液,推断B为Fe,A为浓硫酸或浓硝酸,两反应均生成D,则D为H2O,故J为O2,由于G与J(氧气)反应得到F,且F与D(水)反应得到A与G,可推知,A为HNO3,F为NO2,G为NO,E为Fe(NO3)3,H为Fe(NO3)2,K为KNO3,据此解答.
解答:
解:A、B是中学化学里常用的物质,A是化合物,B是单质,E溶液中滴入KSCN溶液呈红色,说明E含有Fe3+离子,E中加入NaOH溶液得到K与I,H溶液中加入NaOH溶液得到K与L,且L与D、J转化得到I,K为钠盐,I为Fe(OH)3,L为Fe(OH)2,H为含Fe2+离子的溶液,推断B为Fe,A为浓硫酸或浓硝酸,两反应均生成D,则D为H2O,故J为O2,由于G与J(氧气)反应得到F,且F与D(水)反应得到A与G,可推知,A为HNO3,F为NO2,G为NO,E为Fe(NO3)3,H为Fe(NO3)2,K为KNO3,
(1)常温下,Fe被浓HNO3钝化生成致密的氧化膜,Fe与浓硝酸需要再加热条件下发生反应,故答案为:加热;Fe被浓HNO3钝化生成致密的氧化膜;
(2)F→G的反应方程式为:3NO2+H2O=2HNO3+NO;G→F的反应方程式为:2NO+O2=2NO2,
故答案为:3NO2+H2O=2HNO3+NO;2NO+O2=2NO2;
(3)L转化为I的现象为:白色絮状沉淀迅速变成灰绿色,最后变成红褐色,该反应的化学方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:白色絮状沉淀迅速变成灰绿色,最后变成红褐色;4Fe(OH)2+O2+2H2O=4Fe(OH)3.
(1)常温下,Fe被浓HNO3钝化生成致密的氧化膜,Fe与浓硝酸需要再加热条件下发生反应,故答案为:加热;Fe被浓HNO3钝化生成致密的氧化膜;
(2)F→G的反应方程式为:3NO2+H2O=2HNO3+NO;G→F的反应方程式为:2NO+O2=2NO2,
故答案为:3NO2+H2O=2HNO3+NO;2NO+O2=2NO2;
(3)L转化为I的现象为:白色絮状沉淀迅速变成灰绿色,最后变成红褐色,该反应的化学方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:白色絮状沉淀迅速变成灰绿色,最后变成红褐色;4Fe(OH)2+O2+2H2O=4Fe(OH)3.
点评:本题考查无机物推断,E溶液中滴入KSCN溶液呈红色是推断突破口,再结合转化关系推断,需要学生熟练掌握元素化合物性质,题目难度中等.

练习册系列答案
相关题目
工业上用铝土矿(主要成分为Al2O3,含Fe2O3杂质)为原料冶炼铝的工艺流程如下,下列叙述正确的是( )
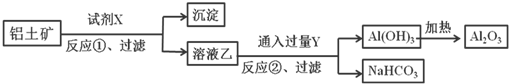

| A、反应①中试剂X是氢氧化钠溶液 |
| B、反应①、过滤后所得沉淀为氢氧化铁 |
| C、图中所示转化反应中包含一个氧化还原反应 |
| D、将试剂X和Y进行对换,最终可以达到相同的效果 |
欲除去下列物质中混入的少量杂质(括号内物质为杂质),不能达到目的是( )
| A、乙酸乙酯(乙酸):加饱和Na2CO3溶液,充分振荡静置后,分液 |
| B、乙醇(水):加入新制生石灰,蒸馏 |
| C、溴苯(溴):加入NaOH溶液,充分振荡静置后,分液 |
| D、乙酸(乙醇):加入金属钠,蒸馏 |
下列操作会使实验结果偏高的是( )
| A、滴定管蒸馏水洗后未用标准液润洗,就直接装入标准液 |
| B、在配置一定量浓度的溶液,定容时蒸馏水加多了,液面超过了刻度线 |
| C、硫酸铜晶体的结晶水测量时,没有在干燥器中冷却 |
| D、测量1mol H2的体积时,镁带表面氧化镁没有擦除 |
以下化石能源的加工所得产品不符合事实的是( )
| A、石油分馏-丙炔 |
| B、石油裂解-乙烯 |
| C、石油裂化-汽油 |
| D、天然气热分解-炭黑 |
下列叙述中正确的是( )
| A、硝酸、硫酸均能将木炭氧化成二氧化碳 |
| B、Na2O2与水反应,Na与水反应均能生成气体 |
| C、C、S分别在氧气中燃烧均可生成两种相应氧化物 |
| D、NaHCO3、Na2CO3、(NH4)2CO3三种固体受热后均能生成气体 |
下列各组反应,最后不生成沉淀的是 ( )
| A、NaAlO2溶液中加过量的盐酸 |
| B、Al2(SO4)2溶液中加过量的氨水 |
| C、NaOH溶液中加入过量的AlCl3溶液 |
| D、AlCl3溶液中加入过量的NaOH溶液. |
