题目内容
A、B、C、D均为中学化学中的常见物质,请根据题中信息回答下列问题:
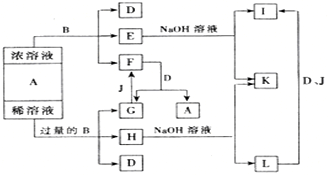
(1)若它们存在如下反应转化关系:A+B→C+D(未配平,反应条件略去).该转化关系中所涉及的反应为非置换反应,且A、D分子的核外电子总数都为10个,B与C能发生反应,则反应的方程式是 .
(2)若它们存在如下反应转化关系:A+B→C+D+H2O(未配平,反应条件略去).
①该转化关系中所涉及的反应为氧化还原反应.若C、D两种气体均能使澄清石灰水变浑浊,鉴别C、D两种气体不能选用下列试剂中的 (填写字母编号).
a.Ba(OH)2溶液 b.酸性KMnO4溶液 c.紫色石蕊试液d.H2O2与BaCl2混合液 e.酸化的Ba(NO3)2溶液
②该转化关系中所涉及的反应为非氧化还原反应.若A是造成温室效应的主要气体之一,C、D均为钠盐,D与B反应能转化为C.当参加反应的A、B物质的量之比为3:4时,则反应所得溶液中各种离子的浓度由大到小的顺序为 .
③若该反应为氧化还原反应,A是一种气体,B、D溶液显碱性,且D溶液具有强氧化性,则在绿矾溶液中加入少量D溶液,发生反应的离子方程式为 .
(1)若它们存在如下反应转化关系:A+B→C+D(未配平,反应条件略去).该转化关系中所涉及的反应为非置换反应,且A、D分子的核外电子总数都为10个,B与C能发生反应,则反应的方程式是
(2)若它们存在如下反应转化关系:A+B→C+D+H2O(未配平,反应条件略去).
①该转化关系中所涉及的反应为氧化还原反应.若C、D两种气体均能使澄清石灰水变浑浊,鉴别C、D两种气体不能选用下列试剂中的
a.Ba(OH)2溶液 b.酸性KMnO4溶液 c.紫色石蕊试液d.H2O2与BaCl2混合液 e.酸化的Ba(NO3)2溶液
②该转化关系中所涉及的反应为非氧化还原反应.若A是造成温室效应的主要气体之一,C、D均为钠盐,D与B反应能转化为C.当参加反应的A、B物质的量之比为3:4时,则反应所得溶液中各种离子的浓度由大到小的顺序为
③若该反应为氧化还原反应,A是一种气体,B、D溶液显碱性,且D溶液具有强氧化性,则在绿矾溶液中加入少量D溶液,发生反应的离子方程式为
考点:无机物的推断
专题:推断题
分析:(1)A、B、C、D均为中学化学中的常见物质,它们存在如下反应转化关系:A+B→C+D,为非置换反应,若A、D分子的核外电子总数都为10个,B与C能发生反应,则A为NH3,D为H2O,该反应为氨气与氧气的反应;
(2)A、B、C、D均为中学化学中的常见物质,它们存在如下反应转化关系:A+B→C+D+H2O,
①为氧化还原反应,若C、D两种气体均能使澄清石灰水变浑浊,C、D可能为二氧化碳或二氧化硫中的一种,该反应为C与浓硫酸的反应,可利用二氧化硫的漂白性和还原剂区别;
②为非氧化还原反应,若A是造成温室效应的主要气体之一,则A为二氧化碳,C、D均为钠盐,D与B反应能转化为C,所以B为NaOH,D为NaHCO3,C为Na2CO3,当参加反应的A、B物质的量之比为3:4时,利用原子守恒计算C、D的物质的量并比较溶液中各种离子的浓度由大到小;
③若该反应为氧化还原反应,A是一种气体,B、D溶液显碱性,且D溶液具有强氧化性,则A为氯气,B为氢氧化钠,D为次氯酸钠,在绿矾溶液中加入少量D溶液,亚铁离子被次氯酸根氧化;
(2)A、B、C、D均为中学化学中的常见物质,它们存在如下反应转化关系:A+B→C+D+H2O,
①为氧化还原反应,若C、D两种气体均能使澄清石灰水变浑浊,C、D可能为二氧化碳或二氧化硫中的一种,该反应为C与浓硫酸的反应,可利用二氧化硫的漂白性和还原剂区别;
②为非氧化还原反应,若A是造成温室效应的主要气体之一,则A为二氧化碳,C、D均为钠盐,D与B反应能转化为C,所以B为NaOH,D为NaHCO3,C为Na2CO3,当参加反应的A、B物质的量之比为3:4时,利用原子守恒计算C、D的物质的量并比较溶液中各种离子的浓度由大到小;
③若该反应为氧化还原反应,A是一种气体,B、D溶液显碱性,且D溶液具有强氧化性,则A为氯气,B为氢氧化钠,D为次氯酸钠,在绿矾溶液中加入少量D溶液,亚铁离子被次氯酸根氧化;
解答:
解:(1)为非置换反应,若A、D分子的核外电子总数都为10个,B与C能发生反应,则A为NH3,D为H2O,该反应为氨气与氧气的反应,反应为4NH3+5O2
4NO+6H2O,
故答案为:4NH3+5O2
4NO+6H2O;
(2)①为氧化还原反应,若C、D两种气体均能使澄清石灰水变浑浊,C、D可能为二氧化碳或二氧化硫中的一种,该反应为C与浓硫酸的反应,可利用二氧化硫的漂白性和还原剂区别,则
a.与Ba(OH)2溶液反应,均生成白色沉淀,不能鉴别,故选;
b.二氧化硫与酸性KMnO4溶液反应使其褪色,二氧化碳不能,可鉴别,故不选;
c.均使紫色石蕊试液变红,不能鉴别,故选;
d.二氧化硫与H2O2与BaCl2混合液反应生成白色沉淀,而二氧化碳不能,可鉴别,故不选;
e.二氧化硫与酸化的Ba(NO3)2溶液反应生成白色沉淀,而二氧化碳不能,可鉴别,故不选,
故答案为:ac;
②非氧化还原反应,若A是造成温室效应的主要气体之一,则A为二氧化碳,B为NaOH,C、D均为钠盐,D与B反应能转化为C,所以D为NaHCO3,C为Na2CO3,当参加反应的A、B物质的量之比为3:4时,设生成C为x,D为y,则
,解得x:y=1:2,溶液中Na2CO3与NaHCO3的物质的量之比为1:2,碳酸根和碳酸氢根水解,溶液呈碱性,所以溶液中各种离子的浓度由大到小为Na+>HCO3->CO32->OH->H+,
故答案为:Na+>HCO3->CO32->OH->H+;
③若该反应为氧化还原反应,A是一种气体,B、D溶液显碱性,且D溶液具有强氧化性,则A为氯气,B为氢氧化钠,D为次氯酸钠,在绿矾溶液中加入少量D溶液,亚铁离子被次氯酸根氧化,反应的离子方程式为6Fe2++3ClO-+3H2O=2Fe(OH)3 ↓+4Fe3++3Cl-,
故答案为:6Fe2++3ClO-+3H2O=2Fe(OH)3 ↓+4Fe3++3Cl-;
| ||
| △ |
故答案为:4NH3+5O2
| ||
| △ |
(2)①为氧化还原反应,若C、D两种气体均能使澄清石灰水变浑浊,C、D可能为二氧化碳或二氧化硫中的一种,该反应为C与浓硫酸的反应,可利用二氧化硫的漂白性和还原剂区别,则
a.与Ba(OH)2溶液反应,均生成白色沉淀,不能鉴别,故选;
b.二氧化硫与酸性KMnO4溶液反应使其褪色,二氧化碳不能,可鉴别,故不选;
c.均使紫色石蕊试液变红,不能鉴别,故选;
d.二氧化硫与H2O2与BaCl2混合液反应生成白色沉淀,而二氧化碳不能,可鉴别,故不选;
e.二氧化硫与酸化的Ba(NO3)2溶液反应生成白色沉淀,而二氧化碳不能,可鉴别,故不选,
故答案为:ac;
②非氧化还原反应,若A是造成温室效应的主要气体之一,则A为二氧化碳,B为NaOH,C、D均为钠盐,D与B反应能转化为C,所以D为NaHCO3,C为Na2CO3,当参加反应的A、B物质的量之比为3:4时,设生成C为x,D为y,则
|
故答案为:Na+>HCO3->CO32->OH->H+;
③若该反应为氧化还原反应,A是一种气体,B、D溶液显碱性,且D溶液具有强氧化性,则A为氯气,B为氢氧化钠,D为次氯酸钠,在绿矾溶液中加入少量D溶液,亚铁离子被次氯酸根氧化,反应的离子方程式为6Fe2++3ClO-+3H2O=2Fe(OH)3 ↓+4Fe3++3Cl-,
故答案为:6Fe2++3ClO-+3H2O=2Fe(OH)3 ↓+4Fe3++3Cl-;
点评:本题考查无机物的推断,综合考查元素化合物知识,较好的考查学生分析能力、计算能力及知识综合应用能力,答题时要注意熟记常见元素化合物知识,题目难度中等.

练习册系列答案
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案
相关题目
某学生的实验报告所列出的下列数据中合理的是( )
| A、用10mL量筒量取7.13mL稀盐酸 |
| B、用酸式滴定管量取13.17mL稀盐酸 |
| C、用广泛pH试纸测得某溶液的pH为2.3 |
| D、用天平称取物品的质量为5.872g |
下列叙述正确的是( )
| A、稀释浓硫酸时,应将蒸馏水沿玻璃棒缓慢注入浓硫酸中 |
| B、配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出 |
| C、分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D、从碘水中提取单质碘时,可以用无水乙醇代替CCl4 |
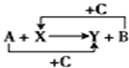 已知A、B、C是单质且C是绿色植物光合作用的产物之一,X、Y是化合物,它们之间的转化关系如图(反应条件略).下列A、B间的对应关系,不正确的是( )
已知A、B、C是单质且C是绿色植物光合作用的产物之一,X、Y是化合物,它们之间的转化关系如图(反应条件略).下列A、B间的对应关系,不正确的是( )| A、A是铝,B是铁 |
| B、A是碳,B是硅 |
| C、A是氢气,B是铜 |
| D、A是钠,B是氢气 |
一些装有化学物质的容器上常贴有危险化学品的标志.下列标志中,应贴在装有酒精的容器上的是( )
A、 剧毒品 |
B、 易燃液体 |
C、 氧化剂 氧化剂 |
D、 遇湿易燃物品 |
关于小苏打水溶液的表述正确的是( )
| A、c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3) |
| B、c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-) |
| C、HCO3-的电离程度大于HCO3-的水解程度 |
| D、存在的电离有:NaHCO3=Na++HCO3-,HCO3-=H++CO32- |
在溶液中能大量共存,且溶液为无色透明的离子组是( )
| A、K+、Cu2+、Na+、Cl- |
| B、K+、NO3-、Na+、CO32- |
| C、H+、NO3-、Na+、HCO3- |
| D、Ag+、Na+、Cl-、SO42- |
常温常压下,下列气体在水中的溶解度最大的是( )
| A、NH3 |
| B、NO |
| C、Cl2 |
| D、H2 |