题目内容
下列两种物质间发生反应,消耗等物质的量的酸,产生气体最多的是( )
| A、木炭与浓硝酸 |
| B、铜与稀硝酸 |
| C、锌与稀硫酸 |
| D、木炭与浓硫酸 |
考点:浓硫酸的性质,硝酸的化学性质
专题:元素及其化合物
分析:A.木炭与浓硝酸反应:C+4HNO3=CO2↑+4NO2↑+2H2O;
B.铜与稀硝酸反应:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O;
C.锌与稀硫酸反应:Zn+H2SO4=ZnSO4+H2↑;
D.木炭与浓硫酸:C+2H2SO4(浓)CO2↑+2SO2↑+2H2O;
依据方程式分别取相同物质的量的酸计算产生气体的物质的量.
B.铜与稀硝酸反应:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O;
C.锌与稀硫酸反应:Zn+H2SO4=ZnSO4+H2↑;
D.木炭与浓硫酸:C+2H2SO4(浓)CO2↑+2SO2↑+2H2O;
依据方程式分别取相同物质的量的酸计算产生气体的物质的量.
解答:
解:各取1mol酸分别计算生成气体的物质的量.
A.依据反应C+4HNO3=CO2↑+4NO2↑+2H2O,消耗1mol硝酸生成
mol气体;
B.依据反应3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,消耗1mol硝酸生成
mol气体;
C.依据反应Zn+H2SO4=ZnSO4+H2↑,消耗1mol稀硫酸生成1mol气体;
D.依据反应C+2H2SO4(浓)CO2↑+2SO2↑+2H2O,消耗1mol浓硫酸生成
mol气体;
所以消耗相同物质的量的酸生成气体最的是D,
故选:D.
A.依据反应C+4HNO3=CO2↑+4NO2↑+2H2O,消耗1mol硝酸生成
| 5 |
| 4 |
B.依据反应3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,消耗1mol硝酸生成
| 1 |
| 4 |
C.依据反应Zn+H2SO4=ZnSO4+H2↑,消耗1mol稀硫酸生成1mol气体;
D.依据反应C+2H2SO4(浓)CO2↑+2SO2↑+2H2O,消耗1mol浓硫酸生成
| 3 |
| 2 |
所以消耗相同物质的量的酸生成气体最的是D,
故选:D.
点评:本考查了浓硫酸和浓硝酸的性质及相关计算,解题关键是正确书写出各个反应的化学方程式,依据方程式中消耗酸和生成气体的物质的量之比计算解答,题目难度不大.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案
相关题目
下列反应对应的离子方程式书写正确的是( )
| A、用氢氟酸在玻璃上“刻字”:SiO2+4H++4F-═SiF4↑+2H2O |
| B、实验室制取氯气:2MnO4-+8H++6Cl-═2MnO2↓+3Cl2↑+4H2O |
| C、将铁粉放入硫酸铁和硫酸铜的混合溶液中,初始阶段发生的反应:Fe+2Fe3+═3Fe2+ |
| D、常温下,铁与过量的浓硝酸反应:Fe+6H++3NO3-═Fe3++3NO2↑+3H2O |
根据如图的转化关系判断下列说法正确的是(反应条件已略去)( )
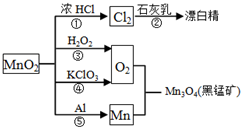

| A、反应①②③④⑤均属于氧化反应和离子反应 |
| B、反应⑤说明该条件下铝的还原性强于锰 |
| C、相同条件下生成等量的O2,反应③和④转移的电子数之比为1:1 |
| D、反应①中氧化剂与还原剂的物质的量之比为1:4 |
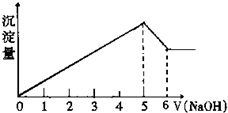 有一镁、铝合金,在适量稀硫酸中恰好完全溶解,再加入氢氧化钠溶液,析出沉淀的物质的量随氢氧化钠溶液的体积变化如图所示,则合金中镁、铝的物质的量之比为( )
有一镁、铝合金,在适量稀硫酸中恰好完全溶解,再加入氢氧化钠溶液,析出沉淀的物质的量随氢氧化钠溶液的体积变化如图所示,则合金中镁、铝的物质的量之比为( )| A、2:1 | B、4:1 |
| C、1:1 | D、1:2 |
下列解释事实的方程式不准确的是( )
A、铝热法炼铁:Fe2O3+2Al
| ||||
B、工业上用NH3制备NO:4NH3+5O2
| ||||
| C、向受酸雨影响的湖泊中喷洒CaCO3粉末:CO32-+2H+═H2O+CO2↑ | ||||
| D、过氧化钠用于呼吸面具中作为氧气的来源:2Na2O2+2CO2═2Na2CO3+O2 |
下列事实、离子方程式及其对应关系均正确的是.( )
| A、向淀粉碘化钾溶液中滴加稀硫酸,在空气中放置一段时间后溶液变蓝:4H++4I-+O2═2I2+2H2O | ||||
| B、向K2Cr2O7溶液中滴加少量浓硫酸,溶液变为黄色:Cr2O72-(橙色)+H2O?2CrO42-(黄色)+2H+ | ||||
| C、0.01mol?L-1 NH4Al(SO4)2溶液与0.02mol?L-1 Ba(OH)2溶液等体积混合有白色沉淀生成:Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O | ||||
D、用铜电极电解饱和食盐水:2Cl-+2H2O
|
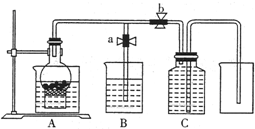 某同学设计如图所示装置来试验用粗铁粒与某浓度稀硝酸反应制取NO气体.
某同学设计如图所示装置来试验用粗铁粒与某浓度稀硝酸反应制取NO气体.