题目内容
下列解释事实的方程式不准确的是( )
A、铝热法炼铁:Fe2O3+2Al
| ||||
B、工业上用NH3制备NO:4NH3+5O2
| ||||
| C、向受酸雨影响的湖泊中喷洒CaCO3粉末:CO32-+2H+═H2O+CO2↑ | ||||
| D、过氧化钠用于呼吸面具中作为氧气的来源:2Na2O2+2CO2═2Na2CO3+O2 |
考点:化学方程式的书写,离子方程式的书写
专题:化学用语专题
分析:A.铝热法炼铁原理是铝和氧化铁在高温下发生置换反应;
B.高温、高压、催化剂条件下,氨气被氧化生成NO;
C.难溶物写化学式;
D.过氧化钠能和二氧化碳反应生成氧气.
B.高温、高压、催化剂条件下,氨气被氧化生成NO;
C.难溶物写化学式;
D.过氧化钠能和二氧化碳反应生成氧气.
解答:
解:A.铝热法炼铁原理是铝和氧化铁在高温下发生置换反应,反应方程式为Fe2O3+2Al
Al2O3+2Fe,故A正确;
B.高温、高压、催化剂条件下,氨气被氧化生成NO,反应方程式为4NH3+5O2
4NO+6H2O,故B正确;
C.难溶物写化学式,离子方程式为CaCO3+2H+═H2O+CO2↑+Ca2+,故C错误;
D.过氧化钠能和二氧化碳反应生成氧气,反应方程式为2Na2O2+2CO2═2Na2CO3+O2,故D正确;
故选C.
| ||
B.高温、高压、催化剂条件下,氨气被氧化生成NO,反应方程式为4NH3+5O2
| ||
| 高温高压 |
C.难溶物写化学式,离子方程式为CaCO3+2H+═H2O+CO2↑+Ca2+,故C错误;
D.过氧化钠能和二氧化碳反应生成氧气,反应方程式为2Na2O2+2CO2═2Na2CO3+O2,故D正确;
故选C.
点评:本题考查了化学反应方程式及离子方程式的书写,明确物质间的反应是解本题关键,知道金属冶炼方法的选取与金属活泼性强弱之间的关系,氨的催化氧化是高考高频点,要熟练掌握元素化合物知识.

练习册系列答案
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
现有常温下的五种溶液(如表).下列有关叙述中正确的是( )
| (1) | (2) | (3) | (4) | (5) | |
| 溶液 | 氨水 | 氢氧化钠 | 醋酸 | 盐酸 | 醋酸铵 |
| pH | 11 | 11 | 3 | 3 | 8.3 |
| A、五种溶液中,水电离出的c(OH-)最小的是⑤ |
| B、将①、④两种溶液等体积混合,所得溶液中:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| C、分别将①、②、③、④加水稀释100倍,稀释后四种溶液的pH:①>②>③>④ |
| D、在⑤中加入适量的④至溶液呈中性,所得溶液中:c(Na+)>c(CH3COO-)>c(Cl-)>c(H+)=c(OH-) |
下列实验,能达到实验目的是( )
A、 配置一定物质的量浓度的H2SO4溶液 |
B、 收集和吸收多余的SO2 |
C、 保护钢闸门不被腐蚀 |
D、 制取和收集NO2 |
下列两种物质间发生反应,消耗等物质的量的酸,产生气体最多的是( )
| A、木炭与浓硝酸 |
| B、铜与稀硝酸 |
| C、锌与稀硫酸 |
| D、木炭与浓硫酸 |
下列离子或分子组中大量共存且满足相应要求的是( )
| A、K+、AlO2-、Cl-、MnO4- 要求:无色澄清溶液 |
| B、Fe3+、NO3-、I-、HCO3- 要求:逐滴滴加盐酸立即产生气体 |
| C、Na+、K+、Ag+、NO3- 要求:逐滴滴加氨水先有沉淀产生,后沉淀消失 |
| D、NH4+、Al3+、SO42-、CH3COOH 要求:滴加NaOH浓溶液立刻产生气体 |
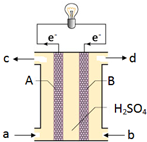 “长征”火箭发射使用的燃料是偏二甲肼(C2H8N2),并使用四氧化二氮作为氧化剂,这种组合的两大优点是,既能在短时间内产生巨大能量将火箭送上太空,产物又不污染空气(产物都是空气成分).某校外研究性学习小组拟将此原理设计为原电池,如图所示,结合学习过的电化学原理分析其设计方案,下列说法正确的是( )
“长征”火箭发射使用的燃料是偏二甲肼(C2H8N2),并使用四氧化二氮作为氧化剂,这种组合的两大优点是,既能在短时间内产生巨大能量将火箭送上太空,产物又不污染空气(产物都是空气成分).某校外研究性学习小组拟将此原理设计为原电池,如图所示,结合学习过的电化学原理分析其设计方案,下列说法正确的是( )| A、B为正极 |
| B、从a口通入四氧化二氮气体 |
| C、从d口排除的是NO气体 |
| D、A极发生的电极反应式:C2H8N2-16e-+8H2O=CO2+N2+16H+ |
某有机物的结构如图所示,下列有关它的说法正确的是( )


| A、能与氢氧化钠溶液反应 |
| B、4个碳原子可能在同一平面内 |
| C、与它具有相同官能团的同分异构体还有4种 |
| D、与乙醇互为同系物 |
下列说法正确的是( )
| A、在中和热的测定实验中,将氢氧化钠溶液迅速倒入盛有盐酸的量热计中,立即读出并记录溶液的起始温度 |
B、如图,一段时间后给烧杯内地溶液中加入黄色的K3[Fe(CN)6]溶液,可看到Fe电极附近有蓝色沉淀生成 |
| C、用标准盐酸滴定待测NaOH溶液,水洗后的酸式滴定管未经标准液润洗,则测定结果偏低 |
| D、用加热的方式可提取NH4Cl固体中混有的少量的碘 |