题目内容
利用实验仪器(规格和数量不限),能完成相应实验的一项是( )
| 选项 | 实验仪器(省略夹持装置) | 相应实验 |
| A | 烧杯、玻璃棒、酒精灯 | 溶液的浓缩结晶 |
| B | 蒸馏烧瓶、冷凝管、酒精灯 | 由工业酒精制无水酒精 |
| C | 天平、玻璃棒、胶头滴管、容量瓶 | 配制0.5mol?L-1的溶液100mL |
| D | 烧杯、玻璃棒、胶头滴管、分液漏斗 | 用溴水和CCl4除去NaBr溶液中的少量NaI |
| A、A | B、B | C、C | D、D |
考点:过滤、分离与注入溶液的仪器,计量仪器及使用方法
专题:化学实验常用仪器
分析:A.溶液的蒸发浓缩实验中,需要使用蒸发皿;
B.蒸馏操作中,需要使用温度计控制馏分的温度;
C.配制一定浓度的溶液时,需要在烧杯中溶解或稀释;
D.用溴水和CCl4除去NaBr溶液中的少量NaI,应在烧杯中反应后用分液的方法分离.
B.蒸馏操作中,需要使用温度计控制馏分的温度;
C.配制一定浓度的溶液时,需要在烧杯中溶解或稀释;
D.用溴水和CCl4除去NaBr溶液中的少量NaI,应在烧杯中反应后用分液的方法分离.
解答:
解:A.提供的仪器中,缺少蒸发皿,无法完成溶液的蒸发浓缩,故A错误;
B.没有温度计,无法通过蒸馏操作用工业酒精制无水酒精,故B错误;
C.仪器中没有烧杯,无法稀释或者溶解溶质,故C错误;
D.用溴水和CCl4除去NaBr溶液中的少量NaI,应用烧杯中反应后用分液的方法分离,用到的仪器有烧杯、玻璃棒、胶头滴管、分液漏斗等,可完成实验,故D正确;
故选D.
B.没有温度计,无法通过蒸馏操作用工业酒精制无水酒精,故B错误;
C.仪器中没有烧杯,无法稀释或者溶解溶质,故C错误;
D.用溴水和CCl4除去NaBr溶液中的少量NaI,应用烧杯中反应后用分液的方法分离,用到的仪器有烧杯、玻璃棒、胶头滴管、分液漏斗等,可完成实验,故D正确;
故选D.
点评:本题考查较为综合,涉及基础实验操作,侧重于学生的分析能力和实验能力的考查,为高频考点,注意把握实验的方法、步骤和使用的仪器,注重相关基础知识的积累,难度不大.

练习册系列答案
相关题目
下列说法正确的是( )
| A、在氨水中加入少量的水或氯化铵固体后,都能使溶液中的c(OH-)减小 |
| B、反应Hg(l)+H2SO4(aq)═HgSO4(aq)+H2(g)在常温下不能自发进行,则△H<0 |
| C、工业电解食盐水中,电解池被阳离子交换膜隔成阴极室和阳极室,目的是避免阳极产生的气体与烧碱反应 |
| D、在等浓度的NaCl和Na2CrO4稀溶液中滴加AgNO3溶液,先析出AgCl沉淀,则Ksp(AgCl)<Ksp(Ag2CrO4) |
向NaOH(aq)滴入HCOOH(aq)的过程中,所得到的混合溶液中离子浓度的大小关系可能正确的是( )
| A、c(OH-)=c(Na+)>c(HCOO-)>c(H+) |
| B、c(Na+)=c(HCOO-) |
| C、c(Na+)>c(HCOO-)>c(OH-)>c(H+) |
| D、c(H+)>c(HCOO-)>c(Na+)>c(OH-) |
下列两种物质间发生反应,消耗等物质的量的酸,产生气体最多的是( )
| A、木炭与浓硝酸 |
| B、铜与稀硝酸 |
| C、锌与稀硫酸 |
| D、木炭与浓硫酸 |
某有机物的分子式为C9H9ClO2,分子中含有1个苯环,苯环上有两个取代基,并能与NaHCO3溶液反应的同分异构体的数目为(不考虑立体异构)( )
| A、12种 | B、15种 |
| C、18种 | D、21种 |
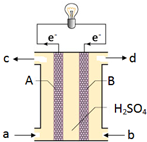 “长征”火箭发射使用的燃料是偏二甲肼(C2H8N2),并使用四氧化二氮作为氧化剂,这种组合的两大优点是,既能在短时间内产生巨大能量将火箭送上太空,产物又不污染空气(产物都是空气成分).某校外研究性学习小组拟将此原理设计为原电池,如图所示,结合学习过的电化学原理分析其设计方案,下列说法正确的是( )
“长征”火箭发射使用的燃料是偏二甲肼(C2H8N2),并使用四氧化二氮作为氧化剂,这种组合的两大优点是,既能在短时间内产生巨大能量将火箭送上太空,产物又不污染空气(产物都是空气成分).某校外研究性学习小组拟将此原理设计为原电池,如图所示,结合学习过的电化学原理分析其设计方案,下列说法正确的是( )| A、B为正极 |
| B、从a口通入四氧化二氮气体 |
| C、从d口排除的是NO气体 |
| D、A极发生的电极反应式:C2H8N2-16e-+8H2O=CO2+N2+16H+ |
下列说法中正确的是( )
| A、NO2溶于水得到HNO3,所以NO2属于酸性氧化物 |
| B、过氧化钠与水反应的离子方程式为:Na2O2+2H2O═2Na++2OH-+O2↑ |
| C、漂白粉和水玻璃长期暴露在空气中失效,其原理完全相同 |
| D、足量Zn与一定量浓硫酸充分反应得到混合气体 |
室温下,下列各组离子在指定溶液中能大量共存的是( )
| A、在pH=0的溶液中:Cl-、Na+、K+、C6H5-O-(C6H5一为苯基) |
| B、加入铝屑有氢气放出的溶液中:NH4+、K+、HCO3-、Br- |
| C、在H2SO3溶液中:HSO3-、K+、Cl-、Ba2+ |
| D、在葡萄糖(C6H12O6)溶液中:SO42-、MnO4-、K+、H+ |
设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A、1mol?L-1 Na2CO3溶液中,含CO32-数目小于NA |
| B、标准状况下,11.2L O2和O3组成的混合气体含有原子数为NA |
| C、14 g聚乙烯与聚丙烯的混合物,含C-H键的数目为2NA |
| D、常温常压下,22.4L CO2与足量Na2O2反应转移电子数为NA |