题目内容
11.A、B、C、D四种元素在周期表中分别处于元素X的四周(如图),已知X元素最高价氧化物的化学式为X2O5,且五种元素中有一种元素的原子半径是它所处的同族中最小的.试确定:| B | ||
| A | X | C |
| D |
A:硅,B:氮,C:硫,D:砷.
(2)C、D、X最高价氧化物对应水化物酸性由强到弱的顺序:(填化学式)H2SO4>H3PO4>H3ASO4
(3)写出A、B、X气态氢化物的化学式,并排列稳定性由强到弱的顺序:NH3>PH3>SiH4.
(4)下列关于D元素化合物的性质叙述中不正确的是C
A.D的单质在通常状况下是固体
B.D难以与H2化合生成氢化物
C.气态氢化物有两种,为DH3和DH5.
分析 A、B、C、D四种元素在周期表中分别处于元素X的四周,X元素最高价氧化物的化学式为X2O5,则X处于VA族,且五种元素中有一种元素的原子半径是它所处的同族中最小的,由元素位置可知,B为N元素、A为Si、X为P、C为S、D为As.
解答 解:A、B、C、D四种元素在周期表中分别处于元素X的四周,X元素最高价氧化物的化学式为X2O5,则X处于VA族,且五种元素中有一种元素的原子半径是它所处的同族中最小的,由元素位置可知,B为N元素、A为Si、X为P、C为S、D为As.
(1)A为硅,B为氮,C为硫,D为砷,故答案为:硅;氮;硫;砷;
(2)由于非金属性S>P>As,故最高价氧化物对应水化物酸性由强到弱的顺序:H2SO4>H3PO4>H3ASO4,
故答案为:H2SO4>H3PO4>H3ASO4;
(3)非金属性N>P>Si,故气态氢化物稳定性由强到弱的顺序:NH3>PH3>SiH4,
故答案为:NH3>PH3>SiH4;
(4)A.As的单质在通常状况下是固体,故A正确;
B.As的非金属性比P弱,难以与H2化合生成氢化物,故B正确;
C.As气态氢化物为PH3,故C错误,
故选:C.
点评 本题考查元素周期表与元素周期律应用,熟练掌握元素周期律表的结构,注意对基础知识的理解掌握.

练习册系列答案
 小题狂做系列答案
小题狂做系列答案
相关题目
1.下列有机物名称正确的是( )
| A. | 2-乙基戊烷 | B. | 1,2-二氯丁烷 | ||
| C. | 2,2-二甲基-4-己烯 | D. | 3,4-二甲基辛烷 |
2.下列说法正确的是( )
| A. | 纯净物是指由同种元素组成的物质 | B. | 由同种元素组成的纯净物叫单质 | ||
| C. | 由不同种分子组成的物质叫化合物 | D. | 一种元素只能组成一种单质 |
6.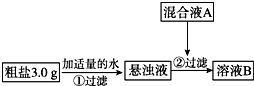 目前国内外使用的融雪剂一般有两大类:一类是以醋酸钾为主要成分的有机融雪剂;另一类是以“氯盐”为主要成分的无机融雪剂,如氯化钠、氯化钙、氯化镁等,通称“化冰盐”.某研究性学习小组拟对融雪氯盐(如图称为粗盐)(主要含有氯化钠及不溶性杂质、Mg2+、Ca2+等)进行回收提纯研究.
目前国内外使用的融雪剂一般有两大类:一类是以醋酸钾为主要成分的有机融雪剂;另一类是以“氯盐”为主要成分的无机融雪剂,如氯化钠、氯化钙、氯化镁等,通称“化冰盐”.某研究性学习小组拟对融雪氯盐(如图称为粗盐)(主要含有氯化钠及不溶性杂质、Mg2+、Ca2+等)进行回收提纯研究.
该小组设计流程如图:
(1)加入混合液A的主要成分是NaOH、Na2CO3 (填化学式).
(2)为检验溶液B中的Mg2+、Ca2+,通常分别取少量溶液B于两支试管中,进行如下实验:
步骤一:检验Mg2+,向其中一支试管中加入NaOH溶液(填化学式),看是否有沉淀生成.
步骤二:检验Ca2+,向另一支试管中加入某溶液,看是否有沉淀生成.下列三种溶液,其沉淀效果最好的是A.
A.0.1mol•L-1 Na2CO3溶液
B.0.1mol•L-1 Na2SO3溶液
C.0.1mol•L-1 Na2C2O4溶液
(3)在除杂过程中,向粗盐悬浊液中加混合液A时需控制溶液pH=12以确保Mg2+除尽,根据提供的数据计算,溶液B中Mg2+物质的量浓度将被控制在1.8×10-7mol•L-1以下.
(4)对溶液B加热并不断滴加6mol•L-1的盐酸,同时用pH试纸检测溶液,直至pH=2时停止加盐酸,得到溶液C.该操作的目的是除去NaOH和Na2CO3.
(5)溶液C倒入蒸发皿中,加热蒸发并不断搅拌,直到有大量固体析出时停止加热.
(6)足量CaCO3固体分别加入:①30mL水 ②10mL 0.2mol/LNa2CO3溶液 ③50mL 0.01mol/L氯化钙溶液 ④100mL 0.01mol/L盐酸中溶解至溶液饱和.
请确定各溶液中Ca2+的浓度由大到小的顺序为:③④①②.
 目前国内外使用的融雪剂一般有两大类:一类是以醋酸钾为主要成分的有机融雪剂;另一类是以“氯盐”为主要成分的无机融雪剂,如氯化钠、氯化钙、氯化镁等,通称“化冰盐”.某研究性学习小组拟对融雪氯盐(如图称为粗盐)(主要含有氯化钠及不溶性杂质、Mg2+、Ca2+等)进行回收提纯研究.
目前国内外使用的融雪剂一般有两大类:一类是以醋酸钾为主要成分的有机融雪剂;另一类是以“氯盐”为主要成分的无机融雪剂,如氯化钠、氯化钙、氯化镁等,通称“化冰盐”.某研究性学习小组拟对融雪氯盐(如图称为粗盐)(主要含有氯化钠及不溶性杂质、Mg2+、Ca2+等)进行回收提纯研究.| 化学式 | CaCO3 | CaSO3 | CaC2O4 | Mg(OH)2 |
| Ksp | 2.8×10-9 | 6.8×10-8 | 4.0×10-9 | 1.8×10-11 |
(1)加入混合液A的主要成分是NaOH、Na2CO3 (填化学式).
(2)为检验溶液B中的Mg2+、Ca2+,通常分别取少量溶液B于两支试管中,进行如下实验:
步骤一:检验Mg2+,向其中一支试管中加入NaOH溶液(填化学式),看是否有沉淀生成.
步骤二:检验Ca2+,向另一支试管中加入某溶液,看是否有沉淀生成.下列三种溶液,其沉淀效果最好的是A.
A.0.1mol•L-1 Na2CO3溶液
B.0.1mol•L-1 Na2SO3溶液
C.0.1mol•L-1 Na2C2O4溶液
(3)在除杂过程中,向粗盐悬浊液中加混合液A时需控制溶液pH=12以确保Mg2+除尽,根据提供的数据计算,溶液B中Mg2+物质的量浓度将被控制在1.8×10-7mol•L-1以下.
(4)对溶液B加热并不断滴加6mol•L-1的盐酸,同时用pH试纸检测溶液,直至pH=2时停止加盐酸,得到溶液C.该操作的目的是除去NaOH和Na2CO3.
(5)溶液C倒入蒸发皿中,加热蒸发并不断搅拌,直到有大量固体析出时停止加热.
(6)足量CaCO3固体分别加入:①30mL水 ②10mL 0.2mol/LNa2CO3溶液 ③50mL 0.01mol/L氯化钙溶液 ④100mL 0.01mol/L盐酸中溶解至溶液饱和.
请确定各溶液中Ca2+的浓度由大到小的顺序为:③④①②.
3.下列物质不能通过化合反应直接制得的是( )
| A. | SO2 | B. | H2SiO3 | C. | CuCl2 | D. | Fe﹙OH﹚3 |
20.下列反应属于取代反应的是( )
| A. | CH4+2O2$\stackrel{点燃}{→}$CO2+2H2O | |
| B. | CH2=CH2+Br2→BrCH2CH2Br | |
| C. | CH3CH2CH2Cl+NaOH $→_{△}^{酸}$CH3CH=CH+NaCl+H2O | |
| D. | 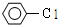 +H2O$→_{△}^{酸}$ +H2O$→_{△}^{酸}$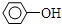 +HCl +HCl |
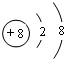 .
.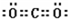 .
.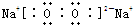 ,其中含有的化学键有离子键、共价键.用电子式表示B、D的单质在常温下反应生成的化合物的形成过程:
,其中含有的化学键有离子键、共价键.用电子式表示B、D的单质在常温下反应生成的化合物的形成过程: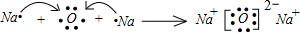 .
.