题目内容
11.下列关于阳离子的说法中错误的是( )①阳离子都是由一个金属原子失去电子而形成的
②非金属原子不能形成阳离子
③阳离子的电子排布一定与稀有气体相同
④阳离子的价态不会大于其原子的最外层电子数
⑤阳离子都是稳定结构,不会再失去电子.
| A. | ①④ | B. | ②④ | C. | ①②③ | D. | ①②③④⑤ |
分析 ①铵根离子中不存在金属原子;
②非金属原子能形成阳离子,如铵根离子;
③阳离子的电子排布不一定与稀有气体相同,如氢离子;
④阳离子的价态可能大于其原子的最外层电子数;
⑤阳离子不都是稳定结构,可能会再失去电子.
解答 解:①阳离子不一定是由一个金属原子失去电子而形成的,如铵根离子,故①错误;
②铵根离子为阳离子,所以非金属原子也可以形成阳离子,故②错误;
③氢离子核外电子数为0,所以阳离子的电子排布不一定与稀有气体相同,故③错误;
④阳离子的价态可能大于其原子的最外层电子数,如铁的最外层电子数为2,可以为+2价,+3价,故④错误;
⑤阳离子不都是稳定结构,可能会再失去电子,如亚铁离子,故⑤错误;
故选D.
点评 本题考查原子结构与性质,题目难度不大,明确阴阳离子构成特点为解答关键,易错选项是①,非金属原子也能形成阳离子,试题有利于提高学生的灵活应用能力.

练习册系列答案
相关题目
1.阅读表短周期主族元素的相关信息:
请回答:
(1)写出E在元素周期表中的位置:第二周期第ⅣA族;C的简单离子的结构示意图: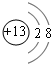 .
.
(2)X的化学式为NaClO.
(3)A、B、C三种元素的简单离子的半径由大到小的顺序为O2->Na+>Al3+(用离子符号表示).
(4)A、B两元素组成的化合物A2B2属于离子化合物(填“离子”或“共价”化合物).
(5)C元素形成的单质能与A的最高价氧化物对应的水化物反应,其离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑.
| 元素代号 | 相关信息 |
| A | A的单质能与冷水剧烈反应,得到强碱性溶液 |
| B | B的原子最外层电子数是其内层电子数的三倍 |
| C | 在第3周期元素中,C的简单离子半径简单最小 |
| D | A、B、D组成的36电子的化合物X是家用消毒剂的主要成分 |
| E | 所有有机物中都含有E元素 |
(1)写出E在元素周期表中的位置:第二周期第ⅣA族;C的简单离子的结构示意图:
 .
.(2)X的化学式为NaClO.
(3)A、B、C三种元素的简单离子的半径由大到小的顺序为O2->Na+>Al3+(用离子符号表示).
(4)A、B两元素组成的化合物A2B2属于离子化合物(填“离子”或“共价”化合物).
(5)C元素形成的单质能与A的最高价氧化物对应的水化物反应,其离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑.
2.下列有关实验基本操作或现象的描述不正确的是( )
| A. | 稀释浓硫酸时,将浓硫酸沿器壁慢慢注入水中,并不断搅拌 | |
| B. | 溶剂蒸发的速率越快,或浓缩后的溶液冷却得越快,析出的晶体颗粒就越大 | |
| C. | 油脂在热NaOH溶液中完全水解后加入饱和食盐水,可观察到液面上有固体析出 | |
| D. | 制备NaCl晶体时,晶体表面含有少量KNO3,用水淋洗后可得到较纯净的NaC1 |
19.天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂.关于维生素P的叙述错误的是( )
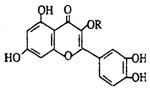

| A. | 可溶于有机溶剂 | B. | 分子中有三个苯环 | ||
| C. | 1mol维生素P可以和6molBr2反应 | D. | 1mol维生素P可以和4molNaOH反应 |
6.下列事实不能用元素周期律解释的只有( )
| A. | 碱性:KOH>NaOH | B. | 元素的金属性:Mg>Al | ||
| C. | 酸性:HNO3>H2CO3 | D. | 相对原子质量:Ar>K |
16.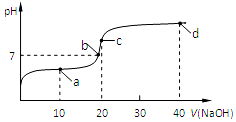 室温时,向20mL,0.1mol/L的醋酸溶液中不断滴加0.1mol/L的NaOH溶液,溶液的pH变化曲线如图所示,在滴定过程中,下列关于溶液中离子浓度大小关系的描述不正确的是( )
室温时,向20mL,0.1mol/L的醋酸溶液中不断滴加0.1mol/L的NaOH溶液,溶液的pH变化曲线如图所示,在滴定过程中,下列关于溶液中离子浓度大小关系的描述不正确的是( )
 室温时,向20mL,0.1mol/L的醋酸溶液中不断滴加0.1mol/L的NaOH溶液,溶液的pH变化曲线如图所示,在滴定过程中,下列关于溶液中离子浓度大小关系的描述不正确的是( )
室温时,向20mL,0.1mol/L的醋酸溶液中不断滴加0.1mol/L的NaOH溶液,溶液的pH变化曲线如图所示,在滴定过程中,下列关于溶液中离子浓度大小关系的描述不正确的是( )| A. | a点时:c(CH3COOH)>c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | |
| B. | b点时:c(Na+)=c(CH3COO-) | |
| C. | c点时:c(OH-)=c(CH3COOH)+c(H+) | |
| D. | d点时:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
3.有如下合成路线,甲经二步转化为丙:
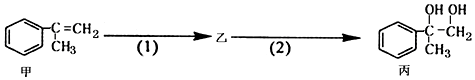
下列叙述错误的是( )
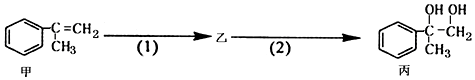
下列叙述错误的是( )
| A. | 物质丙能与氢氧化钠溶液反应 | |
| B. | 甲和丙均可使酸性KMnO4溶液褪色 | |
| C. | 反应(2)属于取代反应 | |
| D. | 步骤(2)产物中可能含有未反应的甲,可用溴水检验是否含甲 |
1.在1.01×105Pa、150℃时,将 ILCH4、2LC2H2、2LC3H6与30LO2混合并点燃,完全反应后,恢复至原来状态,气体的体积是( )
| A. | 35L | B. | 30L | C. | 25L | D. | 20 L |

