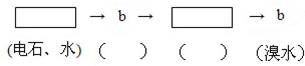题目内容
19.某学生设计氨催化氧化实验,并将制得NO进一步氧化为NO2用水吸收NO2,并检验HNO3的生成.可供选择的固体药品有:NH4Cl、Ca(OH)2、KClO3、MnO2、CaO
可供选择的液体药品有:浓氨水、过氧化氢、浓盐酸、水
可供选择的仪器有:如图
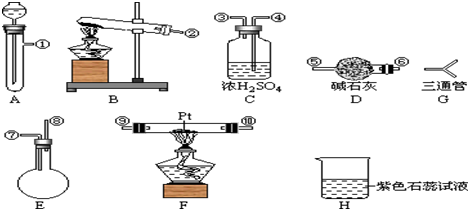
另有铁架台、铁夹、铁圈、乳胶管若干,可供选择.设计实验时,A和B两个制气装置允许使用两次,其余装置只能使用一次.
(1)氨氧化制NO的化学反应为4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,该反应应在装置F中进行.
(2)为快速制NH3和O2,制取NH3的装置最好选择A,其化学反应方程式为NH3•H2O=NH3↑+H2O;制取O2的装置最好选择A,其化学反应方程式为2H2O2 $\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑.
(3)利用快速制NH3和O2的装置组装,各仪器按气流方向连接的正确顺序为
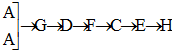 [按装置先后顺序排列]
[按装置先后顺序排列](4)装置C的作用是吸收多余NH3和水蒸气.
(5)装置H中溶液变红,其原因是(用化学方程式表示)4NO2+O2+2H2O=4HNO3.
分析 (1)氨气与氧气在催化剂条件下加热生成一氧化氮和水,依据反应条件和反应物状态选择装置;
(2)要快速制备氨气,则应该是将生石灰加入到浓氨水中,据此选择装置及写出方程式;
双氧水在催化剂条件下,不需要加热就会迅速产生大量氧气,据反应物状态和反应条件选择发生装置并写出方程式;
(3)快速制NH3和O2含有水蒸气,所以需要干燥,用碱石灰进行干燥,然后进入F发生成催化氧化,剩余的氨气需要用浓硫酸吸收,同时还要干燥NO,最后检验硝酸的生成,据此连接仪器;
(4)氨气与浓硫酸反应,可以用浓硫酸吸收过量的氨气和气体中的水蒸气;
(5)由于NO2和剩余的氧气溶于水会有硝酸生成,溶液显酸性,因此石蕊试液变为红色.
解答 解:(1)氨气与氧气在催化剂条件下加热生成一氧化氮和水,化学方程式为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,由于是两种气体之间的反应,所以根据装置的特点可知,应选择装置F制备;
故答案为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;F;
(2)要快速制备氨气,则应该是将生石灰加入到浓氨水中,所以选择的装置是A,反应的化学方程式是NH3•H2O=NH3↑+H2O;
双氧水在催化剂条件下,不需要加热就会迅速产生大量氧气,反应物状态为固体与液体,条件不加热,选择装置A;方程式为:2H2O2 $\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑;
故答案为:A;NH3•H2O=NH3↑+H2O;A;2H2O2 $\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑;
(3)快速制NH3和O2含有水蒸气,所以需要干燥,用碱石灰进行干燥,然后进入F发生成催化氧化,剩余的氨气需要用浓硫酸吸收,同时还要干燥NO,最后检验硝酸的生成,所以正确的连接顺序是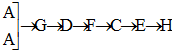 ;
;
故答案为: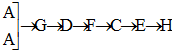 ;
;
(4)C中的浓硫酸用来吸收过来的氨气,干燥气体吸收水蒸气,故答案为:吸收多余NH3和水蒸气;
(5)由于NO2和剩余的氧气溶于水会有硝酸生成,溶液显酸性,因此石蕊试液变为红色,反应的化学方程式是:4NO2+O2+2H2O=4HNO3;
故答案为:4NO2+O2+2H2O=4HNO3.
点评 本题考查气体的制备和性质的检验,熟悉发生装置选择的依据、氨气、氧气的制备原理和性质是解题关键,题目难度中等.

 53随堂测系列答案
53随堂测系列答案I.探究草酸与髙锰酸钾溶液在不同条件下反应的快慢
取4支试管,分别加入0.10mol/L的草酸溶液5mL,按以下表中四种方案分别加人相 应的试剂,使其发生反应.四支试管中均可观察到有气泡产生,且溶液的颜色变化都 为:紫红色→红色→橙红色→橙色→黄色→无色,溶液褪为无色所需的时间如表所 示(表中“一”表示未加入该试剂).
| 实验 编号 | 反应温度 (利用水浴加热) | 稀硫酸 溶液 | MnSO4固体 | 0.10mol/L KMnO4溶液 | 褪色 时间 |
| 1 | 65℃ | ---- | --- | 1mL | 100s |
| 2 | 65℃ | 10滴 | --- | 1mL | 90s |
| 3 | 75℃ | 10滴 | ---- | 1mL | 40s |
| 4 | 75℃ | 10滴 | 加入少许 | 1mL | 3s |
II.测定草酸晶体的纯度
用托盘天平称取草酸晶体(H2C2O4•2H2O)W g;配制成250mL溶液;每次移取25.00mL该溶液于锥形瓶中,用0.10moI/L酸性高锰酸钾溶液滴定;滴定实验重复操 作2~3次.请回答:
(1)实验中需要用到的玻璃仪器除了玻璃棒、烧杯、锥形瓶、胶头滴管、250mL容量瓶 外还需要的一种玻璃仪器是酸式滴定管
(2)上述H2C2O4溶液与酸性KMnO4溶液反应的离子方程为5H2C2O4+2MnO4-+6H+=2Mn2++10CO2↑++8H2O.
(3)若滴定过程中平均消耗酸性髙锰酸钾溶液VmL,则草酸晶体的纯度为$\frac{31.5V}{W}%$(以含W、V的表达式表示).
| A. | Na | B. | Mg | C. | S | D. | Cl |
| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
 为探究乙炔与溴的加成反应,甲同学设计并进行了如下实验:先取一定量工业用电石与水反应,将生成的气体通入溴水中,发现溶液褪色,即证明乙炔与溴水发生了加成反应.
为探究乙炔与溴的加成反应,甲同学设计并进行了如下实验:先取一定量工业用电石与水反应,将生成的气体通入溴水中,发现溶液褪色,即证明乙炔与溴水发生了加成反应.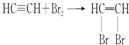
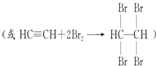 .
.