题目内容
7.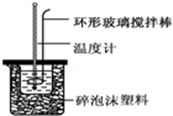 实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液和如图所示装置,进行测定中和热的实验,得到表中的数据:完成下列问题:
实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液和如图所示装置,进行测定中和热的实验,得到表中的数据:完成下列问题:| 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | |
| 盐酸 | NaOH溶液 | ||
| 1 | 20.2 | 20.3 | 23.7 |
| 2 | 20.3 | 20.5 | 23.8 |
| 3 | 21.5 | 21.6 | 24.9 |
(2)在操作正确的前提下,提高中和热测定准确性的关键是提高装置的保温效果.
(3)根据上表中所测数据进行计算,则该实验测得的中和热△H=-56.8kJ/mol[盐酸和NaOH溶液的密度按1g•cm-3计算,反应后混合溶液的比热容(c)按4.18J•(g•℃)-1计算].如用0.5mol/L的盐酸与NaOH固体进行实验,则实验中测得的“中和热”数值将偏大(填“偏大”、“偏小”、“不变”).其理由是氢氧化钠固体溶于水放热.
(4)若某同学利用上述装置做实验,有些操作不规范,造成测得中和热的数值偏低,请你分析可能的原因是ABDF.
A.测量盐酸的温度后,温度计没有用水冲洗干净
B.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓
C.做本实验的当天室温较高
D.将50mL0.55mol/L氢氧化钠溶液取成了50mL0.55mol/L的氨水
E.在量取盐酸时仰视计数
F.大烧杯的盖板中间小孔太大.
分析 (1)金属导热快,热量损失多;
(2)中和热测定实验成败的关键是保温工作;
(3)先求出三次反应的温度差,根据公式Q=cm△T来求出生成0.05mol的水放出热量,最后根据中和热的概念求出反应热;氢氧化钠固体溶于水放热;
(4)根据实验的关键是保温,如果装置有能量散失,则会导致结果偏低,根据实验中用到的试剂以及实验操作知识来判断.
解答 解:(1)不能将环形玻璃搅拌棒改为铜丝搅拌棒,因为铜丝搅拌棒是热的良导体;
故答案为:Cu传热快,热量损失大;
(2)中和热测定实验主要目的是测量反应放出的热量多少,所以提高中和热测定准确性的关键是提高装置的保温效果;
故答案为:提高装置的保温效果;
(3)第1次实验盐酸和NaOH溶液起始平均温度为20.25℃,反应前后温度差为:3.45℃;
第2次实验盐酸和NaOH溶液起始平均温度为20.40℃,反应前后温度差为:3.40℃;
第3次实验盐酸和NaOH溶液起始平均温度为21.55℃,反应前后温度差为:3.35℃;
三组数据均有效,其平均值为3.40℃;
50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液的质量和m=100mL×1g/mL=100g,c=4.18J/(g•℃),代入公式Q=cm△T得生成0.025mol的水放出热量Q=4.18J/(g•℃)×100g×3.40℃;=1421.2J=1.4212KJ,即生成0.025mol的水放出热量1.4212KJ,所以生成1mol的水放出热量为$\frac{1.4212KJ×1mol}{0.025mol}$=56.8kJ,即该实验测得的中和热△H=-56.8kJ/mol;氢氧化钠固体溶于水放热,所以实验中测得的中和热数值将偏大;
故答案为:-56.8 kJ/mol;偏大;氢氧化钠固体溶于水放热;
(4)A.测量盐酸的温度后,温度计没有用水冲洗干净,在测碱的温度时,会发生酸和碱的中和,温度偏高,则温度差减小,实验测得中和热的数值偏小,故A正确;
B、把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓,会导致一部分能量的散失,实验测得中和热的数值偏小,故B正确;
C、做本实验的室温和反应热的数据之间无关,故C错误;
D、将50mL0.55mol/L氢氧化钠溶液取成了50mL0.55mol/L的氨水,由于氨水是弱碱,电离是吸热过程,实验测得中和热的数值偏小,故D正确;
E、在量取盐酸时仰视计数,会使得实际量取体积高于所要量的体积,算过量,可以保证碱全反应,会使得中和和热的测定数据偏高,故E错误;
F、大烧杯的盖板中间小孔太大,会导致一部分能量散失,所以测的数值降低,故F正确.
故答案为:ABDF.
点评 本题主要考查热中和热概念、测定原理及反应热的计算,题目难度中等,注意理解中和热的概念以及测定反应热的误差等问题.

| A. | Na+、I-、CO${\;}_{3}^{2-}$、ClO- | B. | Fe2+、H+、K+、NO${\;}_{3}^{-}$ | ||
| C. | Ba2+、Na+、SCN-、Cl- | D. | Cu2+、Fe2+、Cl-、NO${\;}_{3}^{-}$ |
| 物质 | 氯化铜 | 氧化亚铜 | 氢氧化亚铜 (不稳定) | 氯化亚铜 |
| 颜色 | 固体呈棕色,浓溶液呈绿色,稀溶液呈蓝色 | 红色 | 橙黄色 | 白色 |
| A. | 电解过程中氯离子向阳极移动 | B. | 电解开始时阳极Cu 放电生成Cu2+ | ||
| C. | 阴极反应为2H2O+2e-=H2↑+2OH- | D. | 随溶液pH升高CuCl逐渐转化为CuOH |
| A. | CH3-CH═CH2与  | B. |  与 与 | ||
| C. | HCOOC2H5与CH3COOCH3 | D. |  与 与 |
| A. | 甲苯与溴水 | B. | 乙酸钠溶液与硫酸 | ||
| C. | 甲苯与KMnO4酸性溶液 | D. | 甲酸溶液与银氨溶液水浴共热 |
实验名称:卤素单质的氧化性强弱比较
| 实验步骤 | 实验结论 氧化性从强到弱的顺序:氯、溴、碘 |
| ①氯水+1mL CCl4,振荡,静置,观察四氯化碳层颜色 | |
| ②NaBr溶液+氯水+1mL CCl4,振荡,静置,观察四氯化碳层颜色 | |
| ③KI溶液+氯水+1mL CCl4,振荡,静置,观察四氯化碳层颜色 |
实验设计如下,请回答:
(1)完成该实验需用到的实验仪器是试管、胶头滴管.
(2)②中反应的化学方程式为2NaBr+Cl2═2NaCl+Br2.
③中反应的离子方程式为Cl2+2I-═2Cl-+I2.
(3)CCl4在实验中所起的作用是萃取剂.
(4)该同学的实验设计不足之处是没有比较Br2和I2的氧化性强弱,改进的办法是将溴水滴在KI淀粉试纸上,观察试纸是否变蓝色(或KI溶液+溴水+1 mL CCl4,振荡,静置,观察四氯化碳层颜色).
| A. | 只具有氧化性 | B. | 只具有还原性 | ||
| C. | 既具有氧化性又具有还原性 | D. | 既无氧化性又无还原性 |