题目内容
13.下列说法不正确的是( )| A. | 聚合物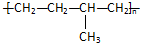 可由单体CH3CH=CH2和CH2=CH2加聚制得 可由单体CH3CH=CH2和CH2=CH2加聚制得 | |
| B. | 1 molCH3COOH与1mol CH3CH2OH在浓硫酸共热下生成的乙酸乙酯分子数为NA | |
| C. | 乙醇、苯酚、乙酸都有羟基,但是羟基上的H活泼性不同,主要是基团之间相互影响造成的 | |
| D. | 等物质的量的乙炔和乙醛分别充分燃烧,所耗用氧气的量相同 |
分析 A.聚合度的主链只有C,为加聚产物;
B.酯化反应为可逆反应;
C.均含-OH,连接基团不同;
D.乙炔为C2H2,乙醛为C2H2.H2O,C2H2消耗氧气相同,H2O不消耗氧气.
解答 解:A.聚合度的主链只有C,为加聚产物,由添键断键法可知,单体为CH3CH=CH2和CH2=CH2,故A正确;
B.酯化反应为可逆反应,则1 molCH3COOH与1mol CH3CH2OH在浓硫酸共热下生成的乙酸乙酯分子数小于NA,故B错误;
C.均含-OH,连接基团不同,则基团之间相互影响,导致羟基上的H活泼性不同,故C正确;
D.乙炔为C2H2,乙醛为C2H2.H2O,C2H2消耗氧气相同,H2O不消耗氧气,则等物质的量的乙炔和乙醛分别充分燃烧,所耗用氧气的量相同,故D正确;
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握有机物的官能团、有机反应为解答的关键,侧重分析与应用能力的考查,注意选项B为易错点,题目难度不大.

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
3.下列变化属于吸热反应的是( )
①水蒸气液化 ②将胆矾加热变为白色粉末 ③浓硫酸稀释④氯酸钾分解制氧气 ⑤生石灰与水反应生成熟石灰.
①水蒸气液化 ②将胆矾加热变为白色粉末 ③浓硫酸稀释④氯酸钾分解制氧气 ⑤生石灰与水反应生成熟石灰.
| A. | ①④ | B. | ②③ | C. | ①④⑤ | D. | ②④ |
4. 在狗年里,人们相互祝愿亲朋好友:狗年旺旺,狗年大发.图是一种形状酷似一条小狗的有机物键线式结构图,化学家将其取名为“doggycene”,下列有关“doggycene”的说法中正确的是( )
在狗年里,人们相互祝愿亲朋好友:狗年旺旺,狗年大发.图是一种形状酷似一条小狗的有机物键线式结构图,化学家将其取名为“doggycene”,下列有关“doggycene”的说法中正确的是( )
 在狗年里,人们相互祝愿亲朋好友:狗年旺旺,狗年大发.图是一种形状酷似一条小狗的有机物键线式结构图,化学家将其取名为“doggycene”,下列有关“doggycene”的说法中正确的是( )
在狗年里,人们相互祝愿亲朋好友:狗年旺旺,狗年大发.图是一种形状酷似一条小狗的有机物键线式结构图,化学家将其取名为“doggycene”,下列有关“doggycene”的说法中正确的是( )| A. | 该分子中所有碳原子不可能处于同一平面 | |
| B. | “doggycene”的分子式为C26H30 | |
| C. | 该物质在常温下呈气态 | |
| D. | 1 mol该物质在氧气中完全燃烧生成CO2和H2O的物质的量之比为1:1 |
1.下列变化中属于物理变化的是( )
| A. | 湿法炼铜 | B. | 用黏土烧制陶瓷 | C. | 钠灯发光 | D. | 钟乳石的形成 |
8.实验室里坩埚的材质种类很多,可以用于熔融烧碱的坩埚是( )
| A. | 氧化铝刚玉坩埚 | B. | 铁坩埚 | C. | 石英坩埚 | D. | 陶瓷坩埚 |
18.下列对实验现象的描述与实际事实不一致的是( )
| A. | 向含少量Br2的CCl4中加NaOH溶液,充分振荡,上下两层均为无色 | |
| B. | 向pH试纸上滴加氯水,先变红后变白 | |
| C. | 将红热的铜丝伸入到盛有氯气的集气瓶中,产生蓝绿色的烟 | |
| D. | 往氯水中加入NaHCO3固体,有气体产生 |
2.判断溶液为中性的依据是( )
| A. | c(OH-)=1×10-7mol/L | B. | c(H+)=1×10-7mol/L | ||
| C. | c(OH-)=c(H+) | D. | pH=7 |
2.下列有关溶液组成的描述合理的是( )
| A. | 弱碱性溶液中可能大量存在Na+、K+、Cl-、HCO3- | |
| B. | 滴加石蕊呈红色的溶液可能大量存在K+、NH4+、Cl-、S2- | |
| C. | 与Al反应能放出H2的溶液中可能大量存在:Fe2+、K+、NO3-、SO42- | |
| D. | 漂白粉的水溶液可能大量存在Fe2+、Cl-、Ca2+、Na+ |