题目内容
4. 在狗年里,人们相互祝愿亲朋好友:狗年旺旺,狗年大发.图是一种形状酷似一条小狗的有机物键线式结构图,化学家将其取名为“doggycene”,下列有关“doggycene”的说法中正确的是( )
在狗年里,人们相互祝愿亲朋好友:狗年旺旺,狗年大发.图是一种形状酷似一条小狗的有机物键线式结构图,化学家将其取名为“doggycene”,下列有关“doggycene”的说法中正确的是( )| A. | 该分子中所有碳原子不可能处于同一平面 | |
| B. | “doggycene”的分子式为C26H30 | |
| C. | 该物质在常温下呈气态 | |
| D. | 1 mol该物质在氧气中完全燃烧生成CO2和H2O的物质的量之比为1:1 |
分析 该有机物为稠环物质,相对分子质量较大,常温下为固体,根据结构简式判断分子式,可根据分子式判断完全燃烧生成CO2和水的物质的量,以此解答该题.
解答 解:A.有机物具有稠环结构,具有苯的结构特点,则碳原子可能在同一个平面上,故A错误;
B.有机物的化学式应为:C26H26,故B错误;
C.有机物碳原子数远大于4,常温下不是气体,故C错误;
D.有机物中的碳全部转化为二氧化碳,氢全部转化为水,所以1molC26H26在氧气中完全燃烧生成CO2和水的物质的量之比为26:13=2:1,故D正确.
故选D.
点评 本题考查有机物的结构和性质,为高频考点,题目难度中等,注意分析该有机物的结构特点,把握有机物的结构特点,注意根据有机物结构简式判断分子式为解答该题的关键.

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案
相关题目
14.下列各组物质所含原子数目一定相同的是( )
| A. | 10g H2O和10g NH3 | |
| B. | 0.1mol CO和标准状况下2.24L Cl2 | |
| C. | 22g CO2和标准状况下11.2 L N2 | |
| D. | 标准状况下11.2 L O2和11.2 L NH3 |
19.误食NaNO2会导致血红蛋白中的Fe2+氧化为Fe3+而中毒,服用维生素C可以解除NaNO2引起的中毒.下列关于上述中毒、解毒过程的说法中正确的是( )
| A. | NaNO2是还原剂 | |
| B. | 维生素C的还原性强于Fe2+ | |
| C. | 1×10-3molFe2+被NaNO2氧化为Fe3+时得到1×10-3mol电子 | |
| D. | 解毒过程中维生素C被还原 |
9.相同温度下,相同物质的量浓度的下列溶质:①NaOH、②NH4Cl、③Na2SO4、④NaHSO4、⑤NH3•H2O,按 c(OH-)由大到小顺序排列正确的是( )
| A. | ⑤①③②④ | B. | ④②③①⑤ | C. | ①⑤③②④ | D. | ①⑤③④② |
16.鲨鱼体内含有的角鲨烯具有抗癌性.实验测得角鲨烯分子是链状结构,分子中含有30个碳原子且碳氢质量比为7.2:1,下列说法不正确的是( )
| A. | 角鲨烯分子式为C30H50 | |
| B. | 角鲨烯可以被酸性KMnO4溶液所氧化 | |
| C. | 1mol角鲨烯最多可与6molH2发生加成反应 | |
| D. | 汽油经过催化裂化可以获得角鲨烯 |
13.下列说法不正确的是( )
| A. | 聚合物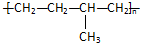 可由单体CH3CH=CH2和CH2=CH2加聚制得 可由单体CH3CH=CH2和CH2=CH2加聚制得 | |
| B. | 1 molCH3COOH与1mol CH3CH2OH在浓硫酸共热下生成的乙酸乙酯分子数为NA | |
| C. | 乙醇、苯酚、乙酸都有羟基,但是羟基上的H活泼性不同,主要是基团之间相互影响造成的 | |
| D. | 等物质的量的乙炔和乙醛分别充分燃烧,所耗用氧气的量相同 |
14.在标有“20℃,25mL”的滴定管内装酸液至刻度“0”时,管内液体的体积( )
| A. | 大于25mL | B. | 等于25mL | C. | 小于25mL | D. | 无法判断 |
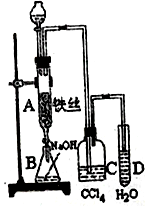 某学生在如图所示的装置中用苯和液溴制取溴苯,请根据下列实验步骤回答有关问题.
某学生在如图所示的装置中用苯和液溴制取溴苯,请根据下列实验步骤回答有关问题. ;
;