题目内容
16.下列离子反应方程式,书写正确的是( )| A. | 向碳酸钠溶液中加醋酸 CO32-+2H+═H2O+CO2↑ | |
| B. | 向稀硫酸溶液中投入铁粉 2Fe+6H+═2Fe3++3H2↑ | |
| C. | 向盐酸中投入碳酸钙 CO32-+2H+═H2O+CO2↑ | |
| D. | 硫酸氢钠溶液中加入氢氧化钡溶液至中性:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O |
分析 A.醋酸为弱酸,离子方程式中醋酸不能拆开;
B.铁与稀硫酸反应生成硫酸亚铁和氢气;
C.碳酸钙难溶物,离子方程式中碳酸钙才能拆开;
D.反应后溶液为中性,则硫酸氢钠与氢氧化钡按照物质的量2:1反应.
解答 解:A.向碳酸钠溶液中加醋酸,醋酸分子需要保留分子式,正确的离子方程式为:CO32-+2CH3COOH═H2O+CO2↑+2CH3COO-,故A错误;
B.向稀硫酸溶液中投入铁粉,反应生成硫酸亚铁和氢气,正确的离子方程式为:2Fe+6H+═2Fe3++3H2↑,故B错误;
C.碳酸钙与盐酸反应生成氯化钙、二氧化碳气体和水,正确的离子方程式为:CaCO3+2H+=Ca2++H2O+CO2↑,故C错误;
D.硫酸氢钠溶液中加入氢氧化钡溶液至中性,反应的离子方程式为:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O,故D正确;
故选D.
点评 本题考查了离子方程式的正误判断,为高考的高频题,属于中等难度的试题,注意掌握离子方程式正误判断常用方法:检查反应能否发生,检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等;试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案
相关题目
6.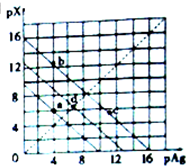 某温度时,卤化银(AgX,X=Cl,Br,I)的3条沉淀溶解平衡曲线如图所示,AgCl,AgBr,AgI的Ksp依次减小.已知pAg=-lgc(Ag+),pX=-lgc(X-),下列说法错误的是( )
某温度时,卤化银(AgX,X=Cl,Br,I)的3条沉淀溶解平衡曲线如图所示,AgCl,AgBr,AgI的Ksp依次减小.已知pAg=-lgc(Ag+),pX=-lgc(X-),下列说法错误的是( )
 某温度时,卤化银(AgX,X=Cl,Br,I)的3条沉淀溶解平衡曲线如图所示,AgCl,AgBr,AgI的Ksp依次减小.已知pAg=-lgc(Ag+),pX=-lgc(X-),下列说法错误的是( )
某温度时,卤化银(AgX,X=Cl,Br,I)的3条沉淀溶解平衡曲线如图所示,AgCl,AgBr,AgI的Ksp依次减小.已知pAg=-lgc(Ag+),pX=-lgc(X-),下列说法错误的是( )| A. | 由a点可知该温度下Ksp(AgCl)=l0-10 | |
| B. | 加入AgNO3可使溶液由b点变到c点 | |
| C. | d点是在水中加入足量的AgBr形成的饱和溶液 | |
| D. | 坐标点(14,8)形成的溶液是AgI的不饱和溶液 |
7.在一个盛有催化剂容积可变的密闭容器中,保持一定的温度和压强,进行以下反应:N2+3H2?2NH3.已知加入1molN2和4molH2时,达到平衡后生成amolNH3.有恒温恒压下欲保持平衡时各组分的体积分数不变.填表(恒温恒压)
| 已知 编号 | 起始状态物质的量/mol | 平衡时NH3的 物质的量/mol | ||
| N2 | H2 | NH3 | ||
| 1 | 4 | 0 | a | |
| ① | 1.5 | 9 | 0 | >1.5a |
| ② | 0 | 0.5 | 1 | 0.5a |
| ③ | m | g(g≥4m) | 0 | am或者$\frac{ag}{4}$ |
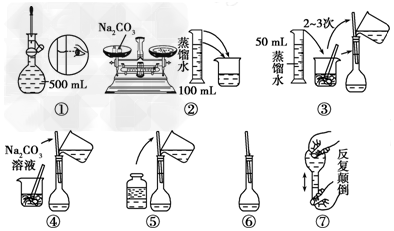
11.(1)若某药品质量约为32.0g,托盘天平准确称其质量,若用↓表示在右盘放上砝码,用↑表示将砝码取下,在下列表格的空格内,用↓和↑表示相应砝码的放上或取下.
(2)配制500mL 0.1mol•L-1 Na2CO3溶液,图中操作②中应该填写的数据为5.3,实验操作的先后顺序为②④③⑤①⑥ (填编号).
(3)在配制一定物质的量浓度的溶液时,用“偏高、偏低、无影响”表示下列操作对所配溶液浓度的影响.
①用量筒取液态溶质,读数时,俯视量筒,所配制溶液的浓度偏低
②将量取液态溶质的量筒用水洗涤,洗涤液倒入容量瓶,所配制溶液的浓度偏高
③定容摇匀后,有少量溶液外流,对所配制溶液的浓度无影响.
| 50g | 20g | 20g | 10g | 5g |

(3)在配制一定物质的量浓度的溶液时,用“偏高、偏低、无影响”表示下列操作对所配溶液浓度的影响.
①用量筒取液态溶质,读数时,俯视量筒,所配制溶液的浓度偏低
②将量取液态溶质的量筒用水洗涤,洗涤液倒入容量瓶,所配制溶液的浓度偏高
③定容摇匀后,有少量溶液外流,对所配制溶液的浓度无影响.
1.下列有关物质应用的说法不正确的是( )
| A. | 氧化铁可用来制造红色油漆和涂料 | |
| B. | 生铁、普通钢和不锈钢中的含碳量依次减小 | |
| C. | 硅胶可用作实验室和袋装食品、瓶装药品等的干燥剂 | |
| D. | 硅是生产光纤制品的基本原料 |
8.相同温度下,体积相同的两个容器中,充入等质量CO2和CO气体,下列判断正确的是( )
| A. | CO2和CO对容器产生的压强之比是7:11 | |
| B. | CO2和CO的密度之比是11:7 | |
| C. | CO2和CO的分子数相等 | |
| D. | CO2和CO的氧原子个数比是22:7 |
5.下列各组物质之间的化学反应,反应产物一定为纯净物的是( )
| A. | CH3-CH=CH-CH3+Br2$→_{△}^{催化剂}$ | |
| B. | CH2=CH-CH2CH3+HCl | |
| C. | CH3-CH=CH2+H2O $→_{加热、加压}^{催化剂}$ | |
| D. | CH3CH3+Cl2$\stackrel{光照}{→}$ |