��Ŀ����
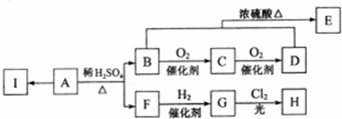
10��A��F�����л�������ͼ��ʾ��ת����ϵ�����ַ�Ӧ�����Ͳ�������ȥ����֪��C��FeCl3��Һ��������ɫ��B��E����Է���������ȣ�C�����ϵ�һ�ȴ��������֣�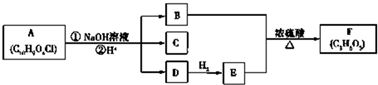
��ʾ��
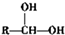 $\stackrel{�Զ���ˮ}{��}$
$\stackrel{�Զ���ˮ}{��}$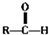 ��RΪ�ǻ���
��RΪ�ǻ�����1��д���������ʵĽṹ��ʽ��BHCOOH��C
 ��
����2��A�еĹ����ŵ���������������ԭ�ӣ�1molA ������NaOH��Һ�г�ַ�Ӧ���������NaOH�����ʵ���Ϊ4mol��
��3�������й�B��D��˵������ȷ����abcd������ĸ����
a������������Cu��OH��2��Ӧb������NaHCO3��Һ�������
c���˴Ź��������϶���2�����շ�d������ʹ���Ը��������Һ��ɫ
��4��д��B��E��Ӧ�Ļ�ѧ����ʽ��
 ��
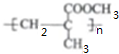
����5��F��ͬ���칹��G���������ص㣺���ܷ���������Ӧ���ڲ���������G�Ľṹ��ʽΪ
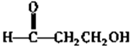 ��
��
���� ��B��E��Ũ������������·���������Ӧ����F����B��E����Է���������ȣ���BΪHCOOH��EΪCH3CH2OH��FΪHCOOCH2CH3��D�������ӳ�����E����DΪCH3CHO��A������������Һ�з���ˮ�����ữ�õ�B��C��D����C��FeCl3��Һ��������ɫ�����з��ǻ�����C�����ϵ�һ�ȴ��������֣�����Ϊ�Գƽṹ����CΪ ��AΪ
��AΪ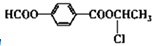 ���ݴ˷������
���ݴ˷������
��� �⣺��B��E��Ũ������������·���������Ӧ����F����B��E����Է���������ȣ���BΪHCOOH��EΪCH3CH2OH��FΪHCOOCH2CH3��D�������ӳ�����E����DΪCH3CHO��A������������Һ�з���ˮ�����ữ�õ�B��C��D����C��FeCl3��Һ��������ɫ�����з��ǻ�����C�����ϵ�һ�ȴ��������֣�����Ϊ�Գƽṹ����CΪ ��AΪ
��AΪ ��
��
��1���������Ϸ�����BΪHCOOH��CΪ ���ʴ�Ϊ��HCOOH��
���ʴ�Ϊ��HCOOH�� ��
��
��2���������Ϸ�����AΪ �������ŵ���������������ԭ�ӣ�����A�к���1��������1��������1����ԭ�ӣ�1����������2��NaOH������1molA ������NaOH��Һ�г�ַ�Ӧ���������NaOH�����ʵ���Ϊ4mol���ʴ�Ϊ����������ԭ�ӣ�4��
�������ŵ���������������ԭ�ӣ�����A�к���1��������1��������1����ԭ�ӣ�1����������2��NaOH������1molA ������NaOH��Һ�г�ַ�Ӧ���������NaOH�����ʵ���Ϊ4mol���ʴ�Ϊ����������ԭ�ӣ�4��
��3���������Ϸ�����BΪHCOOH��DΪCH3CHO��
a���������Ϸ�����BΪHCOOH��DΪCH3CHO��������ȩ�������Ծ���������Cu��OH��2��Ӧ������ȷ��
b���������Ϸ�����BΪHCOOH����NaHCO3��Һ��Ӧ�������ݡ�DΪCH3CHO����NaHCO3��Һ��Ӧ�����Կ���NaHCO3��Һ������ߣ�����ȷ��
c���������Ϸ�����BΪHCOOH��DΪCH3CHO���˴Ź��������϶���2�����շ壬����ȷ��
d���������Ϸ�����BΪHCOOH��DΪCH3CHO��������ȩ��������ʹ���Ը��������Һ��ɫ������ȷ��
��ѡ��abcd��
��4��B��E��Ũ������������·���������Ӧ����F����B��E��Ӧ�Ļ�ѧ����ʽΪ ��
��
�ʴ�Ϊ�� ��
��
��5��FΪHCOOCH2CH3��ͬ���칹��G���������ص㣺���ܷ���������Ӧ������ȩ�����ڲ�����������һ����ԭ��ֻ�����ǻ�����ʽ����ĩ�˵�̼�ϣ�����G�Ľṹ��ʽΪ 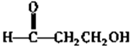 ���ʴ�Ϊ��
���ʴ�Ϊ��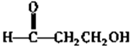 ��
��
���� ���⿼���л�����ƶϣ�Ϊ�߿��������ͣ������ڿ���ѧ�������������ƶ��������ۺ����û�ѧ֪ʶ����������Ŀ�Ѷ��еȣ�ע����������Ϣ��Ϊ������Ĺؼ���

| A�� | ��ˮʹʪ��ĺ�ɫʯ����ֽ������NH3•H2O?NH4++OH- | |
| B�� | ��ҵ���ù�����NaOH��Һ���գ�SO2��SO2+OH-=HSO3- | |
| C�� | ���ռ���Һ��ϴ�����������Ĥ��2OH-+Al2O3=2AlO2-+H2O | |
| D�� | ��ʯ��������й¶��������Ca��OH��2+Cl2=Ca2++Cl-+ClO-+H2O |
| A�� | �ñ����������Һ���������� | |
| B�� | ����ʯ�Ҹ��ﰱ�� | |
| C�� | �����Ƶ�����ʢװŨ���� | |
| D�� | �ñ���̼������Һ�ռ�ʵ������ȡ���������� |
��1����������ӡˢ��·���ϵ�ͭ�Ʊ�CuCl2��
ʵ����ģ����չ������£�

��֪�������ʿ�ʼ�����ͳ�����ȫʱ��pH���±���
| ���� | ��ʼ���� | ������ȫ |
| Fe��OH��2 | 7.6 | 9.6 |
| Fe��OH��3 | 2.7 | 3.7 |
| Cu��OH��2 | 4.4 | 8.0 |
�ٲ����IJ��������ǹ��ˣ�
�������Լ��У�������Ϊ�Լ�a����C��
A��HNO3��Һ B��Fe2��SO4��3��Һ C��FeCl3��Һ
���������Լ�b��ֱ�Ӽ����Լ�c������ҺpH���Ƿ���У�����ǡ����������Dz��ܳ�ȥFe2+��Ӱ������CuCl2���ȣ�
��2����H2O2�����Ṳͬ����ӡˢ��·���Ʊ�����ͭ��
��֪��2H2O2��l��=2H2O ��l��+O2��g����H1=-196kJ/mol
H2O��l��=H2��g��+1/2O2��g����H2=+286kJ/mol
Cu��s��+H2SO4��aq��=CuSO4��aq��+H2��g����H3=+64kJ/mol
��Cu��s��+H2O2��l��+H2SO4��aq��=CuSO4��aq��+2H2O��l����H=-320KJ/mol��
��3������ӦCu+H2O2+H2SO4=CuSO4+2H2O��Ƴ�ԭ��أ��������缫��Ӧʽ��H2O2+2H++2e-=2H2O��
��4��������������Ṳͬ����ӡˢ��·���Ʊ�����ͭ������ӡˢ��·���������ɷֲ����ᷴӦ������ȡ3mol����������ͭ����Ҫ0.5mol/L��������Һ�������4L��
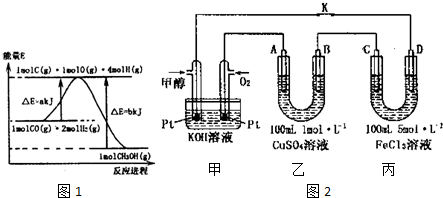
��1���ϳɼ״��ķ�Ӧ���������������仯��ͼ1��ʾ��д���ϳɼ״����Ȼ�ѧ����ʽCO��g��+2H2��g��?CH3OH��g����H=-��b-a��kJ/mol��
��2��ʵ������lL�ܱ������н���ģ��ϳ�ʵ�飮��1molCO��2molH2ͨ�������У��ֱ������300���500�淴Ӧ��ÿ��һ��ʱ���������м״���Ũ�����£����������ݵ�λ��mol•L-l��
| �¶�\ʱ�� | 10min | 20min | 30min | 40min | 50min | 60min |
| 300�� | 0.40 | 0.60 | 0.75 | 0.84 | 0.90 | 0.90 |
| 500�� | 0.60 | 0.75 | 0.78 | 0.80 | 0.80 | 0.80 |
��500��ʱƽ�ⳣ��K����ֵΪ25��
��300��ʱ�����������ݻ�ѹ����ԭ����$\frac{1}{2}$���������������������£���ƽ����ϵ������Ӱ����cd��ѡ���ţ���
a��c��H2����С
b������Ӧ���ʼӿ죬�淴Ӧ���ʼ���
c��CH3OH�����ʵ�������
d������ƽ��ʱ$\frac{c��{H}_{2}��}{c��C{H}_{3}OH��}$��С
��3����ͼ2�Ǽ״�ȼ�ϵ�ع�����ʾ��ͼ������A��B��D��Ϊʯī�缫��CΪͭ�缫������һ��ʱ��Ͽ�K����ʱA��B�����ϲ��������������ͬ��
�ټ��и����ĵ缫��ӦʽΪCH3OH-6e-+8OH-=CO32-+6H2O��
������A�������������ڱ�״���µ����Ϊ2.24l��
�۷�Ӧ������Ҫʹ��װ���н���������ǡ����ȫ��������Ҫ300mL5.0mol•L-lNaOH ��Һ��
| Ԫ�ر�� | �� | �� | �� | �� | �� | �� | �� | �� |
| ԭ�Ӱ뾶/nm | 0.037 | 0.074 | 0.082 | 0.099 | 0.102 | 0.143 | 0.152 | 0.186 |
| ����ϼۻ� ��ͻ��ϼ� | +1 | -2 | +3 | -1 | -2 | +3 | +1 | +1 |
| A�� | Ԫ�آڢ��γɵĻ������������ | |
| B�� | Ԫ�آ���̬�⻯��ķе�С��Ԫ�آ���̬�⻯��ķе� | |
| C�� | Ԫ�آݶ�Ӧ�����Ӱ뾶����Ԫ�آ߶�Ӧ�����Ӱ뾶 | |
| D�� | Ԫ�آܵ�����������ˮ�����Ԫ�آݵ�����������ˮ��������ǿ |
| A�� | ����������PM10�� | B�� | NO2Ũ�� | ||
| C�� | SO2Ũ�� | D�� | CO2Ũ�� |

 ��
��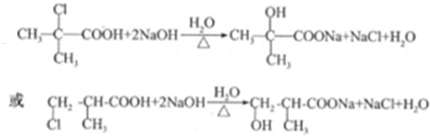 ����дһ����
����дһ����