题目内容
已知FeCl3和MnO2都可做H2O2分解制O2反应的催化剂,为了探究温度对该反应速率的影响,下列实验方案可行的是( )
A、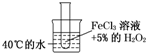 |
B、 |
C、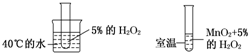 |
D、 |
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:探究温度对该反应速率的影响,一定要将其他影响化学反应速率的因素控制为相等的情况下才能进行实验,得出结论.
解答:
解:A、不能形成对比试验,无法探究温度对该反应速率的影响,故A错误;
B、温度和催化剂都不一样的情况下,探究温度对该双氧水的分解反应速率的影响,故B错误;
C、第一个装置中缺少催化剂二氧化锰,无法探究温度对该反应速率的影响,故C错误;、
D、催化剂是一样的,都是氯化铁,温度不同,这样可以探究温度对该反应速率的影响,故D正确.
故选D.
B、温度和催化剂都不一样的情况下,探究温度对该双氧水的分解反应速率的影响,故B错误;
C、第一个装置中缺少催化剂二氧化锰,无法探究温度对该反应速率的影响,故C错误;、
D、催化剂是一样的,都是氯化铁,温度不同,这样可以探究温度对该反应速率的影响,故D正确.
故选D.
点评:本题主要考查了影响化学反应的因素,解答这类题时注意控制变量法实验的应用,利用相关的化学反应原理进行分析解答,难度中等.

练习册系列答案
相关题目
已知:Fe2O3(s)+C(s)═CO2(g)+2Fe(s)△H=+234.1kJ?mol-1
C(s)+O2(g)=CO2(g)△H=-393.5kJ?mol-1
则2Fe(s)+O2(g)═Fe2O3(s)的△H是( )
C(s)+O2(g)=CO2(g)△H=-393.5kJ?mol-1
则2Fe(s)+O2(g)═Fe2O3(s)的△H是( )
| A、-824.4 kJ?mol-1 |
| B、-627.6kJ?mol-1 |
| C、-744.7kJ?mol-1 |
| D、-168.4kJ?mol-1 |
下列递变不正确的是( )
| A、Na、Mg、Al最外层电子数依次增多,其单质的还原性依次减弱 |
| B、P、S、Cl最高正价依次升高,对应气态氢化物稳定性增强 |
| C、C、N、O原子半径依次增大 |
| D、Na、K、Rb氧化物的水化物碱性依次增强 |
下列关于燃烧热的描述中正确的是( )
| A、已知a g乙烯气体充分燃烧时生成1mol CO2和液态水,放出b kJ的热量,则表示乙烯燃烧热的热化学方程式为2C2H4(g)+6O2(g)═4CO2(g)+4H2O(l)△H=-4b kJ?mol-1 | ||
B、将甲醇蒸气转化为氢气的热化学方程式是CH3OH(g)+
| ||
| C、H2(g)的燃烧热是285.8 kJ?mol-1,则2H2O(g)═2H2(g)+O2(g)△H=+571.6 kJ?mol-1 | ||
D、葡萄糖的燃烧热是2800 kJ?mol-1,则
|
相同质量的下列各烃,完全燃烧后生成水最多的是( )
| A、甲烷 | B、乙烷 | C、乙烯 | D、乙炔 |
四个不同容器在不同条件下进行N2(g)+3H2(g)?2NH3(g)反应,根据下列在相同时间内测定的结果判断,生成氨的速率最快的是( )
| A、用H2表示的反应速率为0.1 mol?L-1?min-1 |
| B、用N2表示的反应速率为0.04 mol?L-1?s-1 |
| C、用N2表示的反应速率为0.2 mol?L-1?s-1 |
| D、用NH3表示的反应速率为0.3 mol?L-1?s-1 |
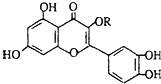 天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂.关于维生素P 的叙述错误的是( )
天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂.关于维生素P 的叙述错误的是( )| A、可以和溴水反应 |
| B、可用有机溶剂萃取 |
| C、分子中有二个苯环 |
| D、1mol维生素P可以和3molNaOH反应 |
下列说法正确的是( )
| A、任何条件下,纯水的pH都是7 |
| B、95℃纯水中c(H+)<10-7 mol?L-1 |
| C、95℃纯水的pH大于7 |
| D、任何条件下,纯水都显中性 |