题目内容
下列关于燃烧热的描述中正确的是( )
| A、已知a g乙烯气体充分燃烧时生成1mol CO2和液态水,放出b kJ的热量,则表示乙烯燃烧热的热化学方程式为2C2H4(g)+6O2(g)═4CO2(g)+4H2O(l)△H=-4b kJ?mol-1 | ||
B、将甲醇蒸气转化为氢气的热化学方程式是CH3OH(g)+
| ||
| C、H2(g)的燃烧热是285.8 kJ?mol-1,则2H2O(g)═2H2(g)+O2(g)△H=+571.6 kJ?mol-1 | ||
D、葡萄糖的燃烧热是2800 kJ?mol-1,则
|
考点:燃烧热
专题:化学反应中的能量变化
分析:根据燃烧热的概念:指1mol可燃物完全燃烧生成稳定的化合物时所放出的热量,反应物中C→CO2(气),H→H2O(液),S→SO2(气)等来回答判断.
解答:
解:A、ag乙烯气体充分燃烧时生成1mol CO2和液态水,放出b kJ的热量,则表示乙烯燃烧热的热化学方程式为2C2H4(g)+6O2(g)═4CO2(g)+4H2O(l)△H=-
kJ?mol-1,故A错误;
B、反应CH3OH(g)+
O2(g)═CO2(g)+2H2(g)的△H=-192.9 kJ?mol-1,CH3OH(g)的燃烧热应该是1mol甲醇燃烧生成二氧化碳气体和液态水所放出的热量,不能是生成氢气,故B错误;
C、H2(g)的燃烧热是285.8 kJ?mol-1,即2H2(g)+O2(g)=2H2O(l),△H=-571.6 kJ?mol-1,所以2H2O(l)═2H2(g)+O2(g)△H=+571.6 kJ?mol-1,故C错误;
D、葡萄糖的燃烧热是2800 kJ?mol-1,即1mol葡萄糖完全燃烧生成二氧化碳气体和液态水时所放出的热量是1400kJ,即
C6H12O6(s)+3O2(g)═3CO2(g)+3H2O(l)△H=-1400kJ?mol-1,故D正确.
故选D.
| 56b |
| a |
B、反应CH3OH(g)+
| 1 |
| 2 |
C、H2(g)的燃烧热是285.8 kJ?mol-1,即2H2(g)+O2(g)=2H2O(l),△H=-571.6 kJ?mol-1,所以2H2O(l)═2H2(g)+O2(g)△H=+571.6 kJ?mol-1,故C错误;
D、葡萄糖的燃烧热是2800 kJ?mol-1,即1mol葡萄糖完全燃烧生成二氧化碳气体和液态水时所放出的热量是1400kJ,即
| 1 |
| 2 |
故选D.
点评:考查反应热的计算燃烧热、热化学方程式书写与理解,注意知识的归纳和整理是关键,难度不大.

练习册系列答案
相关题目
实验室中的药品常按物质的性质、类别等有规律地摆放.现有部分药品按某种规律摆放在实验桌上,如图.做“硫酸的性质”的实验时,某同学取用Ba(OH)2溶液后,应把它放回的位置是( )


| A、A | B、B | C、C | D、D |
下列说法正确的是( )
| A、金属原子失电子越多,其还原性越强 |
| B、CH4的摩尔质量为16g |
| C、10mL质量分数为98%的H2SO4,用水稀释至100mL,H2SO4的质量分数为9.8% |
| D、丁达尔效应可以区分溶液和胶体 |
1克氢气燃烧生成液态水放出142.9kJ热量,表示该反应的热化学方程式正确的是( )
| A、2H2(g)+O2(g)=2H2O(l);△H=-285.8 kJ/mol | ||
B、H2(g)+
| ||
C、H2O(l)=H2(g)+
| ||
| D、2H2+O2=2H2O;△H=-571.6 kJ/mol |
镁粉与一定量某浓度的盐酸反应,但反应速度太快,为减慢反应速度,且不影响产生H2的总量,可向盐酸中加入的物质是( )
| A、Na2CO3 |
| B、CH3COONa |
| C、NaOH |
| D、NaHCO3 |
下列有关叙述正确的是( )
| A、Fe(OH)3胶体能够使水中悬浮的固体颗粒沉降,达到净水目的 |
| B、酸性氧化物都是非金属氧化物 |
| C、可利用焰色反应鉴别氯化钠和硫酸钾 |
| D、在水溶液中能电离出氢离子的物质为酸 |
下列说法正确的是( )
| A、常温常压下,等质量的硫蒸气和硫固体分别在氧气中完全燃烧,前者放出热量比后者少 |
| B、由C(石墨)=C(金刚石)△H=+1.90 kJ/mol可知,金刚石比石墨稳定 |
| C、在稀溶液中,H+(aq)+OH-(aq)=H2O(l)△H=-57.3 kJ/mol,若将含0.5 mol H2SO4的稀硫酸与含0.5mol Ba(OH)2 的氢氧化钡溶液混合,放出的热等于57.3 kJ |
| D、在101 kPa时,2 g H2 完全燃烧生成液态水,放出285.8 kJ热量,则氢气燃烧的热化学方程式可以表示为:2H2(g)+O2(g)=2H2O(l)△H=-571.6 kJ/mol |
下列化学用语正确的是( )
A、S原子的结构示意图: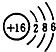 |
B、氯化钠的电子式: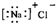 |
| C、乙烯的结构简式:CH2=CH2 |
| D、碳酸钠的电离方程式:NaHCO3=Na++H++CO32- |