题目内容
19.下列有关物质的性质和应用都正确的是( )| A. | MgO、Al2O3熔点高,都可用于制作耐火材料 | |
| B. | 氨气显碱性,可用碱石灰或无水CaCl2干燥 | |
| C. | 氢氟酸具有强酸性,可用于雕刻玻璃 | |
| D. | 铜的活动性比铁弱,可在海轮外壳上装铜块以减缓海轮腐蚀 |
分析 A.高熔点的物质可作耐火材料;
B.无水CaCl2干燥不能干燥氨气;
C.氢氟酸为弱酸;
D.在海轮外壳上装铜块,Fe作负极.
解答 解:A.高熔点的物质可作耐火材料,则MgO、Al2O3熔点高,都可用于制作耐火材料,故A正确;
B.无水CaCl2干燥不能干燥氨气,易形成络合物,而碱石灰可干燥氨气,且氨气不显碱性,故B错误;
C.氢氟酸为弱酸,能与二氧化硅反应,用于雕刻玻璃,故C错误;
D.在海轮外壳上装铜块,Fe作负极,加快海轮腐蚀,故D错误;
故选A.
点评 本题考查性质与用途,为高频考点,把握物质的性质、反应原理为解答的关键,侧重分析与应用能力的考查,选项B为解答的易错点,题目难度不大.

练习册系列答案
相关题目
9.下列叙述中说明某化学平衡一定发生移动的是( )
| A. | 混合体系中气体密度发生变化 | B. | 正、逆反应速率改变 | ||
| C. | 混合物中各组分的浓度改变 | D. | 反应物的转化率改变 |
10.钢铁厂在冷轧过程中会产生高浓度酸性含铁废水,主要含有H+、Cl-、Fe2+、Fe3+等,其处理的主要工艺流程如下:
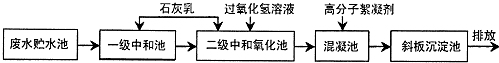
请回答:
(1)废水未经处理直接排放的危害是ab(填字母).
a腐蚀水利设施 b影响水生生物的自然生长
(2)石灰乳用于中和含铁废水中的酸,写出石灰乳与盐酸反应的化学方程式:Ca(OH)2+2HCl═CaCl2+2H2O.
(3)过氧化氧的主要作用是b(填字母).a还原剂 b氧化剂
(4)自来水厂常用漂白粉、液氯、二氧化氯、臭氧等作为消毒剂,杀灭水中的细菌.液氯注入水中后,能杀死水中细菌的物质是HClO(填化学式).
(5)污水处理中的主要化学方法有中和法、混凝法_、_沉淀法_、氧化还原法.
(6)某研究小组对钢铁厂高浓度酸性含铁废水进行监测时,取其样本稀释,测得有关数据如下:
稀释后的溶液中c(Fe2+)=0.12mol/L.

请回答:
(1)废水未经处理直接排放的危害是ab(填字母).
a腐蚀水利设施 b影响水生生物的自然生长
(2)石灰乳用于中和含铁废水中的酸,写出石灰乳与盐酸反应的化学方程式:Ca(OH)2+2HCl═CaCl2+2H2O.
(3)过氧化氧的主要作用是b(填字母).a还原剂 b氧化剂
(4)自来水厂常用漂白粉、液氯、二氧化氯、臭氧等作为消毒剂,杀灭水中的细菌.液氯注入水中后,能杀死水中细菌的物质是HClO(填化学式).
(5)污水处理中的主要化学方法有中和法、混凝法_、_沉淀法_、氧化还原法.
(6)某研究小组对钢铁厂高浓度酸性含铁废水进行监测时,取其样本稀释,测得有关数据如下:
| 离子 | H+ | Cl- | Fe2+ | Fe3+ |
| 浓度(mol•L)-1 | 0.16 | 0.94 | 0.18 |
7.化学与社会、生产、生活密切相关.下列说法正确的是( )
| A. | 用硫磺熏蒸使银耳增白 | |
| B. | 用废旧皮革生产药用胶囊可以提高原子利用率 | |
| C. | 用明矾对自来水进行杀菌消毒 | |
| D. | 限制使用一次性塑料制品的主要目的是防止形成“白色污染” |
14.I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?═?I3-(aq).测得不同温度下该反应的平衡常数如下表:
下列说法正确的是( )
| t/℃ | 5 | 15 | 25 | 35 | 50 |
| K | 1 000 | 850 | 690 | 625 | 400 |
| A. | 反应I2(aq)+I-(aq)?═?I3-(aq)的△H>0 | |
| B. | 利用该反应可以除去硫粉中少量的碘单质 | |
| C. | 在上述平衡体系中加入苯,平衡不移动 | |
| D. | 25℃时,向溶液中加入少量KI固体,平衡常数K小于690 |
4.工业上,将氨气和空气的混合气体通过灼热铂-铑合金网,发生氨氧化反应.若有标准状况下aL氨气完全反应,并转移了b个电子,则阿伏伽德罗常数NA的数值可表示为( )
| A. | $\frac{22.4b}{5a}$ | B. | $\frac{5a}{11.2b}$ | C. | $\frac{22.4a}{5b}$ | D. | $\frac{11.2b}{5a}$ |
8.某溶液中可能含有H+、NH4+、Fe3+、CO32-、SO42-、NO3-中的几种,且各种离子浓度相等.加入铝片,产生H2.现往原溶液中逐滴加入Ba(OH)2溶液至过量,可能发生的离子反应是( )
| A. | H++NH4++2OH-→NH3+2H2O | |
| B. | Ba2++2OH-+SO42-+2H+→BaSO4↓+2H2O | |
| C. | 2Ba2++6OH-+2SO42-+2Fe3+→2BaSO4↓+2Fe(OH)3↓ | |
| D. | Ba2++2OH-+SO42-+NH4++H+→NH3+BaSO4↓+2H2O |
9.只改变一个影响因素,平衡常数K与平衡移动的关系叙述不正确的是( )
| A. | K值不变,平衡可能移动 | |
| B. | 平衡向右移动时,K值不一定移动 | |
| C. | K值有变化,平衡一定移动 | |
| D. | 相同条件下,同一个反应的方程式的化学计量数增大2倍,K值也增大两倍 |
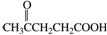 合成聚芳酯E的路线:
合成聚芳酯E的路线: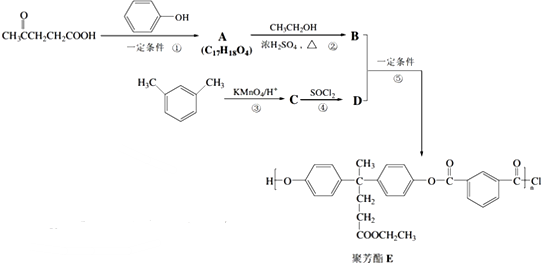
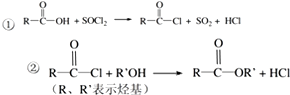
 .
. .
.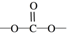 结构
结构 .
.