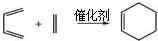题目内容
8.某溶液中可能含有H+、NH4+、Fe3+、CO32-、SO42-、NO3-中的几种,且各种离子浓度相等.加入铝片,产生H2.现往原溶液中逐滴加入Ba(OH)2溶液至过量,可能发生的离子反应是( )| A. | H++NH4++2OH-→NH3+2H2O | |
| B. | Ba2++2OH-+SO42-+2H+→BaSO4↓+2H2O | |
| C. | 2Ba2++6OH-+2SO42-+2Fe3+→2BaSO4↓+2Fe(OH)3↓ | |
| D. | Ba2++2OH-+SO42-+NH4++H+→NH3+BaSO4↓+2H2O |
分析 加入铝片,产生H2的溶液可能为酸性溶液或者碱性溶液,若为酸性溶液则溶液含有含有离子为:H+、NH4+、Fe3+、SO42-中,有因为各溶液离子浓度相等,依据电荷守恒,可知不含三价铁离子;
若为碱性溶液,则氢离子、铵根离子、三价铁离子都不存在,溶液无阳离子,不符合题意,排除,则原溶液中含有H+、NH4+、SO42-,氢离子、铵根离子能够与氢氧根离子反应,硫酸根离子能够与钡离子反应,据此写出离子方程式.
解答 解:加入铝片,产生H2的溶液可能为酸性溶液或者碱性溶液,若为酸性溶液则溶液含有含有离子为:H+、NH4+、Fe3+、SO42-中,有因为各溶液离子浓度相等,依据电荷守恒,可知不含三价铁离子;
若为碱性溶液,则氢离子、铵根离子、三价铁离子都不存在,溶液无阳离子,不符合题意,排除,则原溶液中含有H+、NH4+、SO42-,氢离子与铵根离子离子与氢氧根离子都反应,氢离子先反应,
加入少量氢氧化钡,离子方程式:Ba2++2OH-+SO42-+2H+→BaSO4↓+2H2O;
加入过量氢氧化钡,离子方程式:Ba2++2OH-+SO42-+NH4++H+→NH3+BaSO4↓+2H2O;
故选:BD.
点评 本题考查了离子方程式的书写,准确分析溶液中所含离子成分是解题关键,题目难度中等.

练习册系列答案
相关题目
18.下列说法正确的是( )
| A. | 3-戊醇发生消去反应时可得2种不同的烯烃 | |
| B. | 聚合物 可由单体CH3CH=CH2和CH2=CH2加聚制得 可由单体CH3CH=CH2和CH2=CH2加聚制得 | |
| C. | 醇在Cu/△条件下都能氧化成醛 | |
| D. | 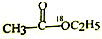 在酸性条件下水解产物是 在酸性条件下水解产物是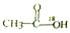 和C2H5OH 和C2H5OH |
19.下列有关物质的性质和应用都正确的是( )
| A. | MgO、Al2O3熔点高,都可用于制作耐火材料 | |
| B. | 氨气显碱性,可用碱石灰或无水CaCl2干燥 | |
| C. | 氢氟酸具有强酸性,可用于雕刻玻璃 | |
| D. | 铜的活动性比铁弱,可在海轮外壳上装铜块以减缓海轮腐蚀 |
16.下列化学变化与氧化还原反应无关的是( )
| A. | 粮食酿醋 | B. | 铁片镀锌 | C. | 盐酸除铁锈 | D. | 铝制品钝化 |
3.下列各组离子在溶液中能大量共存,且通入足量SO2气体后,最终溶液仍然保持澄清的离子组是( )
| A. | Ba2+、Na+、Cl-、NO3- | B. | Fe3+、Ba2+、Cl-、I- | ||
| C. | Na+、NH4+、SO42-、OH- | D. | K+、Ca2+、HCO3-、Cl- |
20.下列过程中不放出热量的是( )
| A. | 碳酸钠固体中加少量水 | B. | 碳酸氢钠固体中加少量水 | ||
| C. | 钠与水的反应 | D. | 过氧化钠与水反应 |
17.下列工作原理或变化过程不涉及化学反应的是( )
| A. |  高炉炼铁 | B. |  火箭发射 | C. |  酸雨的形成 | D. |  丁达尔效应 |
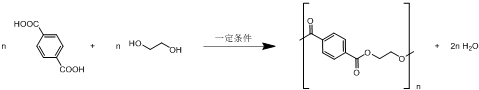 .
.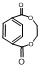 .
.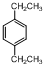 .
.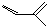 ,两分子该单体发生“Diels-Alder反应”,写出两种不同结构的产物
,两分子该单体发生“Diels-Alder反应”,写出两种不同结构的产物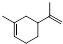 、
、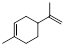 .
.