题目内容
18.有机物B、C、D互为( )| A. | 同位素 | B. | 同系物 | C. | 同分异构体 | D. | 同素异形体 |
分析 先根据碳架结构确定物质的名称:A为丁烷,B为1-丁烯,C为2-丁烯,D为2-甲基-1-丙烯,E为2-甲基丙烷,F为1-丁炔,G为2-丁炔,H为环丁烷;
再根据分子式相同、结构不同的化合物属于同分异构体进行判断.
解答 解:A为丁烷,B为1-丁烯,C为2-丁烯,D为2-甲基-1-丙烯,E为2-甲基丙烷,F为1-丁炔,G为2-丁炔,H为环丁烷;
B、C、D的分子式都为C4H8,三者的结构不同,所以它们互为同分异构体,
故选C.
点评 本题考查有机物的结构与同系物、同分异构体辨析,题目难度不大,明确碳的成键方式及图中碳原子的位置是解答本题的关键,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
7.(1)25℃时,在0.1L 0.2mol•L-1的HA溶液中,有0.001mol的HA电离成离子,则该溶液的pH=2.
(2)25℃时,若向0.1mol/L氨水中加入稀硫酸至溶液的pH=7,此时c(NH4+)=amol/L,则c(SO42-)=0.5amol/L.
(3)室温下,若向0.1mol/L氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1:1,则所得溶液中各离子的物质的量浓度由大到小的顺序是c(NH4+)>c(SO42-)>c(H+)>c(OH-).
(4)电离平衡常数是衡量弱电解质电离程度强弱的物理量.已知:
回答下列问题
?25℃时,有等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液,三溶液的pH由大到小的顺序为Na2CO3溶液>NaCN溶液>CH3COONa溶液.
?向NaCN溶液中通入少量CO2,所发生反应的化学方程式为:NaCN+H2O+CO2=HCN+NaHCO3.
(5)常温下,在一定体积pH=12的Ba(OH)2溶液中,逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液pH=11.若反应后溶液的体积等于Ba(OH)2溶液与NaHSO4溶液的体积之和,则Ba(OH)2溶液与NaHSO4溶液的体积比是1:4.
(2)25℃时,若向0.1mol/L氨水中加入稀硫酸至溶液的pH=7,此时c(NH4+)=amol/L,则c(SO42-)=0.5amol/L.
(3)室温下,若向0.1mol/L氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1:1,则所得溶液中各离子的物质的量浓度由大到小的顺序是c(NH4+)>c(SO42-)>c(H+)>c(OH-).
(4)电离平衡常数是衡量弱电解质电离程度强弱的物理量.已知:
| 化学式 | 电离常数(25℃) |
| HCN | K=4.9×l0-10 |
| CH3COOH | K=1.8×l0-5 |
| H2CO3 | K1=4.3×l0-7、K2=5.6×l0-11 |
?25℃时,有等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液,三溶液的pH由大到小的顺序为Na2CO3溶液>NaCN溶液>CH3COONa溶液.
?向NaCN溶液中通入少量CO2,所发生反应的化学方程式为:NaCN+H2O+CO2=HCN+NaHCO3.
(5)常温下,在一定体积pH=12的Ba(OH)2溶液中,逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液pH=11.若反应后溶液的体积等于Ba(OH)2溶液与NaHSO4溶液的体积之和,则Ba(OH)2溶液与NaHSO4溶液的体积比是1:4.
9.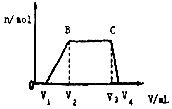 1L某混合溶液,可能含有的离子如表:
1L某混合溶液,可能含有的离子如表:
(1)往该溶液中逐滴加入NaOH溶液,产生沉淀的物质的量(n)与加入NaOH溶液的体积(V)的关系如图所示.则该溶液中一定不含有的离子是Mg2+、Fe2+、Fe3+、CO32-、AlO2-.
(2)BC段离子方程式为NH4++OH-═NH3•H2O.
(3)经检测,该溶液中还含有大量的Cl-、Br-、I-,若向1L该混合溶液中通入一定量的Cl2,溶液中Cl-、Br-、I-的物质的量与通入Cl2的体积(标准状况)的关系如表所示,分析后回答下列问题:
①a=0.15.
②当通入Cl2的体积为2.8L时,溶液中发生反应的离子方程式为Cl2+2I-=I2+2Cl-.
③原溶液中Cl-、Br-、I-的物质的量浓度之比为10:15:4.
 1L某混合溶液,可能含有的离子如表:
1L某混合溶液,可能含有的离子如表:| 可能大量含有的阳离子 | H+、K+、Mg2+、Al3+、NH4+、Fe2+、Fe3+ |
| 可能大量含有的阴离子 | Cl-、Br-、I-、CO32-、AlO2- |
(2)BC段离子方程式为NH4++OH-═NH3•H2O.
(3)经检测,该溶液中还含有大量的Cl-、Br-、I-,若向1L该混合溶液中通入一定量的Cl2,溶液中Cl-、Br-、I-的物质的量与通入Cl2的体积(标准状况)的关系如表所示,分析后回答下列问题:
| Cl2的体积(标准状况) | 2.8L | 5.6L | 11.2L |
| n(Cl-) | 1.25mol | 1.5mol | 2mol |
| n(Br-) | 1.5mol | 1.4mol | 0.9mol |
| N(I-) | a mol | 0 | 0 |
②当通入Cl2的体积为2.8L时,溶液中发生反应的离子方程式为Cl2+2I-=I2+2Cl-.
③原溶液中Cl-、Br-、I-的物质的量浓度之比为10:15:4.
6.下列指定反应的离子方程式正确的是( )
| A. | AlCl3溶液中加入过量氨水:A13++4 NH3•H2O═AlO2-+4NH4++2H2O | |
| B. | NaA1O2溶液中AlO2-的水解:AlO2-+2H2O═A1(OH)3↓+OH- | |
| C. | AgCl悬浊液中加入KI溶液得到黄色沉淀:Ag++I-═AgI↓ | |
| D. | 明矾净水原理:A13++3H2O?A1(OH)3(胶体)+3H+ |
13.下列物质的分子或晶体中包含正四面体结构,且键角不等于109o28’的是( )
| A. | 白磷 | B. | 金刚石 | C. | 氨气 | D. | 甲烷 |
3.对于反应CO(g)+H2O(g)?CO2(g)+H2(g),△H<0,在其他条件不变的情况下,下列说法正确的是( )
| A. | 加入催化剂,改变了反应的途径,反应的△H也随之改变 | |
| B. | 增大压强,正逆反应的化学反应速率都减小 | |
| C. | 升高温度,正反应化学反应速率增大,逆反应化学反应速率减 | |
| D. | 对该反应来说,无沦反应进行到何时,混合气体的总物质的量不变 |
10.化学与人类生活、生产和社会可持续发展密切相关.下列说法正确的是( )
| A. | 往自来水中加入明矾进行杀菌消毒 | |
| B. | 氮化硅陶瓷是一种新型的无机非金属材料 | |
| C. | 在食品袋中放入硅胶、生石灰的透气小袋,可防止食物受潮、氧化变质 | |
| D. | 为提高农作物的产量和质量,应大量使用化肥和农药 |
8.人体中含量最高的微量元素是( )
| A. | 碘 | B. | 铁 | C. | 锌 | D. | 铜 |