题目内容
14.某品牌糖衣片补血剂,除去糖衣后显淡蓝绿色,主要成分是硫酸亚铁,不含其它铁的化合物.某研究性学习小组为测定该补血剂中硫酸亚铁的含量进行了以下探究: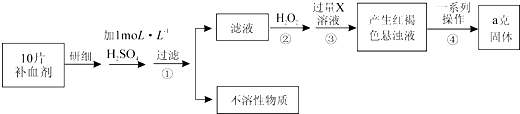
请回答下列问题:
Ⅰ.(1)实验时用10mol•L-1的浓硫酸,配制100mL 1mol•L-1 H2SO4溶液,所需浓硫酸的体积为10.0mL;
(2)下列操作中,容量瓶所具备的功能有(填序号);
A.配制一定体积准确浓度的标准溶液 B.长期贮存溶液
C.常用来代替量筒量取一定体积的液体 D.用来溶解固体溶质
(3)在下列配制过程示意图中,有错误的是①④(填写序号);
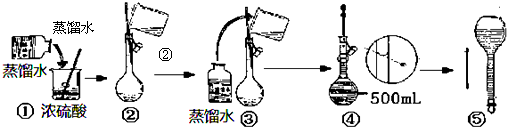
(4)下列说法正确的AC
A.洗涤烧杯2~3次,并将洗涤液移入容量瓶以减少误差
B.某同学将浓硫酸稀释后未冷却至室温便将溶液转移至容量瓶,所配溶液浓度会偏低
C.定容时仰视观察,所配溶液浓度会偏低
Ⅱ.(1)步骤②加入过量H2O2后,溶液中主要存在的金属阳离子是Fe3+;
(2)从红褐色的悬浊液到最后的称量,其过程中所需的基本操作为:
a.过滤,b.洗涤,c.灼烧,d.冷却
(3)若称得固体的质量为ag,则每片补血剂中含硫酸亚铁的质量为0.19ag.
分析 Ⅰ.(1)根据浓硫酸在稀释前后,溶质的物质的量保持不变进行计算;
(2)容量瓶是配制一定体积准确浓度的标准溶液的定容仪器;
(3)稀释浓硫酸时是将浓硫酸倒入水中,并用玻璃棒不断搅拌,使产生的热量迅速扩散;读数时应平视;
(4)根据公式c=$\frac{n}{V}$,可以根据影响n和V的因素来分析回答;
Ⅱ.由流程图可知,该实验原理为:将药品中的Fe2+形成溶液,将Fe2+氧化为Fe3+,使Fe3+转化为氢氧化铁沉淀,再转化为氧化铁,通过测定氧化铁的质量,计算补血剂中铁元素的含量,
(1)步骤②加入过量H2O2将Fe2+氧化为Fe3+;
(2)由氢氧化铁悬浊液最终转化为氧化铁,需要过滤、洗涤的氢氧化铁,然后灼烧生成氧化铁,冷却后称量氧化铁的质量;
(3)根据铁元素守恒可知ag氧化铁中铁元素的质量即为10片补血剂中铁的质量,据此计算.
解答 解:Ⅰ.(1)浓硫酸在稀释前后,溶质的物质的量保持不变,设所需浓硫酸最小体积为V,则100mL×10-3×1mol/L=10mol/L×V,解得V=10.0mL,
故答案为:10.0;
(2)容量瓶作为精密仪器不可用于储存和溶解,也不能测量除其规格以外容积的液体体积,
故答案为:A;
(3)稀释浓硫酸时是将浓硫酸沿器壁倒入水中,并用玻璃棒不断搅拌,使产生的热量迅速扩散;读数时应平视,不能仰视和俯视,
故答案为:①④;
(4)A.洗涤烧杯2~3次,并将洗涤液移入容量瓶,否则浓度偏小,故A正确;
B.未冷却体积偏小,浓度偏大,故B错误;
C.定容时仰视,体积偏大,浓度偏小,故C正确;
故答案为:AC;
Ⅱ.(1)步骤②加入过量H2O2将Fe2+氧化为Fe3+,所以溶液中主要存在的金属阳离子是Fe3+,
故答案为:Fe3+;
(2)由氢氧化铁悬浊液最终转化为氧化铁,需要过滤、洗涤的氢氧化铁,然后灼烧生成氧化铁,冷却后称量氧化铁的质量,
故答案为:过滤;
(3)ag氧化铁中铁元素的质量即为10片补血剂中铁的质量,所以每片补血剂含铁元素的质量:$\frac{ag×\frac{112}{160}}{10}$=0.07ag,含硫酸亚铁的质量为:$\frac{0.07a}{\frac{56}{152}}$=0.19ag,
故答案为:0.19a.
点评 本题考查学生对物质的量浓度溶液的配制实验原理与实验操作的理解、化学计算等知识,题目难度中等,清楚实验原理是解题的关键,需要学生具备扎实的基础知识与综合运用知识分析问题、解决问题的能力.

 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案| A. | NH4+、Ba2+、Brˉ、CO32ˉ | B. | Clˉ、NO3ˉ、Fe2+、H+ | ||
| C. | K+、Na+、SO42ˉ、MnO4ˉ | D. | Na+、H+、SO42ˉ、HCO3ˉ |
| A. | FeCl2→FeCl3 | B. | CuO→Cu | C. | KMnO4→MnO2 | D. | Cl2→NaCl |
| A. | 直线形;平面三角形 | B. | V形;三角锥形 | ||
| C. | 直线形;三角锥形 | D. | V形;平面三角形 |
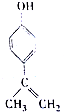
| A. | 该物质的分子式是C9H11O | |
| B. | 该物质分子中的所有C原子可以共面 | |
| C. | 滴入KMnO4(H+)溶液,可观察到紫色褪去,能证明结构中存在碳碳双键 | |
| D. | 1mol该物质分别与浓溴水和H2反应时,最多消耗Br2和H2分别是3mol、4mol |

该有机分子的核磁共振氢谱图如图3(单位是ppm).下列关于该有机物的叙述,不正确的是( )
| A. | 该有机物不同化学环境的氢原子有8种 | |
| B. | 该有机物属于芳香族化合物 | |
| C. | 键线式中的Et代表的基团为-CH2CH3 | |
| D. | 1mol该有机物完全燃烧可以产生6mol水 |
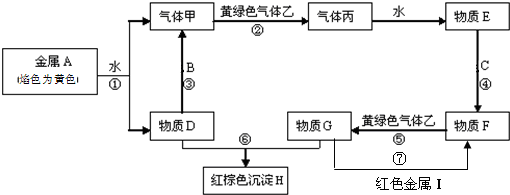
(1)合金中至少有一种金属(填“金属”或“非金属”)元素,目前使用量最大的合金是钢合金,取5.6g碳素钢与足量的稀盐酸充分反应后,生成的氢气在标准状况下的体积小于2.24L(填“>”、“<”或“=”).
(2)合金可用几种不同的合适的材料在熔融状态下混合而成,钛能形成多种类型的合金,下表所示是几种金属的熔、沸点,其中不能形成相应合金的是B.
| Na | Ni | Al | Ti | Sn | |
| 熔点(℃) | 97.5 | 1453 | 660 | 1660 | 231.9 |
| 沸点(℃) | 883 | 2732 | 2200 | 3287 | 2270 |
(3)古代的炼金术士们认为通过炼制可将某些廉价的金属转化为贵重金属银或金,并在实际操作中得到了貌似黄金的“药金”.操作方法是将炉甘石(ZnCO3)、赤铜(Cu2O)和木炭混合加热.相关反应为ZnCO3$\frac{\underline{\;\;△\;\;}}{\;}$ZnO+CO2↑、2ZnO+C$\frac{\underline{\;\;△\;\;}}{\;}$2Zn+CO2↑、2Cu2O+C$\frac{\underline{\;△\;}}{\;}$4Cu+CO2↑
(4)“药金”就是现在人们所说的黄铜,不少骗子常利用其颜色与黄金相似的特点将其冒充为“金元宝”,请你设计一种简单的方法判定某“金元宝”是假的:取少量样品浸入稀盐酸中(或稀硫酸),若有气体产生,则该样品为假黄金;若没有气体产生,则样品为黄金.
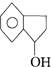 互为同分异构,满足下列三个条件:
互为同分异构,满足下列三个条件: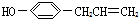
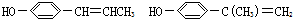 (其中两个).
(其中两个).