题目内容
4.现有金属单质A、B、C、I和气体甲、乙、丙及物质D、E、F、G、H.其中B是地壳中含量最多的金属.它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出).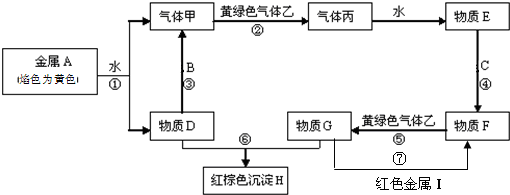
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:CFe、HFe(OH)3
(2)写出反应③的化学方程式:2Al+2NaOH+2H2O═2NaAlO2+3H2↑
写出反应⑦的化学方程式:2FeCl3+Cu═2FeCl2+CuCl2
写出反应⑥的离子方程式Fe3++3OH-=Fe(OH)3↓
分析 金属单质A焰色反应为黄色,故A为Na,与水反应生成NaOH与氢气,则D为NaOH,气体甲为H2;B是地壳中含量最多的金属,氢氧化钠与金属B反应生成氢气,故金属B为Al.黄绿色气体乙为Cl2,与氢气反应生成丙为HCl,HCl溶于水得物质E为盐酸.氢氧化钠与物质G反应生成红褐色沉淀H是Fe(OH)3,故物质G中含有Fe3+,金属C与盐酸反应生成F,F与氯气反应生成G,可知金属C为Fe,物质F为FeCl2,物质G为FeCl3,红色金属I为Cu,据此解答.
解答 解:金属单质A焰色反应为黄色,故A为Na,与水反应生成NaOH与氢气,则D为NaOH,气体甲为H2;B是地壳中含量最多的金属,氢氧化钠与金属B反应生成氢气,故金属B为Al.黄绿色气体乙为Cl2,与氢气反应生成丙为HCl,HCl溶于水得物质E为盐酸.氢氧化钠与物质G反应生成红褐色沉淀H是Fe(OH)3,故物质G中含有Fe3+,金属C与盐酸反应生成F,F与氯气反应生成G,可知金属C为Fe,物质F为FeCl2,物质G为FeCl3,红色金属I为Cu.
(1)C为Fe,H为Fe(OH)3,故答案为:Fe;Fe(OH)3;
(2)反应③的化学方程式:2Al+2NaOH+2H2O═2NaAlO2+3H2↑,
反应⑦的化学方程式:2FeCl3+Cu═2FeCl2+CuCl2,
反应⑥的离子方程式:Fe3++3OH-=Fe(OH)3↓,
故答案为:2Al+2NaOH+2H2O═2NaAlO2+3H2↑;2FeCl3+Cu═2FeCl2+CuCl2;Fe3++3OH-=Fe(OH)3↓.
点评 本题考查无机物的推断,题目难度中等,需要学生熟练掌握元素化合物知识,特殊的颜色与特殊反应是推断的突破口.

练习册系列答案
相关题目
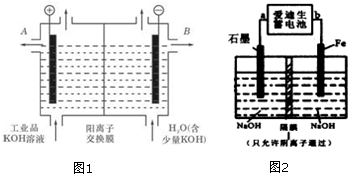
14.用铂电极电解CuSO4溶液,当铜离子浓度降至一半时,停止通电,若使CuSO4溶液恢复到原浓度,应加入的物质是( )
| A. | CuSO4 | B. | CuO | C. | CuSO4•5H2O | D. | Cu(OH)2 |
16.下列有关实验的叙述正确的是( )
| A. | 过滤时,可用玻璃棒搅拌漏斗中的液体以加快过滤速率 | |
| B. | 用湿润的pH试纸测溶液的pH,因溶液被稀释而使测量值变大 | |
| C. | 酸碱滴定管、容量瓶、分液漏斗使用前必须检查是否漏水 | |
| D. | 酸碱滴定实验中,需用待滴定溶液润洗锥形瓶以减小实验误差 |
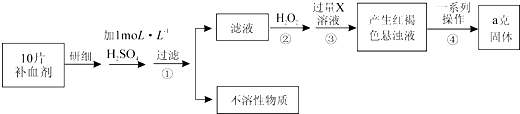
13.人体血红蛋白中含有Fe2+,如果误食亚硝酸盐,会使人中毒,这是因为亚硝酸盐将Fe2+氧化为Fe3+,生成高铁血红蛋白,而丧失与O2结合的能力.服用维生素C可缓解亚硝酸盐的中毒,下列说法中正确的是( )
| A. | 中毒过程中NO2-表现还原性 | |
| B. | 中毒过程中Fe2+表现氧化性 | |
| C. | 解毒过程中维生素C具有还原性 | |
| D. | 解毒过程中维生素C把Fe2+氧化为Fe3+ |