��Ŀ����
����һ�����ȼ������ۺ���������Fe2O3����ĩ�Ļ����ڸ�����ʹ֮��ַ�Ӧ������Ӧ��Ĺ����Ϊ���ȷݣ���������ʵ�飨�ٶ���Ӧǰ����Һ��������䣩��
��������һ�ݹ����м���100mL 2.0mol?L-1��NaOH��Һ������ʹ���ַ�Ӧ����ˣ������Һ�е�c��OH-��=1mol?L-1
������һ�ݹ����м���100mL 4.0mol?L-1��HCl��Һ��ʹ����ȫ���ܽ⣬��÷�Ӧ��������Һ��ֻ��H+��Fe2+��Al3+������������c��H+��=0.1mol?L-1 ���������������������״����Ϊ��������
��������һ�ݹ����м���100mL 2.0mol?L-1��NaOH��Һ������ʹ���ַ�Ӧ����ˣ������Һ�е�c��OH-��=1mol?L-1
������һ�ݹ����м���100mL 4.0mol?L-1��HCl��Һ��ʹ����ȫ���ܽ⣬��÷�Ӧ��������Һ��ֻ��H+��Fe2+��Al3+������������c��H+��=0.1mol?L-1 ���������������������״����Ϊ��������
| A��2.856L |
| B��2.448L |
| C��2.688L |
| D��2.352L |
���㣺�йػ���ﷴӦ�ļ���
ר�⣺
�������ټ�������������Һ������������ʣ�࣬�ɵ���غ��֪��c��Na+��=c��OH-��+c��AlO2-�����ٸ���n=cV����n��AlO2-��������AlԪ���غ����n��Al����
�ڼ������ᷴӦ��������ʣ�࣬�ɵ���غ��֪��c��H+��+2c��Fe2+��+3c��Al3+��=c��Cl-�����ٸ���n=cV����n��Fe2+��������FeԪ���غ����n��Fe2O3����
����2Al+Fe2O3
2Fe+Al2O3������ȷ����Ӧ����ɷּ��������ʵ��������ݵ���ת���غ�����������������ʵ������������������������
�ڼ������ᷴӦ��������ʣ�࣬�ɵ���غ��֪��c��H+��+2c��Fe2+��+3c��Al3+��=c��Cl-�����ٸ���n=cV����n��Fe2+��������FeԪ���غ����n��Fe2O3����
����2Al+Fe2O3
| ||
���
�⣺�ټ�������������Һ������������ʣ�࣬�ɵ���غ��֪��c��Na+��=c��OH-��+c��AlO2-������c��AlO2-��=2mol/L-1mol/L=1mol/L����ÿ����n��Al��=n��AlO2-��=1mol/L��0.1L=0.1mol��
�ڼ������ᷴӦ��������ʣ�࣬����AlԪ���غ㣬c��Al3+��=
=1mol/L���ɵ���غ��֪��c��H+��+2c��Fe2+��+3c��Al3+��=c��Cl-��������0.1mol/L+2c��Fe2+��+3��1mol/L=4mol/L����ã�c��Fe2+��=0.45mol/L��n��Fe2+��=0.45mol/L��0.1L=0.045mol������FeԪ���غ㣬ÿ����n��Fe2O3��=
=0.0225mol��
��2Al+Fe2O3
2Fe+Al2O3����֪0.1molAl��ȫ��Ӧ��ҪFe2O3�����ʵ���=0.1mol��
=0.05mol��0.0225mol����Fe2O3��ȫ��Ӧ��Al��ʣ�࣬����FeΪ0.045mol���μӷ�ӦAlΪ0.0225mol��2=0.045mol��ʣ��AlΪ0.1mol-0.045mol=0.055mol��
���ݵ���ת���غ㣬���з�Ӧ�����������ʵ���Ϊ
+
=0.1275mol��
�ʢ����������������Ϊ��0.1275mol��22.4L/mol=2.856L��
��ѡA��
�ڼ������ᷴӦ��������ʣ�࣬����AlԪ���غ㣬c��Al3+��=
| 0.1mol |
| 0.1L |
| 0.045mol |
| 2 |
��2Al+Fe2O3
| ||
| 1 |
| 2 |
���ݵ���ת���غ㣬���з�Ӧ�����������ʵ���Ϊ
| 0.055mol��3 |
| 2 |
| 0.045mol��2 |
| 2 |
�ʢ����������������Ϊ��0.1275mol��22.4L/mol=2.856L��
��ѡA��
���������⿼��������㣬�ж����ȼ���Ӧ�����ɷ��ǹؼ���ע�������غ㷨���н�𣬲��ؿ���ѧ������˼ά�������ѶȽϴ�

��ϰ��ϵ�д�
�����Ŀ
���л�ѧ����ʽ������������д��ȷ���ǣ�������
| A��������������Һ��ȥ���ڶ�����̼�����е��Ȼ��⣺NaOH+HCl�TNaCl+H2O |
| B����ȥ�Ȼ�����������̼���ƣ�Na2CO3+H2SO4�TNa2SO4+CO2��+H2O |
| C��������ˮ��pHԼΪ5.6��ԭ��CO2+H2O�TH2CO3 |
| D���������ȥ���⣺Fe��OH��3+3HCl�TFeCl3+3H2O |
��NA��ʾ�����ӵ�����������������ȷ���ǣ�������
| A����״���£�22.4L H2���е�ԭ����ΪNA |
| B����������O2��O3����������ԭ������� |
| C�����³�ѹ�£�14g N2���е�����Ϊ7NA |
| D��28g CO��22.4L CO2������̼ԭ������� |
��50mL 1mol?L-1��AlCl3��Һ��������Ũ����ȵ��ǣ�������
| A��150mL1mol?L-1��NaCl |
| B��75 mL2mol?L-1��NH4Cl |
| C��25mL 2mol?L-1��KCl |
| D��75 mL1.5mol?L-1��CaCl2 |
����˵����ȷ���ǣ�������
| A��100g��������Ϊ46%���Ҵ���Һ�У�����14mol���ۼ� |
| B��1���������к���3��̼̼˫�� |
| C����ϩ�ͱ�����ʹ��ˮ��ɫ����ɫ��ԭ����ͬ |
| D���ױ�����������ԭ�Ӷ�����ͬһƽ���� |
����ҩƷ��������������������ˮ�����ƣ�����ʵ��ǣ�������
| A��Na2SO4 |
| B��NaCl |
| C��AgNO3 |
| D��K2CO3 |
�ڻ��Ϸ�Ӧ���ֽⷴӦ���û���Ӧ�����ֽⷴӦ���ֻ�ѧ��Ӧ�У�������Ԫ�ػ��ϼ۷����仯�ķ�Ӧ�����У�������
| A��һ�� | B������ | C������ | D������ |
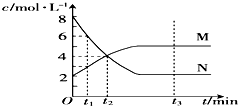 ��һ���¶��£�������ijһ��Ӧ��M��N�����ʵ���Ũ���淴Ӧʱ��仯��������ͼ�������б�������ȷ���ǣ�������
��һ���¶��£�������ijһ��Ӧ��M��N�����ʵ���Ũ���淴Ӧʱ��仯��������ͼ�������б�������ȷ���ǣ�������| A���÷�Ӧ�Ļ�ѧ����ʽΪ2N?M |
| B��t1ʱ��M��Ũ����NŨ�ȵ�2�� |
| C��t3ʱ������Ӧ���ʴ����淴Ӧ���� |
| D��t2ʱ�������淴Ӧ������ȣ���ѧ��Ӧ�ﵽ��ƽ�� |
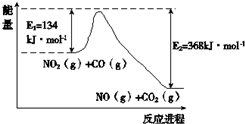 �밴����Ҫ�ش�������Ӧ���⣺
�밴����Ҫ�ش�������Ӧ���⣺