题目内容
与50mL 1mol?L-1的AlCl3溶液中氯离子浓度相等的是( )
| A、150mL1mol?L-1的NaCl |
| B、75 mL2mol?L-1的NH4Cl |
| C、25mL 2mol?L-1的KCl |
| D、75 mL1.5mol?L-1的CaCl2 |
考点:物质的量浓度
专题:物质的量浓度和溶解度专题
分析:根据化学式可知1mol?L-1的AlCl3溶液中氯离子浓度为3mol/L,结合各选项中化学式判断溶液中氯离子浓度,注意离子的浓度与溶液的体积无关,与物质的构成有关.
解答:
解:1mol?L-1的AlCl3溶液中氯离子浓度为:3mol/L.
A、150 mL 1 mol?L-1的NaCl溶液中,氯离子浓度为:1 mol?L-1,故A错误;
B、75 mL 2 mol?L-1的NH4Cl溶液中,氯离子浓度为:2mol/L,故B错误;
C、25 mL 2mol?L-1的KCl溶液中,氯离子浓度为:2mol/L,故C错误;
D、75mL 1.5 mol?L-1的CaCl2溶液中氯离子浓度为:3mol/L,故D正确;
故选D.
A、150 mL 1 mol?L-1的NaCl溶液中,氯离子浓度为:1 mol?L-1,故A错误;
B、75 mL 2 mol?L-1的NH4Cl溶液中,氯离子浓度为:2mol/L,故B错误;
C、25 mL 2mol?L-1的KCl溶液中,氯离子浓度为:2mol/L,故C错误;
D、75mL 1.5 mol?L-1的CaCl2溶液中氯离子浓度为:3mol/L,故D正确;
故选D.
点评:本题考查了物质的量浓度的计算,题目难度较小,明确物质的构成是解答本题的关键,并注意注意离子的浓度与溶液的体积无关,与物质的构成有关..

练习册系列答案
相关题目
能实现下列物质间直接转化的元素是( )
单质
氧化物
酸或碱
盐.
单质
| +O2 |
| +H2O |
| NaOH或HCl |
| A、镁 | B、硫 |
| C、铜 | D、N2 |
下列事实不能用勒沙特列原理解释的是( )
| A、硫酸工业中,使用过量的空气以提高二氧化硫的利用率 |
| B、配制氯化铁溶液时,将氯化铁加入盐酸中,然后加水稀释 |
| C、实验室常用排饱和食盐水的方法收集氯气 |
| D、二氧化氮与四氧化二氮的平衡体系,加压缩小体积后颜色加深 |
根据某种共性,可将SO3、CO2归为同类氧化物.下列物质中也属于这类氧化物的是( )
| A、CaCO3 |
| B、SO2 |
| C、KMnO4 |
| D、Na2O |
2007年3月,温家宝指出“优化结构、提高效益和降低消耗、保护环境”,这是我国国民经济和社会发展的基础性要求.你认为下列行为不符合这个要求的是( )
| A、加快太阳能、风能、生物质能、海洋能等清洁能源的开发利用 |
| B、大力发展农村沼气,将废弃的秸轩转化为清洁高效的能源 |
| C、将煤转化成气体燃料可以有效地减少“温室效应”的气体产生 |
| D、研制开发以水代替有机溶剂的化工涂料 |
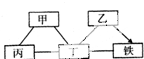 现有铁、氧化铁、稀硫酸、氢氧化钙溶液、碳酸钠溶液等五种物质,存在着如图所示的相互反应或转化关系(图中“一”表示物质间可以发生化学反应,“→”表示物质间存在相应的转化关系).下列判断合理的是( )
现有铁、氧化铁、稀硫酸、氢氧化钙溶液、碳酸钠溶液等五种物质,存在着如图所示的相互反应或转化关系(图中“一”表示物质间可以发生化学反应,“→”表示物质间存在相应的转化关系).下列判断合理的是( )| A、丙可能是碳酸钠溶液 |
| B、丁可能是氢氧化钙溶液 |
| C、乙必须通过置换反应转化为铁 |
| D、甲和丁的反应一定是中和反应 |
现有一包铝热剂是铝粉和氧化铁(Fe2O3)粉末的混合物,在高温下使之充分反应,将反应后的固体分为两等份,进行如下实验(假定反应前后溶液的体积不变):
①向其中一份固体中加入100mL 2.0mol?L-1的NaOH溶液,加热使其充分反应后过滤,测得溶液中的c(OH-)=1mol?L-1
②向另一份固体中加入100mL 4.0mol?L-1的HCl溶液,使固体全部溶解,测得反应后所得溶液中只有H+、Fe2+和Al3+三种阳离子且c(H+)=0.1mol?L-1 ,则产生的气体的体积(标准状况)为( )
①向其中一份固体中加入100mL 2.0mol?L-1的NaOH溶液,加热使其充分反应后过滤,测得溶液中的c(OH-)=1mol?L-1
②向另一份固体中加入100mL 4.0mol?L-1的HCl溶液,使固体全部溶解,测得反应后所得溶液中只有H+、Fe2+和Al3+三种阳离子且c(H+)=0.1mol?L-1 ,则产生的气体的体积(标准状况)为( )
| A、2.856L |
| B、2.448L |
| C、2.688L |
| D、2.352L |
空气的成分中,能导致温室效应的气体是( )
| A、氮气 | B、氧气 |
| C、二氧化碳 | D、稀有气体 |