题目内容
13.氯化铜、氯化亚铜是重要的化工原料,广泛用作有机合催化剂.已知:氯化铜容易潮解.

I.实验室用如图所示装置,用还原铜粉和氯气来制备氯化铜.
(1)石棉绒的作用是增大铜粉与氯气的接触面积;B装置中的试剂是饱和NaCl溶液.E和F装置及试剂可用一有碱石灰(或生石灰)的干燥管替换(填装置及所装试剂).
(2)当Cl2排尽空气后,加热D.则D中发生反应的化学方程式为Cu+Cl2$\frac{\underline{\;\;△\;\;}}{\;}$CuCl2.
(3)若实验测得CuCl2质量分数为90.0%,则其中可能含有的杂质是石棉绒(Cu或CuCl)(一种即可).
Ⅱ.另取纯净CuCl2固体用于制备CuCl.
75.00gCuCl2固体$\underset{\stackrel{(1)溶解}{→}}{加入0.2mol/L100.00mLHCl及适量蒸馏水}$200.00mL溶液(黄绿色)$→_{通入SO_{2}△}^{(2)还原}$CuCl(白色沉淀)
(4)溶解时加入HCl溶液的目的主要是Cu2++2H2O?Cu(OH)2+2H+,加酸抑制Cu2+的水解(结合离子方程式回答).
(5)若接上述操作用10.0mol/L的HCl代替0.2mol/L HCl,通人SO2后,200.00mL黄绿色溶液颜色褪去,但无白色沉淀.对此现象:
甲同学提出假设:c(H+)过大.
为验证此假设,可取75.00g CuCl2固体与100mL0.2mol/LHCl及50mL9.8mol/LH2SO4配制成200.00mL溶液再按上述操作进行实验.
乙同学查阅资料:体系中存在平衡2Cl-(aq)+CuCl(s)=CuCl32-(aq).则出现此现象另一可能的原因是c(Cl-)过大.
分析 A中浓盐酸和二氧化锰在加热条件下制备氯气,B为饱和食盐水,用于除去HCl,C为浓硫酸,用于干燥氯气,D中加热条件下反应生成氯化铜,E为浓硫酸,可防止空气中的水蒸气进入D中,F为氢氧化钠溶液,可吸收氯气,防止污染空气;
另取纯净CuCl2固体用于制备CuCl,应先将氯化铜溶液盐酸中,以防止铜离子水解而导致溶液浑浊,然后通入二氧化硫,发生氧化还原反应可生成CuCl,注意氯离子浓度不能过大,防止生成CuCl32-,以此解答该题.
解答 解:(1)石棉绒的作用是增大铜粉与氯气反应的接触面积;氯气有毒,所以B装置是吸收尾气,而氯气用氢氧化钠吸收,E为浓硫酸,可防止空气中的水蒸气进入D中,F为氢氧化钠溶液,可吸收氯气,防止污染空气,可用装有碱石灰(或生石灰)的干燥管代替,
故答案为:增大铜粉与氯气的接触面积;饱和NaCl溶液; 装有碱石灰(或生石灰)的干燥管;
(2)当Cl2排尽空气后,加热A,铜与氯气反应生成氯化铜,化学反应方程式为Cu+Cl2 $\frac{\underline{\;\;△\;\;}}{\;}$CuCl2,
故答案为:Cu+Cl2 $\frac{\underline{\;\;△\;\;}}{\;}$CuCl2;
(3)若实验测得CuCl2质量分数为90.0%,可能含有的杂质是氯化亚铜或单质铜中的一种或两种,也可能混有石棉绒,故答案为:石棉绒(Cu或CuCl);
(4)因为氯化铜是强酸弱碱盐,溶液中存在Cu2++2H2O?Cu(OH)2+2H+,所以溶解时加入HCl溶液,抑制氯化铜的水解,
故答案为:Cu2++2H2O?Cu(OH)2+2H+,加酸抑制Cu2+的水解;
(5)设9.8mol/LH2SO4的体积为VmL,则0.2×0.1+V×9.8×2=10×0.1,解之得V=50ml,体系中存在平衡2Cl- (aq)+CuCl(s)?CuCl32- (aq),是氯离子的浓度过大平衡正向移动,
故答案为:50;c(Cl-) 过大.
点评 本题考查物质的制备实验方案,为高考常见题型,侧重于基础知识的综合应用以及学生的实验能力的考查,题目涉及盐的水解平衡的应用,尾气处理以及反应方程式的书写等,难度中等.

 阅读快车系列答案
阅读快车系列答案| A. | 放热的反应发生时不必加热 | |
| B. | 反应是放热还是吸热必须看反应物和生成物所具有的总能量的相对大小 | |
| C. | 需要加热才能发生的反应一定是吸热反应 | |
| D. | 放热反应在常温下一定很容易发生 |
| A. | 氧化物、化合物 | B. | 盐、电解质 | C. | 溶液、胶体 | D. | 分散系、溶液 |
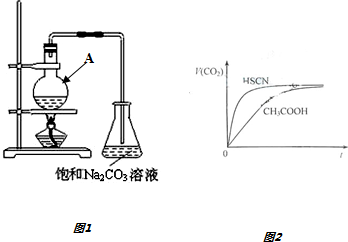
(1)仪器A的名称是圆底烧瓶.往仪器A中加入原料的正确顺序及操作是先加入乙醇,然后边摇动试管边慢慢加入浓硫酸,再加冰醋酸.
(2)在仪器A中生成乙酸乙酯的化学反应方程式为CH3COOH+C2H5OH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O.
(3)欲提高乙酸的转化率,可采取的措施有乙醇过量、及时分离出乙酸乙酯等.
(4)目前对该反应的催化剂进行了新的探索,初步表明质子(H+ )液体可用作该反应的催化剂,且能重复使用.实验数据如下表所示(乙酸和乙醇以等物质的量混合)
| 同一反应时间 | 同一反应温度 | ||||
| 反应温度/℃ | 转化率 (%) | 选择性(%)* | 反应时间/h | 转化率(%) | 选择性 (%)* |
| 40 | 77.8 | 100 | 2 | 80.2 | 100 |
| 60 | 92.3 | 100 | 3 | 87.8 | 100 |
| 80 | 92.6 | 100 | 4 | 92.3 | 100 |
| 120 | 94.5 | 98.7 | 6 | 93.0 | 100 |
| *选择性100%表示反应生成的产物是乙酸乙酯和水 | |||||
A.120℃,4h B.80℃,2h C.60℃,4h D.40℃,3h
(5)常温下,将20mL 0.10mol•L-1 CH3COOH溶液和20mL 10mol•L-1 HSCN溶液分别与20mL 0.10mol•L-1 NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)变化的示意图如图2所示,由图分析:反应初始阶段,两种溶液产生CO2气体的速率存在明显差异的原因是HSCN的酸性比CH3COOH强,其溶液中c(H+)较大,故其溶液与NaHCO3溶液的反应速率快,反应结束后所得两溶液中,c(CH3COO-)<c(SCN-)(填“>”、“<”或“=”)
(6)设计一个简单的实验证明醋酸是弱酸.
Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g)△H=a kJ mol-1
(1)已知:①Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g)△H1=+489.0kJ mol-1
②C(石墨)+CO2(g)=2CO(g)△H2=+172.5kJ mol-1
则a=-28.5kJ mol-1.
(2)冶炼铁反应的平衡常数表达式K=$\frac{{c}^{3}(C{O}_{2})}{{c}^{3}(CO)}$,温度升高后,K值减小(填“增大”、“不变”或“减小”).
(3)在T℃时,该反应的平衡常数K=64,在2L恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡.
| Fe2O3 | CO | Fe | CO21 | |
| 甲/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| 乙/mol | 1.0 | 2.0 | 1.0 | 1.0 |
②下列说法正确的是ac(填字母).
a.若容器内气体密度恒定时,标志反应达到平衡状态 b.甲容器中CO的平衡转化率大于乙的
c.甲、乙容器中,CO的平衡浓度之比为2:3 d.增加Fe2O3可以提高CO的转化率
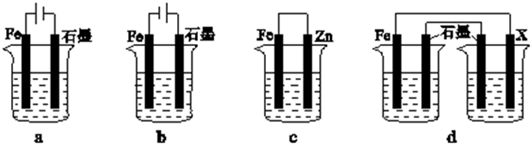
(4)采取一定措施可防止钢铁腐蚀.下列装置中的烧杯里均盛有等浓度、等体积的NaCl溶液.
①在a~c装置中,能保护铁的是bc(填字母).
②若用d装置保护铁,X极的电极材料应是锌(填名称).
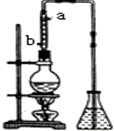 市售乙醛通常为40%左右的乙醛溶液.久置的乙醛溶液会产生分层现象,上层为无色油状液体,下层为水溶液.据测定,上层物质为乙醛的加合物(C2H4O)n,它的沸点比水的沸点高,分子中无醛基.乙醛在溶液中易被氧化,为从变质的乙醛溶液中提取乙醛(仍得到溶液),可利用如下反应原理:(C2H4O)n$\stackrel{{H}^{+}}{→}$n(C2H4O)
市售乙醛通常为40%左右的乙醛溶液.久置的乙醛溶液会产生分层现象,上层为无色油状液体,下层为水溶液.据测定,上层物质为乙醛的加合物(C2H4O)n,它的沸点比水的沸点高,分子中无醛基.乙醛在溶液中易被氧化,为从变质的乙醛溶液中提取乙醛(仍得到溶液),可利用如下反应原理:(C2H4O)n$\stackrel{{H}^{+}}{→}$n(C2H4O)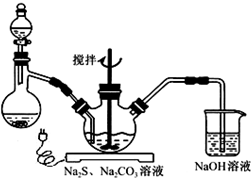 NaCN为剧毒无机物.某化学兴趣小组查阅资料得知,实验室里的氰化钠溶液可使用硫代硫酸钠溶液进行统一解毒销毁,他们开展了以下三个实验,根据要求回答问题:
NaCN为剧毒无机物.某化学兴趣小组查阅资料得知,实验室里的氰化钠溶液可使用硫代硫酸钠溶液进行统一解毒销毁,他们开展了以下三个实验,根据要求回答问题: