题目内容
1.乙酸是一种重要的有机原料,在化工生产和生活中有广泛的用途.某小组组装下列装置如图1由乙醇、冰醋酸和浓硫酸为原料制备乙酸乙酯,回答下列问题.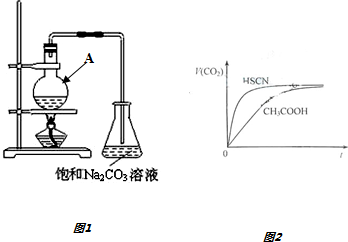
(1)仪器A的名称是圆底烧瓶.往仪器A中加入原料的正确顺序及操作是先加入乙醇,然后边摇动试管边慢慢加入浓硫酸,再加冰醋酸.
(2)在仪器A中生成乙酸乙酯的化学反应方程式为CH3COOH+C2H5OH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O.
(3)欲提高乙酸的转化率,可采取的措施有乙醇过量、及时分离出乙酸乙酯等.
(4)目前对该反应的催化剂进行了新的探索,初步表明质子(H+ )液体可用作该反应的催化剂,且能重复使用.实验数据如下表所示(乙酸和乙醇以等物质的量混合)
| 同一反应时间 | 同一反应温度 | ||||
| 反应温度/℃ | 转化率 (%) | 选择性(%)* | 反应时间/h | 转化率(%) | 选择性 (%)* |
| 40 | 77.8 | 100 | 2 | 80.2 | 100 |
| 60 | 92.3 | 100 | 3 | 87.8 | 100 |
| 80 | 92.6 | 100 | 4 | 92.3 | 100 |
| 120 | 94.5 | 98.7 | 6 | 93.0 | 100 |
| *选择性100%表示反应生成的产物是乙酸乙酯和水 | |||||
A.120℃,4h B.80℃,2h C.60℃,4h D.40℃,3h
(5)常温下,将20mL 0.10mol•L-1 CH3COOH溶液和20mL 10mol•L-1 HSCN溶液分别与20mL 0.10mol•L-1 NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)变化的示意图如图2所示,由图分析:反应初始阶段,两种溶液产生CO2气体的速率存在明显差异的原因是HSCN的酸性比CH3COOH强,其溶液中c(H+)较大,故其溶液与NaHCO3溶液的反应速率快,反应结束后所得两溶液中,c(CH3COO-)<c(SCN-)(填“>”、“<”或“=”)
(6)设计一个简单的实验证明醋酸是弱酸.
分析 (1)根据仪器的特点确定名称;浓硫酸密度大,应将浓硫酸加入到乙醇中,以防酸液飞溅,乙酸易挥发,冷却后再加入乙酸;
(2)酯化反应的本质为酸脱羟基,醇脱氢,该反应生成乙酸乙酯和水,且为可逆反应;
(3)该反应生成乙酸乙酯和水,且为可逆反应,欲提高乙酸的转化率,应改变条件使平衡正向进行分析,两种反应物增大一种量灰提高另一种的转化率,减少生成物浓度促进平衡正向进行;
(4)根据表中数据分析温度转化率的影响,选择最佳的温度和反应时间;
(5)由生成二氧化碳的曲线斜率可知HSCN反应较快,则可知HSCN中中c(H+)较大,说明HSCN酸性较强,再利用盐类水解的规律来分析离子浓度的关系;
(6)根据醋酸的电离平衡移动的影响因素来回答判断即可,若加入的物质影响醋酸离子的浓度,同时还会引起氢离子的浓度变化,则说明存在电离平衡,醋酸是弱酸.
解答 解:(1)仪器A的名称是圆底烧瓶,为防止酸液飞溅,应将密度大的液体加入到密度小的液体中,乙酸易挥发,冷却后再加入乙酸,
故答案为:圆底烧瓶;先加入乙醇,然后边摇动试管边慢慢加入浓硫酸,再加冰醋酸;
(2)酯化反应的本质为酸脱羟基,醇脱氢,乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,该反应为可逆反应,化学方程式为:CH3COOH+C2H5OH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O,
故答案为:CH3COOH+C2H5OH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O,
(3)CH3COOH+C2H5OH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O反应是可逆反应,欲提高乙酸的转化率可以增加乙醇的量,平衡正向进行,乙酸转化率增大,也可以分离出乙酸乙酯,促进平衡正向进行,增大乙酸的转化率等,
故答案为:乙醇过量、及时分离出乙酸乙酯等;
(4)由表格中的同一反应时间来看,60℃时反应的转化率已经较高,且选择性为100%,同一温度时反应时间选择4小时转化率较高,
故选C;
(5)由Ka(CH3COOH)=1.8×10-5和Ka(HSCN)=0.13可知,CH3COOH的酸性弱于HSCN的,即在相同浓度的情况下HSCN溶液中H+的浓度大于CH3COOH溶液中H+的浓度,浓度越大反应速率越快;又酸越弱,反应生成的相应的钠盐越易水解,即c(CH3COO-)<c(SCN-),
故答案为:HSCN的酸性比CH3COOH强,其溶液中c(H+)较大,故其溶液与NaHCO3溶液的反应速率快;<;
(6)在醋酸溶液中滴加石蕊试液,溶液变红色,证明醋酸能电离出H+;在上述溶液中加入少量的CH3COONH4晶体,振荡溶液,溶液颜色变浅,说明c(H+)变小,证明醋酸溶液中存在CH3COOH?CH3COO-+H+的电离平衡.(注意:用CH3COONH4晶体而不是用CH3COONa晶体,是因为CH3COONH4在溶液中呈中性,故选择之).
答:在醋酸溶液中滴加石蕊试液,溶液变红色,证明醋酸能电离出H+;在上述溶液中加入少量的CH3COONH4晶体,振荡溶液,溶液颜色变浅,说明c(H+)变小,证明醋酸溶液中存在电离平衡,醋酸是弱酸.
点评 本题考查了乙酸乙酯的制备方法、可逆反应特点,题目难度中等,注意掌握乙酸乙酯的反应原理及制备方法,明确可逆反应特点,浓硫酸、饱和碳酸钠溶液、长导管在酯化反应中的作用为考查的热点,要求学生熟练掌握.

| X | Y |
| Z |
| A. | 气态氢化物的沸点:X<Y<Z | |
| B. | 最高正化合价:Y>X | |
| C. | X、Y、Z的最高价氧化物对应水化物中,Z的酸性最强 | |
| D. | 若X、Y、Z的原子序数之和等于25,则它们都是非金属元素 |
| A. | 浓硝酸存放在带橡胶塞的棕色玻璃瓶中 | |
| B. | 四氯化碳萃取溴水中的溴时,水从分液漏斗下口流出 | |
| C. | 红热的铜丝在氯气中剧烈燃烧,生成棕黄色的烟 | |
| D. | 某溶液中滴加BaCl2溶液,产生不溶于稀硝酸的白色沉淀,该溶液中一定含有Ag+ |
| A. | 分散质粒子的直径在1~100 nm之间的微粒称为胶体 | |
| B. | 电泳现象可证明胶体属于电解质溶液 | |
| C. | 利用丁达尔效应可以区别溶液与胶体 | |
| D. | Fe(OH)3胶体带正电荷,可以产生电泳现象 |
| A. | 2H2(g)+O2(g)=2H2O(l)△H1 | B. | C(s)+$\frac{1}{2}$O2(g)=CO(g)△H2 | ||
| C. | HCl(aq)+NaOH(aq)=NaCl(aq)+H2O( l )△H3 | D. | C6H12O6(s)+6O2(g)=6CO2(g)+6H2O( l )△H4 |
下表是该反应在不同温度下的化学平衡常数(K):
| 温度/℃ | 250 | 310 | 350 |
| K | 2.041 | 0.250 | 0.012 |
(2)某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应达到平衡后,测得c(CO)=0.5mol•L-1,则此时的温度为310℃.
(3)在容积固定的密闭容器中发生上述反应,各物质的浓度如下表:
| 时间/min/浓度mol/L | c(CO) | c(H2) | c(CH3OH) |
| 0 | 0.8 | 1.6 | 0 |
| 2 | 0.6 | 1.2 | 0.2 |
| 4 | 0.3 | 0.6 | 0.5 |
| 6 | 0.3 | 0.6 | 0.5 |
②反应达到平衡时CO的转化率为62.5%.
③反应在第2min时改变了反应条件,改变的条件可能是A(填序号).
A.使用催化剂 B.降低温度 C.增加H2的浓度
(4)向容积相同、温度分别为T1和T2的两个密闭容器中均充入1 molCO和2mol H2,发生反应CO(g)+2 H2(g)?CH3OH(g)△H=a kJ/mol.恒温恒容下反应相同时间后,分别测得体系中CO的百分含量分别为w1和w2;
已知T1<T2,则ω1Dω2(填序号).
A.大于 B.小于 C.等于 D.以上都有可能.
| A. | 2.4 g金属镁变为镁离子时失去的电子数为0.1NA | |
| B. | 1 mol HCl气体中的粒子数与0.5 mol/L盐酸中溶质粒子数相等 | |
| C. | 在标准状况下,22.4 L CH4与18 g H2O所含有电子数均为10NA | |
| D. | CO和N2为等电子体,22.4 L的CO气体与1 mol N2所含的电子数相等 |
| A. | 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 | |
| B. | 容量瓶检漏的操作是:在容量瓶中注入适量的水,塞上玻璃瓶塞,左手五指托住瓶底,右手食指顶住瓶塞,倒置,观察是否漏水 | |
| C. | 在分液漏斗中分离两种液体时,要先从下端放出密度较大的液体,关闭活塞,取另一只烧杯后打开活塞再放出密度较小的液体 | |
| D. | 蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 |
